Компоненты крови: описание и показание к применению. Цельная кровь это Компоненты цельной крови
Компоненты крови, показания к их применению.
Эритроцитная масса (эритроциты и неболь-шое кол-во консерванта и стабилизатора);
Эритроцитная взвесь (эритроцитная масса в ресуспендирующем растворе – эритронаф или эритроцифонит );
Размороженные и отмытые эритроциты;
Плазма (нативная, сухая, свежезаморожен-ная);
Повышение онкотического давления крови;
2. Повышение ОЦК;
3. Повышение содержания белка в крови;
4. Дезинтоксикационное действие;
5. Стимулирование диуреза.
Препараты крови, показания к их применению
Посттрансфузионные реакции при переливании крови, их профилактика и лечение.
Посттрансфузионные осложнения при переливании крови, профилактика и лечение.
В целях профилактики пирогенных и аллергических реакций у больных с изосенсибилизацией к антигенам HLA, лейкоцитарным или тромбоцитарным антигенам необходимо использовать отмытые донорские эритроциты, концентраты тромбоцитов, лейкоцитную массу, подобранные с учетом специфичности антител у реципиента. Пациентам, сенсибилизированным множественными гемотрансфузиями, рекомендуется проводить перед переливанием медикаментозную антигистаминную премедикацию препаратами, предупреждающими проявление аллергических реакций.
Профилактика гемотрансфузионных реакций включает:
1) строгое выполнение всех требований и условий по заготовке, хранению и переливанию консервированной крови, ее компонентов и препаратов;
2) применение систем одноразового использования;
3) тщательный сбор трансфузионного и акушерского анамнеза:
• количество предшествующих трансфузий;
• интервал между ними;
• вид трансфузионного раствора;
• через сколько времени после трансфузии была реакция и ее характер (повышение температуры на 0,5—2,0 °С, мышечные боли, удушье, отеки, кожная сыпь, одышка);
• признаки посттрансфузионного гемолитического осложнения (желтушность кожи и слизистых, темный цвет мочи, боли в пояснице, животе, за грудиной);
• количество беременностей, родов, ранних выкидышей, антенатальной гибели плода, гемолитической болезни новорожденных;
4) определение групповой и резус-принадлежности врачом и в лаборатории. Скрининг антител в лаборатории;
5) определение показания для применения донорской крови и ее компонентов;
6) проведение контрольных исследований групп крови больного и донора. Постановка проб на совместимость.
Во время трансфузии:.
1) трансфузии (за исключением экстренных) должны производиться капельным методом или со скоростью 500 мл/ч;
2) биологическая проба;
3) во время гемотрансфузии за больным устанавливается наблюдение со стороны врача или среднего медицинского персонала для своевременного выявления клинических проявлений посттрансфузионных реакций или осложнений.
1) наблюдение за больным в течение 24 ч после трансфузии:
• на протяжении первых 2 ч после окончания переливания регистрируют температуру тела и артериальное давление;
• каждый час: объем, цвет первой порции мочи, суточный диурез. Возникшую посттрансфузионную реакцию или осложнение врач записывает в историю болезни/родов;
2) мешок или флакон с остатком (не менее 10 мл) гемотрансфузионной среды с этикеткой хранят 48 ч, а пробирку с кровью больного, взятую до переливания, хранят в течение 7 дней в холодильнике при +2—6 °С;
3) каждая трансфузия записывается в:
• журнал регистрации переливания трансфузионных сред, форма 009/у (приказ МЗ СССР № 1030 от 04.10.80);
• историю болезни/родов в виде протокола или в листке регистрации переливания трансфузионных сред, форма 005/у (приказ МЗ СССР № 1030 от 04.10.80).
Посттрансфузионные реакции. Трансфузионная терапия в подавляющем большинстве случаев не сопровождается реакциями. Однако у некоторых больных во время или вскоре после трансфузии развиваются реактивные проявления, которые в отличие от осложнений не сопровождаются серьезными и длительными нарушениями функции органов и систем, встречаются у 1 —3 % больных. При возникновении реакций и осложнений врач, проводящий гемотрансфузию, обязан немедленно прекратить переливание, не удаляя иглу из вены.
Больных, у которых возникли посттрансфузионные реакции, должны обязательно наблюдать врач и фельдшер и необходимо своевременно лечить. В зависимости от причины возникновения и клинических проявлений различают пирогенные, аллергические и анафилактические реакции.
Пирогенные реакции. Такие реакции обычно начинаются через 20 — 30 мин после трансфузии и продолжаются от нескольких минут до нескольких часов. Они проявляются в основном общим недомоганием, лихорадкой и ознобом. При тяжелых реакциях температура тела повышается более чем на 2 °С, появляются потрясающий озноб, цианоз губ, сильная головная боль.
Легкие реакции обычно проходят без лечения. При средних и тяжелых реакциях больного необходимо согреть, накрыв теплым одеялом, под ноги положить грелку, дать выпить крепкий горячий чай или кофе. При высокой гипертермии вводятся гипосенси-билизирующие, жаропонижающие препараты, литические смеси, промедол.
Аллергические реакции. Эти реакции появляются спустя несколько минут от начала трансфузии. В клинической картине преобладают симптомы аллергического характера: одышка, удушье, тошнота, рвота. Появляются зуд кожи, крапивница, отеки Квинке. В крови обнаруживается лейкоцитоз с эозинофилией. Указанные симптомы могут сочетаться с общими признаками лихорадочного состояния.
Для лечения применяются антигистаминные, гипосенсибили-зирующие средства, при необходимости — промедол, глюкокортикоиды, сердечно-сосудистые средства.
Анафилактические реакции. В редких случаях гемотрансфузии могут явиться причиной развития реакций анафилактического типа. Клиническая картина характеризуется острыми вазомоторными расстройствами: беспокойством больного, покраснением лица, цианозом, удушьем, эритематозной сыпью; учащается пульс, АД снижается. Часто реактивные проявления быстро купируются.
Иногда может развиться тяжелое осложнение — анафилактический шок, требующий немедленной интенсивной терапии. Течение анафилактического шока острое. Он развивается во время трансфузии или в первые минуты после нее. Больные беспокойны, жалуются на затрудненное дыхание. Кожные покровы обычно гиперемированы. Появляются цианоз слизистых оболочек, акроцианоз, выступает холодный пот. Дыхание шумное, свистящее, слышное на расстоянии (бронхоспазм). Артериальное давление очень низкое или не определяется аускультативным методом, тоны сердца глухие, и легких при перкуссии выслушивается коробочный оттенок перкуторного тона, при аускультации — свистящие сухие хрипы. Может развиться отек легких с клокочущим дыханием, кашлем с выделением пенистой розовой мокроты. При этом выслушиваются разнокалиберные влажные хрипы над всей поверхностью легких.
Проводится полная противошоковая терапия. Применяются кортикостероиды внутривенно, реополиглюкин, сердечно-сосудистые, антигистаминные средства, проводится купирование бронхо- и ларингоспазма. Острый отек гортани с асфиксией служит показанием к срочной трахеостомии. При нарастании процесса и прогрессировании дыхательной недостаточности больного переводят на искусственную вентиляцию легких (ИВЛ). При судорогах проводится противосудорожная терапия. Корректируют водно-электролитные нарушения и стимулируют диурез. При необходимости проводят реанимационные мероприятия в полном объеме.
Посттрансфузионные осложнения. В отличие от посттрансфузионных реакций посттрансфузионные осложнения представляют опасность для жизни больного, так как нарушается деятельность жизненно важных органов и систем. Осложнения могут быть связаны с несовместимостью по системе АВ0 или резус-фактору, недоброкачественностью перелитых компонентов крови, состоянием организма реципиента, неучтенными противопоказаниями к гемотрансфузии, техническими погрешностями при выполнении гемотрансфузии. В профилактике посттрансфузионных осложнений ведущая роль принадлежит организационным мероприятиям, тщательному соблюдению соответствующих инструкций и приказов.
Осложнения, связанные с переливанием несовместимых компонентов крови. Чаще всего первым и грозным признаком наступившего осложнения является гемотрансфузионный шок. Он может развиться уже во время проведения биологической пробы, во время трансфузии или в ближайшие минуты и часы после нее. Наиболее ранний и характерный признак гемотрансфузионного шока — остро наступающее расстройство кровообращения и дыхания. В отличие от несовместимости по системе АВО резус-несовместимость характеризуется поздним проявлением симптомов и стертостью клинической картины шока. Также реактивные проявления и симптомы шока бывают выражены незначительно при переливании несовместимой крови больным, находящимся под наркозом, получающим глюкокортикоидные гормоны или лучевую терапию.
Длительность шока в большинстве случаев превышает 1 ч. Нередко в первые часы или даже сутки после трансфузии единственным симптомом несовместимости перелитой крови является острый внутрисосудистый гемолиз, который проявляется симптомами гемолитической желтухи и в среднем продолжается 1 — 2 сут, в тяжелых случаях до 3 —6 сут. степень гемолиза нарастает с увеличением дозы перелитой несовместимой крови.
Особенно выражен гемолиз при переливании резус-несовместимой крови.
Наряду с симптомами шока и острого гемолиза, к характерным признакам гемотрансфузионного осложнения относится серьезное нарушение в свертывающей системе крови — ДВС-синдром.
Наступающие в результате переливания несовместимой крови шок, острый гемолиз, ишемия почек приводят к развитию острой почечной недостаточности. Если купируются явления гемотрансфузионного шока, вслед за кратковременным периодом относительно спокойного состояния больного с 1 — 2-х суток заболевания уже выявляются нарушения функции почек. Наступает олигурический, а затем — анурический период острой почечной недостаточности. Длительность олигоанурического периода варьирует от 3 до 30 сут и более, чаще 9—15 сут. Затем в течение 2 — 3 недель диурез восстанавливается.
Лечение гемотрансфузионного шока начинается немедленно после установления диагноза. Оно должно быть направлено на решение двух задач: 1) терапия гемотрансфузионного шока; 2) терапия и профилактика органных поражений, прежде всего почек и ДВС-синдрома.
Полностью меняется система для вливания. Порядок введения, выбор и дозировки лекарственных средств зависят от тяжести шока и расписаны в специальных методических указаниях.
Очень эффективно проведение неотложного плазмафереза с удалением не менее 1,3—1,8 л плазмы, содержащей патологические вещества. При необходимости плазмаферез повторяют через 8— 12 ч. Возмещение объема удаленной плазмы проводится переливаниями альбумина, свежезамороженной плазмы и кристаллоидных растворов.
Проводится профилактика и лечение нарушений свертывания крови и острой почечной недостаточности.
Посттрансфузионные осложнения, вызванные недоброкачественностью перелитой крови. Бактериальное загрязнение. Инфицирование компонента крови может произойти на любом этапе технологического процесса, а также в лечебном учреждении при нарушениях требований асептики и антисептики.
При переливании инфицированного компонента крови развивается бактериальный шок с быстрым летальным исходом. В других случаях наблюдаются явления тяжелого токсикоза. Бактериальный шок проявляется развитием у больного резчайшего озноба, высокой температуры, тахикардии, тяжелой гипотонии, цианоза, судорог. Отмечаются возбуждение, затемнение сознания, рвота, непроизвольная дефекация.
Данное осложнение возможно лишь при грубейших нарушениях организации гемотрансфузии в отделении и правил хранения компонентов крови. У всех больных развивается шок и острый внутрисосудистый гемолиз. В дальнейшем возникают токсический гепатит и острая почечная недостаточность.
Нарушение температурного режима хранения компонентов крови. Переливание перегретых компонентов крови происходит чаще всего в результате применения неправильных методов согревания компонентов крови перед переливанием, размораживания плазмы, а также при несоблюдении температурного режима хранения компонентов крови. При этом наблюдаются денатурация белков и гемолиз эритроцитов. Развивается шок с явлениями резкой интоксикации, развитием ДВС-синдрома и острой почечной недостаточности.
Переливание «подмороженных» эритроцитов может произойти при грубом нарушении температурного режима хранения. При замораживании происходит гемолиз эритроцитов. У больного развиваются острый внутрисосудистый гемолиз, ДВС-синдром и острая почечная недостаточность.
Осложнения, связанные с техническими погрешностями при выполнении гемотрансфузии. Воздушная эмболия. В результате попадания воздуха (достаточно 2 — 3 мл) в вену больного из-за технических погрешностей в выполнении гемотрансфузии возникает воздушная эмболия. Особенно опасно попадание воздуха в центральные вены через катетер. Причинами этого могут быть неправильное заполнение кровью системы для переливания, дефект системы (негерметичность, приводящая к «подсосу» воздуха в магистраль), попадание воздуха в конце трансфузии из-за несвоевременного отключения системы.
Тромбоэмболия. Из-за отрыва венозного тромба и попадания его в артериальное русло (головной мозг, легкие, почки) возникает тромбоэмболия. Сгустки крови могут попасть в вену больного из-за переливания через систему без фильтра. Острые нарушения сердечной деятельности. При быстром вливании больших объемов жидкостей на фоне сердечной слабости могут проявляться острые нарушения сердечной деятельности. О них свидетельствуют симптомы острой сердечной недостаточности — сердечная астма, отек легких, инфаркт миокарда.
Калиевая и цитратная интоксикации. При переливании больших объемов цельной консервированной крови, стабилизированной нитратными гемоконсервантами, возникает калиевая и цитратная интоксикация. Для профилактики достаточно ввести 10 мл 10 % раствора СаС12 на каждые 500 мл консервированной крови.
Дата добавления: 2018-05-12 ; просмотров: 482 ;
Компоненты и препараты крови
А. Цельная кровь. Консервант — цитроглюкофосфат-аденин. Максимальный срок хранения — 42 сут. Кровь — драгоценный продукт и требует бережного отношения. Цельную кровь сейчас используют редко, поскольку переливание ее отдельных компонентов более эффективно. Тромбоциты и нестабильные факторы свертывания в консервированной крови быстро теряют свои свойства, что значительно снижает ее ценность. Свежая кровь сохраняет все свои качества, однако современные требования к проверке донорской крови делают ее использование практически невозможным. Поэтому при угрожающих жизни кровотечениях переливают эритроцитарную массу, ресуспендированную в физиологическом растворе, и, в зависимости от показаний, другие компоненты крови. При введении больших объемов крови в короткие сроки для предупреждения объемной перегрузки переливание проводят под контролем ЦВД или ДЗЛА.
Б. Концентраты эритроцитов — препараты выбора при профузных кровотечениях. Объем одной дозы эритроцитарной массы составляет 250—350 мл (гематокрит — 50—80%). Существует три вида концентратов: эритроцитарная масса, замороженные эритроциты, отмытые эритроциты. Переливание одной дозы эритроцитарной массы повышает гематокрит реципиента на 3—4%. Эритроцитарную массу не применяют для ускорения заживления ран, «улучшения самочувствия» и вместо препаратов железа. Замороженные эритроциты прекрасно сохраняют способность к переносу кислорода, однако их применение ограничено высокой стоимостью (одна доза стоит на 40 долларов дороже). Замороженные эритроциты используют главным образом для пополнения банков редких групп крови, для отсроченных аутогемотрансфузий и для получения отмытых эритроцитов, полностью свободных от лейкоцитов, тромбоцитов и сывороточных белков. FDA разрешает хранить замороженные эритроциты в течение 10 лет. После размораживания клетки используют в течение 24 ч. Отмытые эритроциты стоят еще дороже (на 10 долларов за дозу) и в повседневной практике не используются. Больные, у которых переливание крови осложняется пирогенными негемолитическими реакциями, как правило, сенсибилизированы к поверхностным антигенам тромбоцитов и гранулоцитов. Переливание отмытых эритроцитов (или использование специальных лейкоцитарных фильтров) позволяет избежать этого осложнения.
В. Альбумин поступает в продажу в виде 5% и 25% раствора в 0,9% NaCl. Кроме того, выпускается белковая фракция плазмы (Плазманат), содержащая 88% альбумина и 12% глобулина. Для инактивации вирусов все препараты альбумина пастеризуют при 60°C в течение 10 ч. Сообщалось о нескольких случаях артериальной гипотонии при переливании белковой фракции плазмы, по-видимому, из-за присутствия в ней активатора прекалликреина. Частота этого осложнения при использовании современных препаратов альбумина сравнительно невелика. Принято считать, что препараты альбумина содержат мало солей, тем не менее концентрация натрия в них достигает 145 мэкв/л. Вопрос о преимуществах альбумина перед солевыми растворами остается спорным. Большинство клиник и травматологических центров предпочитает солевые растворы как более дешевые.
Г. Тромбоцитарная масса. Если в крови больного содержится более 75 000 мкл–1 полноценных тромбоцитов, то свертывание, как правило, не нарушено. Инвазивные исследования у больных с содержанием тромбоцитов менее 50 000 мкл–1 могут сопровождаться кровотечением. При снижении количества тромбоцитов до 30 000 мкл–1 и ниже возникают спонтанные кровотечения. При врожденных и приобретенных тромбоцитопатиях (например, при лечении аспирином) кровотечения возникают даже при нормальном содержании тромбоцитов. Одна доза тромбоцитарной массы содержит 50—100 млрд клеток в 50—70 мл плазмы. При тромбаферезе от донора получают 300—500 млрд тромбоцитов в 200—400 мл плазмы, что соответствует 6 дозам. Переливание одной дозы тромбоцитарной массы повышает содержание тромбоцитов в крови на 5000—10 000 мкл–1. Основное препятствие для использования тромбоцитарной массы — наличие в крови реципиента антитромбоцитарных антител, разрушающих донорские тромбоциты.
Д. Свежезамороженная плазма содержит все факторы свертывания, стабильные и нестабильные. В свежезамороженной плазме нет тромбоцитов, а содержание фибриногена относительно невелико. Показания к применению:
1. Дефицит антитромбина III.
2. Болезни печени, сопровождающиеся нарушениями синтеза факторов свертывания и кровоточивостью.
3. Передозировка непрямых антикоагулянтов.
4. Обменное или массивное переливание крови при коагулопатии или продолжающемся кровотечении (в дополнение к эритроцитарной массе).
6. Кровотечение или предстоящее инвазивное исследование у больных с выраженным дефицитом факторов свертывания II, V, VII, IX, X, XI или XIII.
Свежезамороженную плазму не используют для восстановления ОЦК, парентерального питания и в профилактических целях после массивных переливаний крови и операций с применением АИК.
Е. Криопреципитат. При оттаивании свежезамороженной плазмы на холоде образуется белый студенистый осадок, богатый факторами свертывания VIII, XIII, фибриногеном, фибронектином. Криопреципитат лиофилизируют и подвергают тепловой обработке для инактивации вирусов. Применяют при дефиците фактора свертывания VIII (гемофилия A); болезни фон Виллебранда (при неэффективности лечения десмопрессином ); дисфибриногенемиях, уремической тромбоцитопатии (при неэффективности лечения десмопрессином); дефиците фактора свертывания XIII; ДВС-синдроме.
Ж. Фибриноген. Применение человеческого фибриногена в настоящее время прекращено из-за чрезвычайно высокого риска заражения вирусным гепатитом. Для восполнения дефицита фибриногена используют криопреципитат.
З. Концентраты факторов свертывания. До 60-х годов для лечения дефицита факторов свертывания VIII и IX использовали только свежезамороженную плазму. С 1965 г. стали применять криопреципитат. В начале 70-х годов началось производство концентратов факторов свертывания. Больные гемофилией получили возможность самостоятельно использовать эти концентраты в домашних условиях, что значительно облегчило их жизнь. К сожалению, одновременно увеличился риск заражения вирусным гепатитом (до 90%); даже тепловая обработка сухих концентратов при 60°C в течение 72 ч не устраняла полностью угрозу инфекционных осложнений. У значительной части реципиентов обнаружили антитела к ВИЧ. Новые методы обработки концентратов позволили решить эту проблему. С 1 января 1990 г. не было зарегистрировано ни одного случая заражения ВИЧ при использовании концентратов факторов свертывания. В настоящее время разрабатываются методы получения рекомбинантных факторов свертывания.
И. Кровь «универсального» донора
Клетки крови группы 0(I) не имеют поверхностных антигенов A и B, поэтому доноров с этой группой крови называют «универсальными». Доказано, что переливание крови группы 0(I) относительно безопасно и оправдано в экстренных ситуациях, когда кровь требуемой группы или кровь, проверенная на индивидуальную совместимость, недоступна. Проведены сотни переливаний крови группы 0(I) (в основном при травмах), гемолитических трансфузионных реакций не отмечено. Риск сенсибилизации реципиента составляет 6%.
К. Другие препараты
1. Десмопрессин (1-дезамино-8-D-аргининвазопрессин) — синтетический аналог АДГ, нашедший широкое применение в терапии коагулопатий. Он вызывает дозозависимое ускорение всех реакций, катализируемых фактором свертывания VIII. Десмопрессин — препарат выбора в лечении легких форм гемофилии A и нарушений гемостаза при уремии. Дозу 0,3 мкг/кг вводят в течение 15—30 мин.
2. Препараты эритропоэтина (эпоэтин альфа, эпоэтин бета) производят биотехнологическими методами. Они стимулируют эритропоэз, но терапевтический эффект наступает не сразу, поэтому для лечения острых анемий их не применяют. Назначают в дозе 50—100 ед/кг 3 раза в неделю.
3. Апротинин — ингибитор протеаз (трипсина, плазмина, калликреина), в низких концентрациях угнетает фибринолиз. Полагают, что апротинин можно использовать для профилактики кровотечений после операций с применением АИК. Ведутся клинические испытания.
III. Экспериментальные кровезаменители. Поскольку переливание крови и ее компонентов не является абсолютно безопасным, ведутся поиски «идеальных» кровезаменителей, способных переносить кислород. Все эти препараты находятся на стадии доклинических или клинических испытаний.
А. Фторуглероды. Флюосол (20% эмульсия) — фторированный углеводород; кислород растворяется в нем в 10—20 раз лучше, чем в воде. Подобными свойствами обладают все фторуглероды. Однако сами они в воде нерастворимы и используются в виде эмульсии, что снижает их сродство к кислороду. В отличие от S-образной кривой диссоциации оксигемоглобина, кривая диссоциации оксифторуглеродов линейна. T1/2 флюосола при введении максимальной дозы (40 мл/кг) составляет всего 24 ч. При легкой или умеренной анемии его применение нецелесообразно, при тяжелой — неэффективно. Ведутся дальнейшие исследования.
Б. Очищенный гемоглобин получают из гемолизата эритроцитов путем очистки от стромальных белков. Препарат содержит 7 г% гемоглобина и обладает сродством к кислороду, в два раза большим, чем нативный гемоглобин. О сродстве гемоглобина к кислороду судят по величине P50 (paO2, при котором 50% гемоглобина насыщено кислородом). Для очищенног гемоглобина P50 составляет 12—14 мм рт. ст. Кроме того, поскольку препарат не содержит эритроцитов, он не увеличивает вязкости крови и позволяет снизить сердечный выброс, среднее АД и потребление кислорода. Препарат проходит испытания.
В. Пиридоксилированный полимер гемоглобина. Коллоидно-онкотические свойства препарата, концентрация гемоглобина (14 г%) и P50 — такие же, как у крови. T1/2 препарата в организме составляет 40—48 ч, он лишен недостатков очищенного гемоглобина. Препарат активно изучается.
IV. Варианты трансфузионной терапии
А. Отказ от переливания крови. По мере углубления наших знаний физиологии понятие «сигнал к началу переливания крови» утратило свое значение. Уровень гемоглобина ниже 100 г/л уже давно не считается достаточным показанием к переливанию крови. Здоровый человек без особых последствий переносит потерю 20% крови, если ее возместить солевыми растворами. Показания к переливанию крови и ее компонентов должны определяться самым тщательным образом.
Б. Аутогемотрансфузия (рис) — переливание больному его собственной крови, полученной заблаговременно. Каждые 72 ч берут 1 дозу крови, последнюю — не позже чем за 72 ч до операции; при этом гематокрит не должен быть менее 33%. Заготовку крови можно начинать за 6 нед до операции (максимальный срок хранения консервированной крови). Больному назначают препараты железа. Если необходимо сократить интервалы между взятием крови, назначают препараты эритропоэтина.
С. Реинфузия крови (рис). Показания: большая (1 л и более): 1) операционная, послеоперационная, 2) посттравматическая кровопотеря (травма селезенки, печени, почек), 3) внематочная беременность, 4) кровотечения во внутренние полости организма.
Противопоказания: 1) гнойное загрязнение излившейся крови; 2) загрязнение излившейся крови толстокишечным содержимым; 3) операция по поводу злокачественных опухолей; 4) почечная недостаточность.
Реинфузия крови из закрытых серозных полостей (плевральная полость, полость перикарда, брюшинная полость) в связи с возможным гемолизом и инфицированием ( при длительном пребывании – свыше суток) возможно только после проведения пробы на гемолиз (проба И.С. Колесникова): разведение в пробирке 1 мл крови в 20 мл изотонического раствора натрия хлорида. После центрифугирования или отстаивания содержимого пробирки производится визуальная оценка пробы. Появление желто-розового окрашивания надосадочной жидкости указывает на выраженный гемолиз и непригодность крови для реинфузии.

Рисунок 39 Методика сбора крови с операционного поля
Отсасывание крови из операционной раны осуществляют за счет регулируемого в границах 60-150 мм рт ст разряжения, создаваемого в флаконе с гемоконсервантом (глюгицир – 1 мл на 4 мл крови, либо гепарин 500 ЕД на 1000 мл собираемой крови) вакуум-отсосом. Дозировка поступления жидкости в наконечник отсоса (реополиглюкин, физраствор)

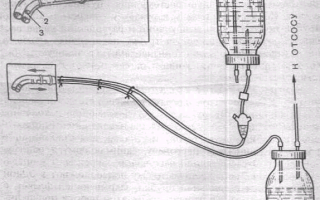
Рисунок 40 Периливание крови при ее реинфузии
При работе представленной системы последовательно происходит: 1) открытое предварительное фильтрование реинфузируемой крови через 4 слоя марли;
2) накопление крови во флаконе после промежуточной фильтрации;
3) переливание крови в вену больного с одновременной микрофильтрацией через фильтр капельницы.
Компоненты крови: описание и показание к применению
Цельная кровь состоит из клеточного и бесклеточного компонентов. Клеточный компонент включает в себя эритроциты, лейкоциты и тромбоциты. Бесклеточные компоненты крови включают в себя альбумин, плазменную фракцию белка (ПФБ), свежезамороженную плазму (СЗП), криопреципитат и другие растворенные в плазме факторы свертывания. Переливание отдельных компонентов крови предпочтительно (в сравнении с трансфузией цельной крови) при коррекции специфического физиологического дефицита; к тому же оно экономичнее.
Врачу ОНП чаще всего приходится прибегать к переливанию эритроцитарной массы; значительно реже используются концентраты свежезамороженных факторов свертывания крови, тромбоцитарная масса, альбумин и ПБФ. Трансфузия цельной крови в настоящее время применяется редко, обычно только у детей младенческого возраста.
Переливание всех компонентов крови, кроме химически и термически обработанных (альбумин, ПБФ), сопряжено с риском заражения гепатитом. При трансфузии возможна передача и других инфекционных заболеваний, включая СПИД. Потенциальными осложнениями трансфузии являются реакции несовместимости и изоиммунизации, а также аллергические и токсические реакции.
Цельная кровь
Даже цельная кровь в момент ее введения уже не является действительно цельной. Уже через сутки после ее хранения в растворе цитрат-фосфат-декстрозы (ЦФД) или цитрат-фосфат-декстроза-аденина (ЦФДА) при 4’С в ней отсутствуют функционируюшие гранулоциты; остается лишь 50 % функциональной активности тромбоцитов и VIII фактора свертывания. После 72-часового хранения цельной крови активность обоих компонентов становится ничтожной.
Длительное хранение замороженной крови приводит к потере 50 % активности фактора V на 3–5-й день и к повышению сродства гемоглобина к кислороду на 4–6-й день при одновременном уменьшении жизнеспособности эритроцитов, а также их способности к деформированию. Примерно на 5-й день хранения возрастает концентрация водородных ионов, аммиака и калия, что способствует микроагрегации тромбоцитов и фибрина, а также быстрому скоплению лейкоцитов. Пригодность депонированных продуктов крови стандартно оценивается по наличию, по крайней мере, 70 % жизнеспособных эритроцитов через 24 ч после трансфузии. Этот стандарт удовлетворяется при хранении крови с ЦФД-буфером не более 21 дня, а с ЦФДА-1 — не более 35 дней. Уменьшение способности эритроцитов видоизменять свою форму ограничивает возможность их прохождения через тканевые капилляры, а повышение их сродства к кислороду способствует уменьшению оксигенации тканей. Эти последние эффекты исчезают через 24–48 ч после возвращения эритроцитов в более “естественную” среду циркуляторного русла. Недостатки переливания цельной крови включают следующее: ограничение концентрации лабильных факторов свертывания; избыточное накопление побочных продуктов метаболизма; перегрузку объемом; загрязнение вирусами или бактериями; антигенные воздействия. В тех случаях, когда необходимо замещение объема и массы эритроцитов, обычно вполне достаточно введения концентратов эритроцитов и кристаллоидных растворов. Однако при массивной трансфузии лучше использовать (если позволяют возможности) свежую цельную кровь; дополнительную пользу в таких случаях может принести и гемоаутотрансфузия.
Компоненты и препараты крови
А. Цельная кровь. Консервант — цитроглюкофосфат-аденин. Максимальный срок хранения — 42 сут. Кровь — драгоценный продукт и требует бережного отношения. Цельную кровь сейчас используют редко, поскольку переливание ее отдельных компонентов более эффективно. Тромбоциты и нестабильные факторы свертывания в консервированной крови быстро теряют свои свойства, что значительно снижает ее ценность. Свежая кровь сохраняет все свои качества, однако современные требования к проверке донорской крови делают ее использование практически невозможным. Поэтому при угрожающих жизни кровотечениях переливают эритроцитарную массу, ресуспендированную в физиологическом растворе, и, в зависимости от показаний, другие компоненты крови. При введении больших объемов крови в короткие сроки для предупреждения объемной перегрузки переливание проводят под контролем ЦВД или ДЗЛА.
Б. Концентраты эритроцитов — препараты выбора при профузных кровотечениях. Объем одной дозы эритроцитарной массы составляет 250—350 мл (гематокрит — 50—80%). Существует три вида концентратов: эритроцитарная масса, замороженные эритроциты, отмытые эритроциты. Переливание одной дозы эритроцитарной массы повышает гематокрит реципиента на 3—4%. Эритроцитарную массу не применяют для ускорения заживления ран, «улучшения самочувствия» и вместо препаратов железа. Замороженные эритроциты прекрасно сохраняют способность к переносу кислорода, однако их применение ограничено высокой стоимостью (одна доза стоит на 40 долларов дороже). Замороженные эритроциты используют главным образом для пополнения банков редких групп крови, для отсроченных аутогемотрансфузий и для получения отмытых эритроцитов, полностью свободных от лейкоцитов, тромбоцитов и сывороточных белков. FDA разрешает хранить замороженные эритроциты в течение 10 лет. После размораживания клетки используют в течение 24 ч. Отмытые эритроциты стоят еще дороже (на 10 долларов за дозу) и в повседневной практике не используются. Больные, у которых переливание крови осложняется пирогенными негемолитическими реакциями, как правило, сенсибилизированы к поверхностным антигенам тромбоцитов и гранулоцитов. Переливание отмытых эритроцитов (или использование специальных лейкоцитарных фильтров) позволяет избежать этого осложнения.
В. Альбумин поступает в продажу в виде 5% и 25% раствора в 0,9% NaCl. Кроме того, выпускается белковая фракция плазмы (Плазманат), содержащая 88% альбумина и 12% глобулина. Для инактивации вирусов все препараты альбумина пастеризуют при 60°C в течение 10 ч. Сообщалось о нескольких случаях артериальной гипотонии при переливании белковой фракции плазмы, по-видимому, из-за присутствия в ней активатора прекалликреина. Частота этого осложнения при использовании современных препаратов альбумина сравнительно невелика. Принято считать, что препараты альбумина содержат мало солей, тем не менее концентрация натрия в них достигает 145 мэкв/л. Вопрос о преимуществах альбумина перед солевыми растворами остается спорным. Большинство клиник и травматологических центров предпочитает солевые растворы как более дешевые.
Г. Тромбоцитарная масса. Если в крови больного содержится более 75 000 мкл–1 полноценных тромбоцитов, то свертывание, как правило, не нарушено. Инвазивные исследования у больных с содержанием тромбоцитов менее 50 000 мкл–1 могут сопровождаться кровотечением. При снижении количества тромбоцитов до 30 000 мкл–1 и ниже возникают спонтанные кровотечения. При врожденных и приобретенных тромбоцитопатиях (например, при лечении аспирином) кровотечения возникают даже при нормальном содержании тромбоцитов. Одна доза тромбоцитарной массы содержит 50—100 млрд клеток в 50—70 мл плазмы. При тромбаферезе от донора получают 300—500 млрд тромбоцитов в 200—400 мл плазмы, что соответствует 6 дозам. Переливание одной дозы тромбоцитарной массы повышает содержание тромбоцитов в крови на 5000—10 000 мкл–1. Основное препятствие для использования тромбоцитарной массы — наличие в крови реципиента антитромбоцитарных антител, разрушающих донорские тромбоциты.
Д. Свежезамороженная плазма содержит все факторы свертывания, стабильные и нестабильные. В свежезамороженной плазме нет тромбоцитов, а содержание фибриногена относительно невелико. Показания к применению:
1. Дефицит антитромбина III.
2. Болезни печени, сопровождающиеся нарушениями синтеза факторов свертывания и кровоточивостью.
3. Передозировка непрямых антикоагулянтов.
4. Обменное или массивное переливание крови при коагулопатии или продолжающемся кровотечении (в дополнение к эритроцитарной массе).
6. Кровотечение или предстоящее инвазивное исследование у больных с выраженным дефицитом факторов свертывания II, V, VII, IX, X, XI или XIII.
Свежезамороженную плазму не используют для восстановления ОЦК, парентерального питания и в профилактических целях после массивных переливаний крови и операций с применением АИК.
Е. Криопреципитат. При оттаивании свежезамороженной плазмы на холоде образуется белый студенистый осадок, богатый факторами свертывания VIII, XIII, фибриногеном, фибронектином. Криопреципитат лиофилизируют и подвергают тепловой обработке для инактивации вирусов. Применяют при дефиците фактора свертывания VIII (гемофилия A); болезни фон Виллебранда (при неэффективности лечения десмопрессином ); дисфибриногенемиях, уремической тромбоцитопатии (при неэффективности лечения десмопрессином); дефиците фактора свертывания XIII; ДВС-синдроме.
Ж. Фибриноген. Применение человеческого фибриногена в настоящее время прекращено из-за чрезвычайно высокого риска заражения вирусным гепатитом. Для восполнения дефицита фибриногена используют криопреципитат.
З. Концентраты факторов свертывания. До 60-х годов для лечения дефицита факторов свертывания VIII и IX использовали только свежезамороженную плазму. С 1965 г. стали применять криопреципитат. В начале 70-х годов началось производство концентратов факторов свертывания. Больные гемофилией получили возможность самостоятельно использовать эти концентраты в домашних условиях, что значительно облегчило их жизнь. К сожалению, одновременно увеличился риск заражения вирусным гепатитом (до 90%); даже тепловая обработка сухих концентратов при 60°C в течение 72 ч не устраняла полностью угрозу инфекционных осложнений. У значительной части реципиентов обнаружили антитела к ВИЧ. Новые методы обработки концентратов позволили решить эту проблему. С 1 января 1990 г. не было зарегистрировано ни одного случая заражения ВИЧ при использовании концентратов факторов свертывания. В настоящее время разрабатываются методы получения рекомбинантных факторов свертывания.
И. Кровь «универсального» донора
Клетки крови группы 0(I) не имеют поверхностных антигенов A и B, поэтому доноров с этой группой крови называют «универсальными». Доказано, что переливание крови группы 0(I) относительно безопасно и оправдано в экстренных ситуациях, когда кровь требуемой группы или кровь, проверенная на индивидуальную совместимость, недоступна. Проведены сотни переливаний крови группы 0(I) (в основном при травмах), гемолитических трансфузионных реакций не отмечено. Риск сенсибилизации реципиента составляет 6%.
К. Другие препараты
1. Десмопрессин (1-дезамино-8-D-аргининвазопрессин) — синтетический аналог АДГ, нашедший широкое применение в терапии коагулопатий. Он вызывает дозозависимое ускорение всех реакций, катализируемых фактором свертывания VIII. Десмопрессин — препарат выбора в лечении легких форм гемофилии A и нарушений гемостаза при уремии. Дозу 0,3 мкг/кг вводят в течение 15—30 мин.
2. Препараты эритропоэтина (эпоэтин альфа, эпоэтин бета) производят биотехнологическими методами. Они стимулируют эритропоэз, но терапевтический эффект наступает не сразу, поэтому для лечения острых анемий их не применяют. Назначают в дозе 50—100 ед/кг 3 раза в неделю.
3. Апротинин — ингибитор протеаз (трипсина, плазмина, калликреина), в низких концентрациях угнетает фибринолиз. Полагают, что апротинин можно использовать для профилактики кровотечений после операций с применением АИК. Ведутся клинические испытания.
III. Экспериментальные кровезаменители. Поскольку переливание крови и ее компонентов не является абсолютно безопасным, ведутся поиски «идеальных» кровезаменителей, способных переносить кислород. Все эти препараты находятся на стадии доклинических или клинических испытаний.
А. Фторуглероды. Флюосол (20% эмульсия) — фторированный углеводород; кислород растворяется в нем в 10—20 раз лучше, чем в воде. Подобными свойствами обладают все фторуглероды. Однако сами они в воде нерастворимы и используются в виде эмульсии, что снижает их сродство к кислороду. В отличие от S-образной кривой диссоциации оксигемоглобина, кривая диссоциации оксифторуглеродов линейна. T1/2 флюосола при введении максимальной дозы (40 мл/кг) составляет всего 24 ч. При легкой или умеренной анемии его применение нецелесообразно, при тяжелой — неэффективно. Ведутся дальнейшие исследования.
Б. Очищенный гемоглобин получают из гемолизата эритроцитов путем очистки от стромальных белков. Препарат содержит 7 г% гемоглобина и обладает сродством к кислороду, в два раза большим, чем нативный гемоглобин. О сродстве гемоглобина к кислороду судят по величине P50 (paO2, при котором 50% гемоглобина насыщено кислородом). Для очищенног гемоглобина P50 составляет 12—14 мм рт. ст. Кроме того, поскольку препарат не содержит эритроцитов, он не увеличивает вязкости крови и позволяет снизить сердечный выброс, среднее АД и потребление кислорода. Препарат проходит испытания.
В. Пиридоксилированный полимер гемоглобина. Коллоидно-онкотические свойства препарата, концентрация гемоглобина (14 г%) и P50 — такие же, как у крови. T1/2 препарата в организме составляет 40—48 ч, он лишен недостатков очищенного гемоглобина. Препарат активно изучается.
IV. Варианты трансфузионной терапии
А. Отказ от переливания крови. По мере углубления наших знаний физиологии понятие «сигнал к началу переливания крови» утратило свое значение. Уровень гемоглобина ниже 100 г/л уже давно не считается достаточным показанием к переливанию крови. Здоровый человек без особых последствий переносит потерю 20% крови, если ее возместить солевыми растворами. Показания к переливанию крови и ее компонентов должны определяться самым тщательным образом.
Б. Аутогемотрансфузия (рис) — переливание больному его собственной крови, полученной заблаговременно. Каждые 72 ч берут 1 дозу крови, последнюю — не позже чем за 72 ч до операции; при этом гематокрит не должен быть менее 33%. Заготовку крови можно начинать за 6 нед до операции (максимальный срок хранения консервированной крови). Больному назначают препараты железа. Если необходимо сократить интервалы между взятием крови, назначают препараты эритропоэтина.
С. Реинфузия крови (рис). Показания: большая (1 л и более): 1) операционная, послеоперационная, 2) посттравматическая кровопотеря (травма селезенки, печени, почек), 3) внематочная беременность, 4) кровотечения во внутренние полости организма.
Противопоказания: 1) гнойное загрязнение излившейся крови; 2) загрязнение излившейся крови толстокишечным содержимым; 3) операция по поводу злокачественных опухолей; 4) почечная недостаточность.
Реинфузия крови из закрытых серозных полостей (плевральная полость, полость перикарда, брюшинная полость) в связи с возможным гемолизом и инфицированием ( при длительном пребывании – свыше суток) возможно только после проведения пробы на гемолиз (проба И.С. Колесникова): разведение в пробирке 1 мл крови в 20 мл изотонического раствора натрия хлорида. После центрифугирования или отстаивания содержимого пробирки производится визуальная оценка пробы. Появление желто-розового окрашивания надосадочной жидкости указывает на выраженный гемолиз и непригодность крови для реинфузии.

Рисунок 39 Методика сбора крови с операционного поля
Отсасывание крови из операционной раны осуществляют за счет регулируемого в границах 60-150 мм рт ст разряжения, создаваемого в флаконе с гемоконсервантом (глюгицир – 1 мл на 4 мл крови, либо гепарин 500 ЕД на 1000 мл собираемой крови) вакуум-отсосом. Дозировка поступления жидкости в наконечник отсоса (реополиглюкин, физраствор)

Рисунок 40 Периливание крови при ее реинфузии
При работе представленной системы последовательно происходит: 1) открытое предварительное фильтрование реинфузируемой крови через 4 слоя марли;
2) накопление крови во флаконе после промежуточной фильтрации;
3) переливание крови в вену больного с одновременной микрофильтрацией через фильтр капельницы.