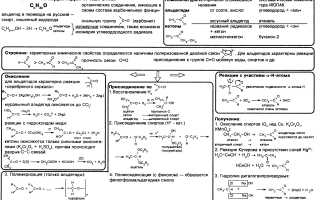
Анализ альдегидов, кетонов и кислот. Гексаметилентетрамин
Альдегиды и кетоны — номенклатура, получение, химические свойства

Строение альдегидов и кетонов
 Альдегиды – органические вещества, молекулы которых содержат карбонильную группу С=O , соединенную с атомом водорода и углеводородным радикалом.
Альдегиды – органические вещества, молекулы которых содержат карбонильную группу С=O , соединенную с атомом водорода и углеводородным радикалом.
Общая формула альдегидов имеет вид:

В простейшем альдегиде – формальдегиде роль углеводородного радикала играет другой атом водорода:

Карбонильную группу, связанную с атомом водорода, часто называют альдегидной:

Кетоны – органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами. Очевидно, общая формула кетонов имеет вид:

Карбонильную группу кетонов называют кетогруппой.
В простейшем кетоне – ацетоне – карбонильная группа связана с двумя метильными радикалами:

Номенклатура и изомерия альдегидов и кетонов
В зависимости от строения углеводородного радикала, связного с альдегидной группой, различают предельные, непредельные, ароматические, гетероциклические и другие альдегиды:

В соответствии с номенклатурой ИЮПАК названия предельных альдегидов образуются от названия алкана с тем же числом атомов углерода в молекуле с помощью суффикса -аль. Например:

Нумерацию атомов углерода главной цепи начинают с атома углерода альдегидной группы. Поэтому альдегидная группа всегда располагается при первом атоме углерода, и указывать ее положение нет необходимости.
Наряду с систематической номенклатурой используют и тривиальные названия широко применяемых альдегидов. Эти названия, как правило, образованы от названий карбоновых кислот, соответствующих альдегидам.
Для названия кетонов по систематической номенклатуре кетогруппу обозначают суффиксом -он и цифрой, которая указывает номер атома углерода карбонильной группы (нумерацию следует начинать от ближайшего к кетогруппе конца цепи). Например:

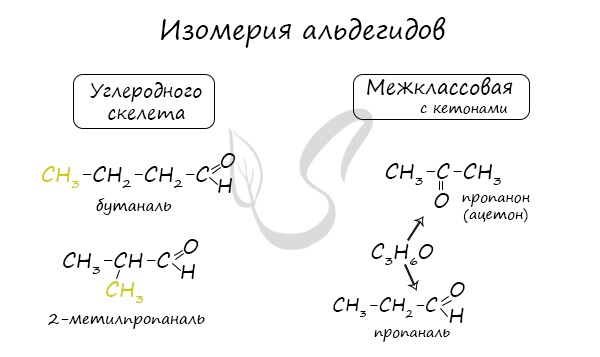
Для альдегидов характерен только один вид структурной изомерии — изомерия углеродного скелета, которая возможна с бутаналя, а для кетонов также и изомерия положения карбонильной группы. Кроме этого, для них характерна и межклассовая изомерия (пропаналь и пропанон).

Физические свойства альдегидов
В молекуле альдегида или кетона вследствие большей электороотрицательности атома кислорода по сравнению с углеродным атомом связь С=O сильно поляризована за счет смещения электронной плотности π-связи к кислороду:

Альдегиды и кетоны — полярные вещества с избыточной электронной плотностью на атоме кислорода. Низшие члены ряда альдегидов и кетонов (формальдегид, уксусный альдегид, ацетон) растворимы в воде неограниченно. Их температуры кипения ниже, чем у соответствующих спиртов. Это связано с тем, что в молекулах альдегидов и кетонов в отличие от спиртов нет подвижных атомов водорода и они не образуют ассоциатов за счет водородных связей. Низшие альдегиды имеют резкий запах; у альдегидов, содержащих от четырех до шести атомов углерода в цепи, неприятный запах; высшие альдегиды и кетоны обладают цветочными запахами и применяются в парфюмерии.

Химические свойства альдегидов и кетонов
Наличие альдегидной группы в молекуле определяет характерные свойства альдегидов.
1. Реакции восстановления.
Присоединение водорода к молекулам альдегидов происходит по двойной связи в карбонильной группе. Продуктом гидрирования альдегидов являются первичные спирты, кетонов — вторичные спирты. Так, при гидрировании уксусного альдегида на никелевом катализаторе образуется этиловый спирт, при гидрировании ацетона — пропанол-2.

Гидрирование альдегидов — реакция восстановления, при которой понижается степень окисления атома углерода, входящего в карбонильную группу.
2. Реакции окисления. Альдегиды способны не только восстанавливаться, но и окисляться. При окислении альдегиды образуют карбоновые кислоты.
Окисление кислородом воздуха. Например, из пропионового альдегида (пропаналя) образуется пропионовая кислота:

Окисление слабыми окислителями (аммиачный раствор оксида серебра).

Если поверхность сосуда, в котором проводится реакция, была предварительно обезжирена, то образующееся в ходе реакции серебро покрывает ее тонкой ровной пленкой. Получается замечательное серебряное зеркало. Поэтому эту реакцию называют реакцией «серебряного зеркала». Ее широко используют для изготовления зеркал, серебрения украшений и елочных игрушек.
3. Реакция полимеризации:
Получение альдегидов и кетонов

Применение альдегидов и кетонов
Формальдегид (метаналь, муравьиный альдегид) H2C=O:
а) для получение фенолформальдегидных смол;
б) получение мочевино-формальдегидных (карбамидных) смол;
в) полиоксиметиленовые полимеры;
г) синтез лекарственных средств (уротропин);
д) дезинфицирующее средство;
е) консервант биологических препаратов (благодаря способности свертывать белок).
Уксусный альдегид (этаналь, ацетальдегид) СН3СН=О:
а) производство уксусной кислоты;
б) органический синтез.
Ацетон СН3-СО-СН3:
а) растворитель лаков, красок, ацетатов целлюлозы;
б) сырье для синтеза различных органических веществ.
Альдегиды
Альдегиды – летучие жидкости органического состава, являющиеся продуктом неполного окисления спиртов. Карбонильная группа в молекулах альдегидов связана с одним атомом водорода и одной группой R.
Не часто встречаются в природе в отдельном виде, но, несомненно, играют важную роль в физиологических процессах растений и животных. Общая формула альдегидов CnH2nO.
Многие альдегиды имеют специфический запах. Высшие альдегиды, в особенности непредельные, используются в пищевой промышленности и парфюмерии.
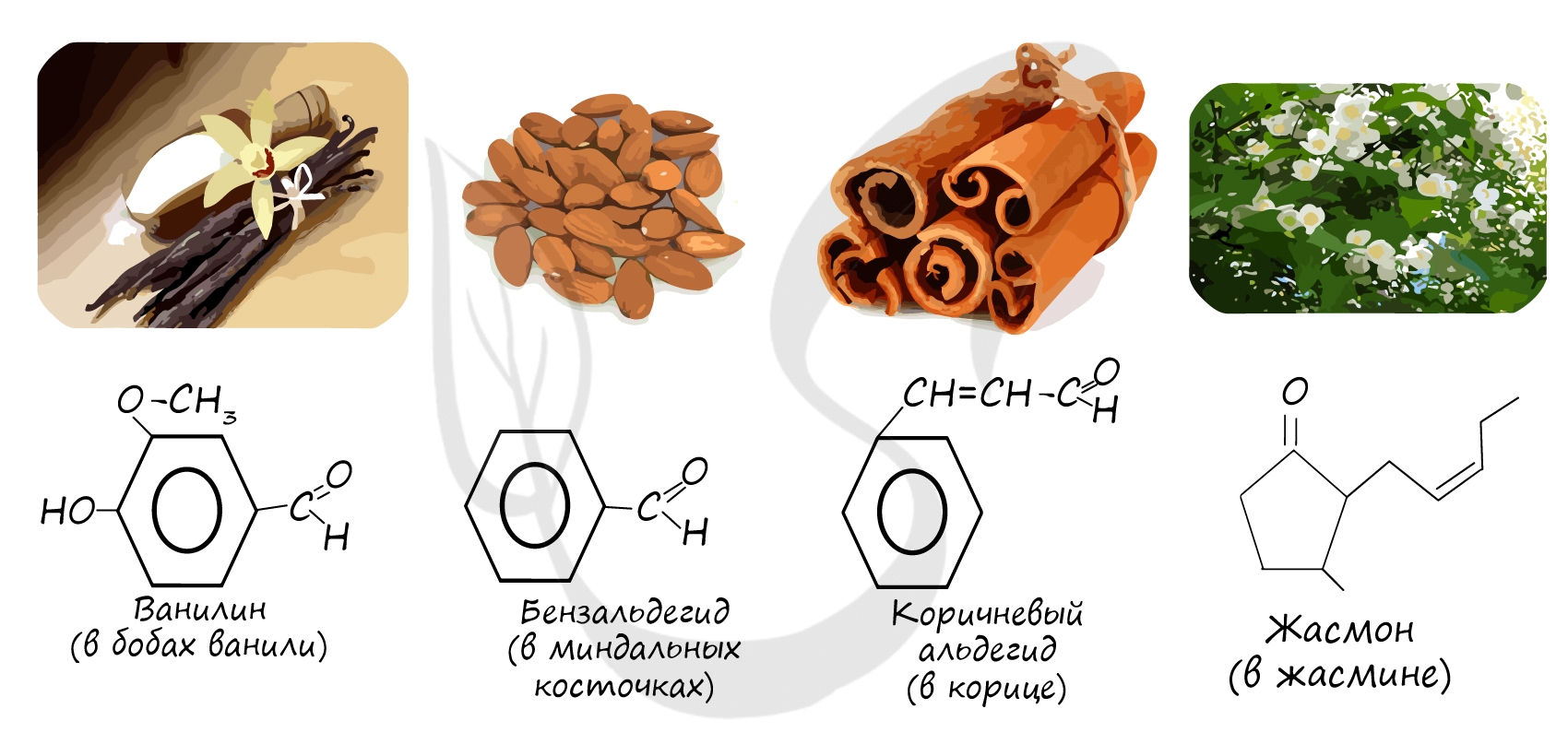
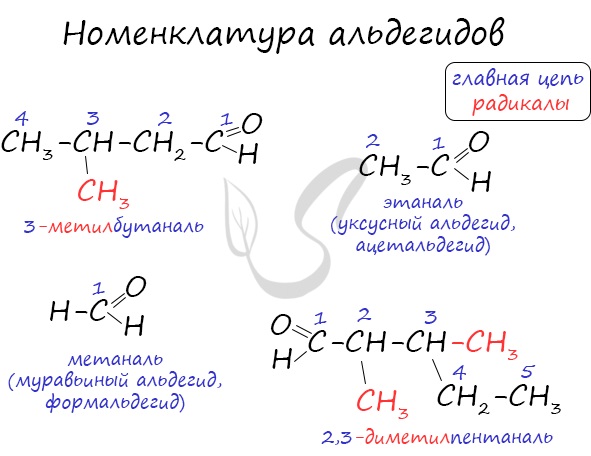
Номенклатура и изомерия альдегидов
Названия альдегидов формируются путем добавления суффикса “аль” к названию алкана с соответствующим числом атомов углерода: метаналь, этаналь, пропаналь, бутаналь, пентаналь и т.д.
Вы можете встретить их молекулярные формулы, где группа OH записана наоборот – HO. Например: метаналь – HCHO, этаналь – CH3CHO, пропаналь – C2H5CHO. Это делают специально для того, чтобы их было легче отличить от спиртов.
Многие альдегиды имеют тривиальные названия. Наиболее известные: метаналь – формальдегид, этаналь – ацетальдегид. Замечу, что формалином называется 40% раствор формальдегида.
Для альдегидов характерна структурная изомерия: углеродного скелета, межклассовая изомерия с кетонами.
Получение альдегидов и кетонов
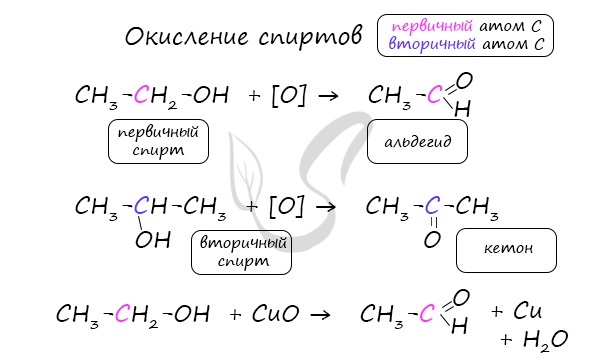
- Окисление спиртов
Важно заметить, что при окислении первичных спиртов образуются альдегиды, при окислении вторичных спиртов – кетоны. Окисление с помощью оксида меди относится к лабораторным способам получения альдегидов.
Этот способ также просто осуществить в лабораторных условиях. При пиролизе (нагревании без доступа кислорода) кальциевых или бариевых солей карбоновых кислот возможно получение кетонов.

В присутствии катализатора и при нагревании спиртов от гидроксогруппы и прилежащего к ней атома углерода отщепляется по атому водорода. В результате образуется карбонильная группа.
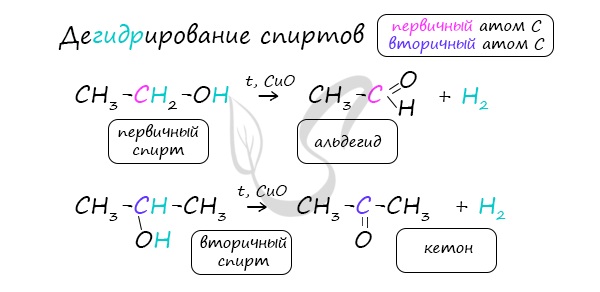
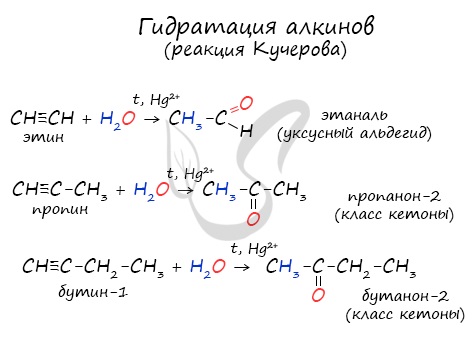
Реакцией Кучерова называют гидратацию алкинов в присутствии солей двухвалентной ртути.
В результате такой реакции ацетилен превращается в уксусный альдегид. Все остальные его гомологи: пропин, бутин, пентин и т.д. превращаются в соответствующие кетоны.
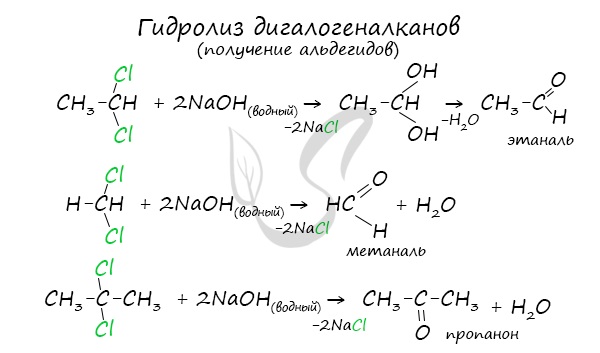
Для получения альдегида два атома галогена должны находиться у первичного атома углерода, для получения кетонов – у вторичного.
В результате такого гидролиза образуются двухатомные спирты, в которых две OH-группы прилежат к одному атому углерода. Такие соединения неустойчивы и распадаются на карбонильное соединение (альдегид или кетон) и воду.
В промышленности окислением метана при температуре 500 °C и в присутствии катализатора получают формальдегид.

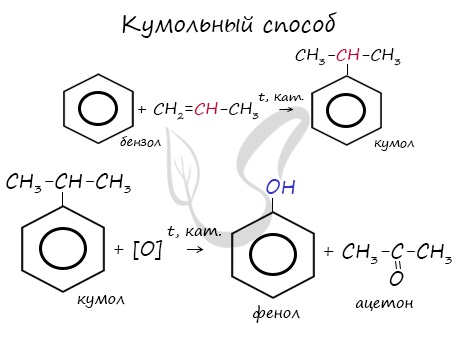
В прошлой теме, посвященной фенолам, мы касались данного способа. В результате такой реакции образуется не только фенол, но и ацетон.
Химические свойства альдегидов и кетонов
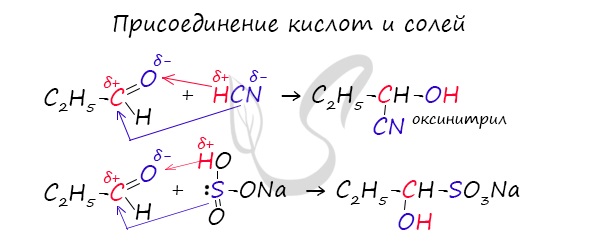
Запомните, что для альдегидов и кетонов характерны реакции присоединения по карбонильной группе. Этот факт особенно поможет сравнить альдегиды и карбоновые кислоты, для которых реакции присоединения не характерны.
Для понимания механизма реакции важно вспомнить об электроотрицательности. В карбонильной группе кислорд, как более электроотрицательный элемент, тянет электронную плотность на себя от углерода. На атоме кислорода возникает частичный отрицательный заряд (δ-), а на атоме углерода частичный положительный (δ+).
Основы школьного курса физики подсказывают, что отрицательный заряд притягивает положительный: именно так и будет происходить при присоединении различных молекул к карбонильной группе альдегидов и кетонов.
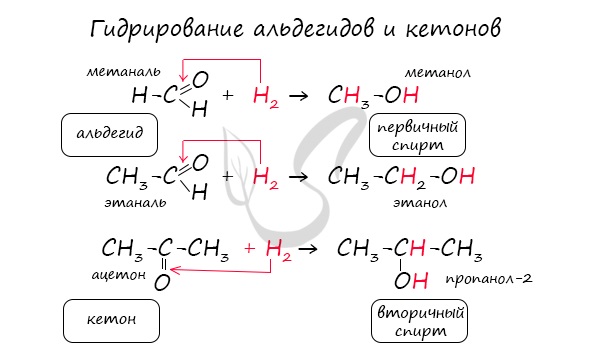
Реакция гидрирования альдегидов происходит по типу присоединения, сопровождается разрывом двойной связи в карбонильной группе. Гидрирование альдегидов приводит к образованию первичных, а гидрирование кетонов – вторичных спиртов.
В результате полного окисления, горения, образуется углекислый газ и вода.
Альдегиды легко окисляются до карбоновых кислот в лабораторных условиях. Это осуществляется с помощью известной реакции серебряного зеркала. Данная реакция является качественной для альдегидов.
Кетоны, в отличие от альдегидов, в реакции окисления не вступают.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли

Важно заметить, что при окислении метаналя, образовавшаяся муравьиная кислота тут же окисляется до угольной кислоты, которая распадается на углекислый газ и воду. Это связано с интересным фактом – наличием альдегидной группы у муравьиной кислоты.

Окисление также возможно другим реагентом – гидроксидом меди II. Эта реакция также относится к качественным для альдегидов, в результате образуется кирпично-красный осадок оксида меди I.

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Альдегиды
Альдегиды – летучие жидкости органического состава, являющиеся продуктом неполного окисления спиртов. Карбонильная группа в молекулах альдегидов связана с одним атомом водорода и одной группой R.
Не часто встречаются в природе в отдельном виде, но, несомненно, играют важную роль в физиологических процессах растений и животных. Общая формула альдегидов CnH2nO.

Многие альдегиды имеют специфический запах. Высшие альдегиды, в особенности непредельные, используются в пищевой промышленности и парфюмерии.

Номенклатура и изомерия альдегидов
Названия альдегидов формируются путем добавления суффикса “аль” к названию алкана с соответствующим числом атомов углерода: метаналь, этаналь, пропаналь, бутаналь, пентаналь и т.д.
Вы можете встретить их молекулярные формулы, где группа OH записана наоборот – HO. Например: метаналь – HCHO, этаналь – CH3CHO, пропаналь – C2H5CHO. Это делают специально для того, чтобы их было легче отличить от спиртов.
Многие альдегиды имеют тривиальные названия. Наиболее известные: метаналь – формальдегид, этаналь – ацетальдегид. Замечу, что формалином называется 40% раствор формальдегида.

Для альдегидов характерна структурная изомерия: углеродного скелета, межклассовая изомерия с кетонами.

Получение альдегидов и кетонов
- Окисление спиртов
Важно заметить, что при окислении первичных спиртов образуются альдегиды, при окислении вторичных спиртов – кетоны. Окисление с помощью оксида меди относится к лабораторным способам получения альдегидов.

Этот способ также просто осуществить в лабораторных условиях. При пиролизе (нагревании без доступа кислорода) кальциевых или бариевых солей карбоновых кислот возможно получение кетонов.

В присутствии катализатора и при нагревании спиртов от гидроксогруппы и прилежащего к ней атома углерода отщепляется по атому водорода. В результате образуется карбонильная группа.

Реакцией Кучерова называют гидратацию алкинов в присутствии солей двухвалентной ртути.
В результате такой реакции ацетилен превращается в уксусный альдегид. Все остальные его гомологи: пропин, бутин, пентин и т.д. превращаются в соответствующие кетоны.

Для получения альдегида два атома галогена должны находиться у первичного атома углерода, для получения кетонов – у вторичного.
В результате такого гидролиза образуются двухатомные спирты, в которых две OH-группы прилежат к одному атому углерода. Такие соединения неустойчивы и распадаются на карбонильное соединение (альдегид или кетон) и воду.

В промышленности окислением метана при температуре 500 °C и в присутствии катализатора получают формальдегид.

В прошлой теме, посвященной фенолам, мы касались данного способа. В результате такой реакции образуется не только фенол, но и ацетон.

Химические свойства альдегидов и кетонов
Запомните, что для альдегидов и кетонов характерны реакции присоединения по карбонильной группе. Этот факт особенно поможет сравнить альдегиды и карбоновые кислоты, для которых реакции присоединения не характерны.
Для понимания механизма реакции важно вспомнить об электроотрицательности. В карбонильной группе кислорд, как более электроотрицательный элемент, тянет электронную плотность на себя от углерода. На атоме кислорода возникает частичный отрицательный заряд (δ-), а на атоме углерода частичный положительный (δ+).
Основы школьного курса физики подсказывают, что отрицательный заряд притягивает положительный: именно так и будет происходить при присоединении различных молекул к карбонильной группе альдегидов и кетонов.

Реакция гидрирования альдегидов происходит по типу присоединения, сопровождается разрывом двойной связи в карбонильной группе. Гидрирование альдегидов приводит к образованию первичных, а гидрирование кетонов – вторичных спиртов.

В результате полного окисления, горения, образуется углекислый газ и вода.
Альдегиды легко окисляются до карбоновых кислот в лабораторных условиях. Это осуществляется с помощью известной реакции серебряного зеркала. Данная реакция является качественной для альдегидов.
Кетоны, в отличие от альдегидов, в реакции окисления не вступают.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли

Важно заметить, что при окислении метаналя, образовавшаяся муравьиная кислота тут же окисляется до угольной кислоты, которая распадается на углекислый газ и воду. Это связано с интересным фактом – наличием альдегидной группы у муравьиной кислоты.

Окисление также возможно другим реагентом – гидроксидом меди II. Эта реакция также относится к качественным для альдегидов, в результате образуется кирпично-красный осадок оксида меди I.

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Анализ альдегидов, кетонов и кислот. Гексаметилентетрамин
Т омский государственный университет
кафедра органической химии
Альдегиды и кетоны
Альдегиды и кетоны отличаются наличием карбонильной группы >С =О.
Карбонильная группа поляризована по связи С-О :
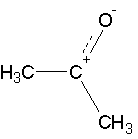
Альдегиды и кетоны можно рассматривать, как производные алканов , у которых одна из метильных (-СН3) или метиленовых групп (-СН 2 –) заменена на карбонильную группу:
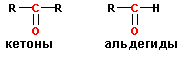
Кетоны имеют в качестве заместителей при карбонильной группе два алкильных радикала, тогда как в альдегидах один заместител ь- алкильная группа, другой- водород. Такое различие приводит к существенным различиям в химических свойствах ( см . ниже).
При наименовании альдегидов и кетонов по правилам номенклатуры ИЮПАК выбирается самая длинная цепь углеродов, включающая в себе карбонильную группу. Нумерация атомов углерода в этой цепи производится с того края, куда ближе карбонильная группа, а при формировании названия к названию углеводорода, соответствующему числу атомов углерода в основной цепи (1-метан, 2- этан, 3-пропан, 4-бутан, 5 –пентан и т.д.) прибавляется окончание -а ль (для альдегидов) или -он для кетонов.
Положение карбонильной группы у кетонов указывается через тире, если возможно существование нескольких изомеров. Положение карбонильной группы альдегидов не указывается цифрой, поскольку во всех случаях она оказывается под первым номером:
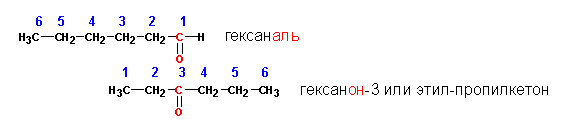
Кетоны часто называют по радикалам, соединенным через карбонильную группу, с добавлением слова кетон. Например, гексанон-3 или метилэтилкетон , ацетон или диметилкетон .
Альдегиды могут быть названы, как производные этаналя или уксусного альдегида:

Другое названи е– триметилэтаналь .
Химические свойства карбонильных соединений
Все реакции карбонильных соединений можно разделить на группы:
– реакции по карбонильной группе (присоединение)
– реакции по углеродному скелету
Реакции присоединения по карбонильной группе (присоединение нуклеофильных реагентов)
1. присоединение воды
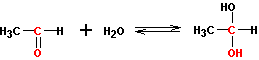
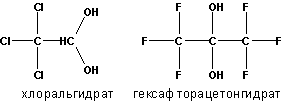
Образующиеся гем-диолы неустойчивы и равновесие в этой реакции сильно смещено влево. Исключение составляют альдегиды и кетоны с электроноакцепторными группами, например, хлораль или гексафторацетон , которые в водной среде существуют в виде гем-диолов :
2. присоединение бисульфита
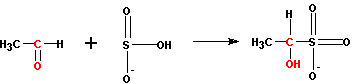
Присоединение идет через более нуклеофильный атом серы, а не кислорода, хотя на нем и имеется отрицательный заряд. Образуются производные алкансульфокислот (соли алканоксисульфокислот ).
Образующиеся аддукты нерастворимы в насыщенном растворе бисульфита натрия или спиртах и выпадают в осадок в виде кристаллов. Так можно отделять карбонильные соединения из смеси со спиртами. Карбонильное соединение выделяется в свободном виде из аддукта при обработке его кислотой.
При реакции с кетонами бисульфиты присоединяются только к метилкетонам СН3-СО-R.
3. присоединение цианидов
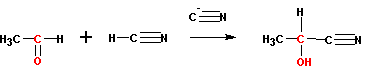
Реакция катализируется цианистым калием или натрием. Образующиеся оксинитрилы (или циангидрины ) могут быть гидролизованы до оксикарбоновых кислот:
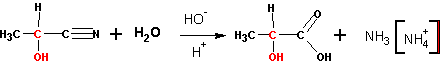
4. присоединение спиртов
При присоединении первой молекулы спирта образуются полуацетали . Реакция катализируется кислотами или основаниями:
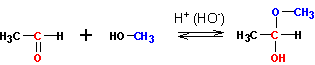
Присоединение второй молекулы спирта приводит к образованию ацеталей . Образование ацеталей катализируется только в кислой среде:
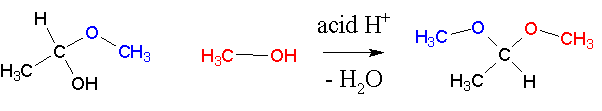
Ацетали устойчивы в нейтральной и щелочной среде, поэтому могут быть использованы для временной защиты альдегидных групп. Ацетали широко распространены в природе.
5. присоединение реактивов Гриньяра
Взаимодействие металлорганических соединений типа R-Mg-X (реактивы Гриньяра ), где Х= галоген, с карбонильными группами (нуклеофильное присоединение по кратной связи С =О):
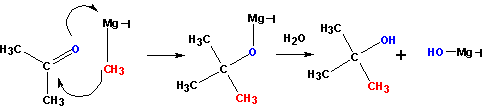
Взаимодействие с формальдегидом, альдегидами, кетонам и – приводит к первичным, вторичным и третичным спиртам, соответственно.
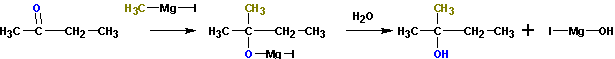
Из кетонов получаются третичные спирты. Так, из метилэтилкетона (бутанон-2) получается 2-метилбутанол-2. Альдегиды в подобной реакции дают вторичные спирты. Из пропионового альдегида ( пропаналь ) получается бутанол-2:
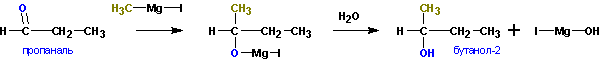
Из формальдегида образуются первичные спирты. При взаимодействии реактивов Гриньяра с галогенангидридами карбоновых кислот и сложными эфирами образуются третичные спирты, у которых имеется два одинаковых алкильных заместителя. При этом расходуется два моля реактива Гриньяра :
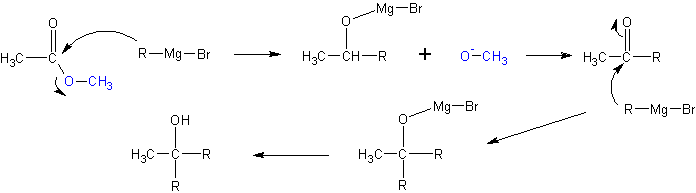
6. Присоединение аммиака и аминов
Первичные амины присоединяются к альдегидам и кетонам с образованием иминов (оснований Шиффа :
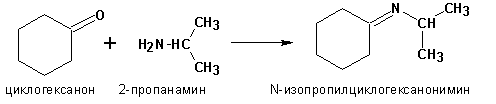
Аналогичная реакция вторичных аминов с карбонильными соединениями дает енамины :
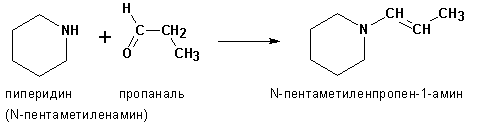
С карбонильными соединениями могут вступать во взаимодействие также гидразин и его производные с образованием гидразонов :
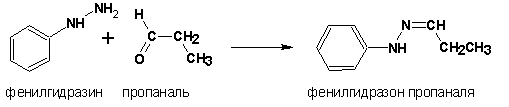
Гидроксиламины присоединяются к альдегидам и кетонам с образованием альдоксимов и кетоксимов :
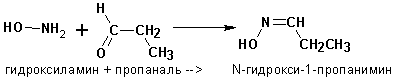
7. Альдольно-кротоновая конденсация
Конденсация может происходить как в кислой среде, так и в щелочной.
Катализируемая кислотой конденсация
В конденсацию вступают енол и протонированная карбонильная группа второй молекулы соединения:
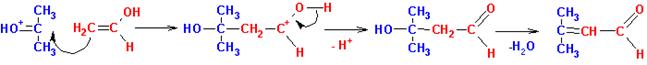
Конденсация, катализируемая основанием
Образование енолят-иона , генерирующего карбанион , протекает по схеме:
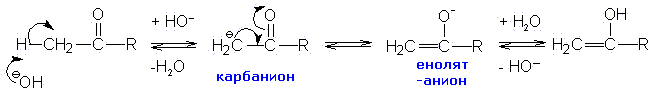
Далее карбанион присоединяется к карбонильной группе второй молекулы, причем протекает С-алкилирование , в отличие от термодинамически невыгодного О- алкилирования :
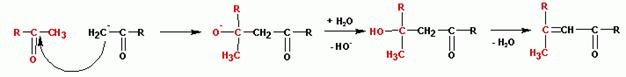
Образующийся альдегидоспирт ( альдоль ) легко теряет воду в присутствии каталитических количеств оснований или кислот, а также при незначительном нагревании, с образованием a , b – ненасыщенного карбонильного соединения, этим завершается реакция конденсации ( R ,Х= алкил или Н):
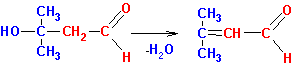
Таким образом, в реакцию альдольн о – кротоновой конденсации (в том числе и самоконденсации ) могут вступать как альдегиды, так и кетоны, имеющие альфа-углеродные атомы водорода. В случае кетонов положение равновесия невыгодно для образования продуктов, тем не менее, проводя реакцию в особых условиях (например, исключая контакт продукта с катализатором основного характера) можно добиваться существенных выходов. Перекрестные реакции между альдегидами и кетонами не имеют лабораторного применения, поскольку образуется трудноразделяемая смесь из четырех продуктов и непрореагировавших исходных соединений. Чаще в синтетических целях проводят реакцию между двумя карбонильными соединениями, одно из которых является источником карбанионов ( метиленовая компонента ), а другое служит карбонильной компонентой (не имеющей альфа-углеродных атомов водорода). Обычно в роли карбонильной компоненты используются формальдегид, ароматические альдегиды, эфиры угольной, щавелевой и муравьиной кислот. В качестве метиленовой компоненты применяют в том числе и С-Н кислоты и даже производные ацетиленовых углеводородов с концевой тройной связью.
8. Реакция Канниццаро
Альдегиды, не имеющие альфа-углеродных атомов водорода при нагревании с сильными основаниями вступают в реакцию окисления-восстановления, когда одна из молекул восстанавливается до спирта за счет окисления второй молекулы до карбоновой кислоты. Такие реакции носят название реакции Канниццаро , и протекают по схеме:
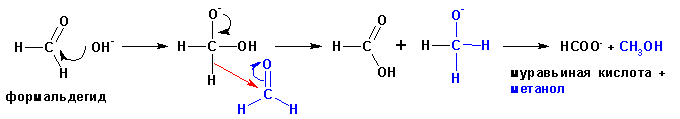
Известны и внутримолекулярные реакции окисления-восстановления:
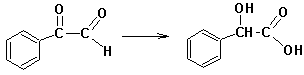
C воеобразной разновидностью внутримолекулярного окисления-восстановления является Бензиловая перегруппировка:
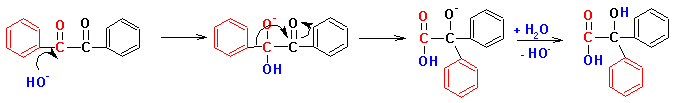
Реакции по углеродному скелету альдегидов и кетонов
Реакции, затрагивающие углеродный скелет, включают:
– кето-енольная таутомерия альдегидов и кетонов;
– галогенирование ( галоформная реакция и замещение a – углеродных атомов водорода)
1. Кето-енольная таутомерия
Карбонильные соединения могут сосуществовать в двух форма х- кетонной и енольной :
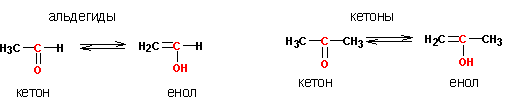
Превращения альдегидов и кетонов в енолы (непредельные спирты) протекает как самопроизвольно, так и с катализом кислотами и основаниями. Енольные формы хоть и присутствуют в альдегидах и кетонах в незначительных концентрациях, но роль в их реакционной способности играют существенную. Через образование енолов идет целый ряд важных реакций альдегидов и кетонов. Рассмотрим механизмы перехода кетонных форм в енольные , протекающие при каталитическом действии кислот и оснований.
Енолизация , катализируемая кислотой
Образование енола может катализироваться кислотой согласно нижеприведенной схеме ( R ‘= алкил или Н):
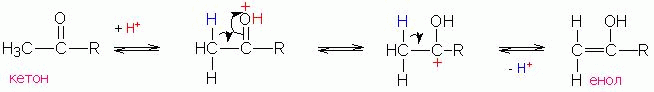
Реакция начинается с протонирования атома кислорода карбонильной группы и завершается отщеплением протона уже от альфа-углеродного атома. Таким образом, формально протон играет роль катализатора.
Енолизация , катализируемая основанием
Образование енолят-иона протекает по схеме:
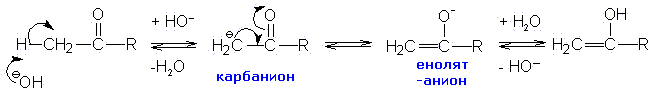
В образовании енолов при катализе основаниями важную роль играет кислотность альф а- углеродных атомов водорода. Их повышенная кислотность связана с близким соседством с карбонильной группой и ее отрицательным индуктивным эффектом, оттягивающим электроны связи С-Н и облегчающим таким образом отщепление протона. Другими словами, отщепление протона облегчено потому, что образующийся карбанион стабилизирован делокализацией отрицательного заряда на карбонильную группу.
К образовавшимся енолам присоединяются галогены по кратной связи С =С. Только в отличие от алкенов , где такое присоединение завершается полным связыванием галогена, у альдегидов и кетонов присоединяется только один атом галогена (на соседний с карбонильной группой углерод). Второй атом галогена (на карбонильную группу) не присоединяется, а реакция завершается отщеплением протона и регенерацией карбонильной группы:
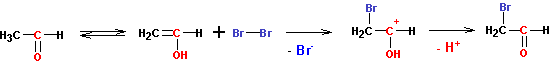
В кислой среде реакция на этом и останавливается. Замещения второго атома водорода на галоген не происходит. А вот в щелочной среде происходит быстрая реакция замещения второго, и еще более быстрая реакция замещения третьего атома углерода на галоген (увеличение числа атомов галогена при углероде резко усиливает кислотность его водородов):
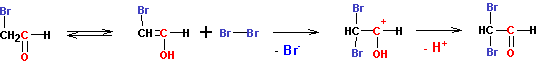
В конечном итоге все три атома водорода оказываются замещены на галогены, после чего следует отщепление группировки СХ3 в виде аниона, с последующим немедленным обменом протоном:
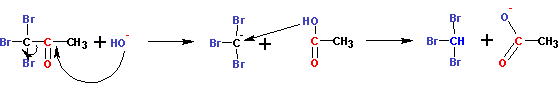
В результате образуется тригалогенметан , называемый галоформом ( иодоформ CHJ 3, бромоформ CHBr 3, хлороформ CHCl 3) и анион карбоновой кислоты. А сам процесс называется галоформной реакцией. Галоформной реакции подвержены любые метилкетоны . Галоформы выпадают в виде окрашенного осадка (желтый иодоформ ), имеют специфический запах и могут служить качественной реакцией на присутствие метилкетонов . Галоформную реакцию дают также спирты, при окислении которых могут образоваться метилкетоны (например, изопропанол ). Окисление осуществляется избыточным количеством галогена.
Окисление альдегидов и кетонов
Альдегиды легко окисляются до соответствующих кислот: