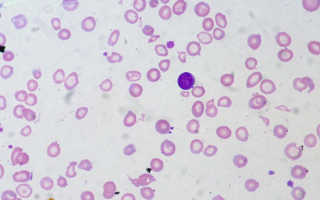
Апластическая приобретенная анемия. Анемии, патология гемостаза, онкогематология Что творится в костном мозге при аплазии
Проявление апластической анемии крови – аплазия костного мозга
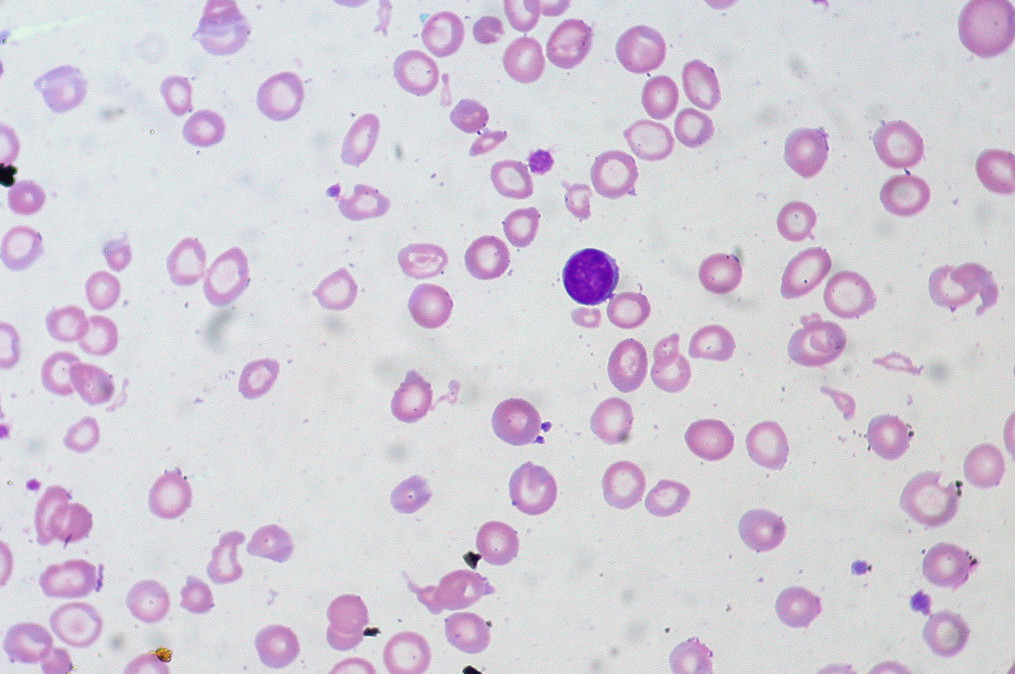
Апластическая анемия – это заболевание, которое включает в себя расстройства функции костного мозга и уменьшение количества элементов крови. Апластическая анемия может повлиять на людей всех возрастов, у некоторых она врожденная, у других – приобретенная.
Анемия иногда появляется внезапно или развивается постепенно, в течение длительного времени, даже в течение нескольких месяцев. Болезнь бывает кратковременная или хроническая. Апластическая анемия может иметь тяжелую форму и привести к смерти.
Причины аплазии костного мозга
На развитие апластической анемии влияние оказывают следующие факторы:
- лучевая терапия и химиотерапия;
- контакт с инсектицидами и гербицидами;
- аутоиммунные расстройства;
- условия труда;
- вирусные инфекции;
- прием некоторых лекарственных препаратов, например, некоторых антибиотиков и средств от ревматоидного артрита;
- гемолитическая анемия;
- заболевания соединительной ткани;
- ночная гемоглобинурия;
- беременность – иногда у женщин, ожидающих ребенка, иммунная система поражает костный мозг.
Симптомы апластической анемии
Симптомы апластической анемии зависят от того, какой компонент крови поврежден.
- слабость и одышка появляются при снижении уровня эритроцитов;
- повышенная восприимчивость к инфекциям и лихорадочное состояние имеет место при снижении уровня лейкоцитов в крови;
- склонность к кровотечению, а также образованию петехий присутствует при пониженном уровне тромбоцитов в крови.
Диагноз ставится при появлении двух из трех изменений в крови. Развитие аплазии костного мозга проходит по-разному, у некоторых пациентов болезнь протекает быстрее, у других медленнее. Иногда наступает период улучшения.
У людей с тяжелой формой заболевания смертность высокая, особенно перед началом лечения. К смерти приводит, как правило, сепсис или грибковая инфекция. Апластическая анемия может перерасти в рак.
Диагностика и лечение аплазии костного мозга
Для диагностики апластической анемии, как правило, требуется исследование крови, а также биопсия костного мозга. После установления диагноза анемии, как правило, проводят дальнейшие исследования, чтобы определить причину анемии.
Основными методами лечения апластической анемии являются: пересадка костного мозга и лечение андрогенами и иммуносупрессивными препаратами. Кроме того, лечение включает в себя переливание тромбоцитов и концентрата эритроцитов. Больным назначают также антибиотики и противогрибковые препараты.
Человек, страдающий от анемии, должен о себе заботиться. Рекомендуется избегать контакта с больными людьми и часто мыть руки в целях профилактики инфицирования.
Больные с анемией чувствуют усталость и трудности с дыханием, даже после минимальных усилий, поэтому они должны отдыхать, как только почувствуют такую необходимость. Следует также избегать занятий спортом, чтобы не допустить риска получения травм или падения.
Апластическая анемия
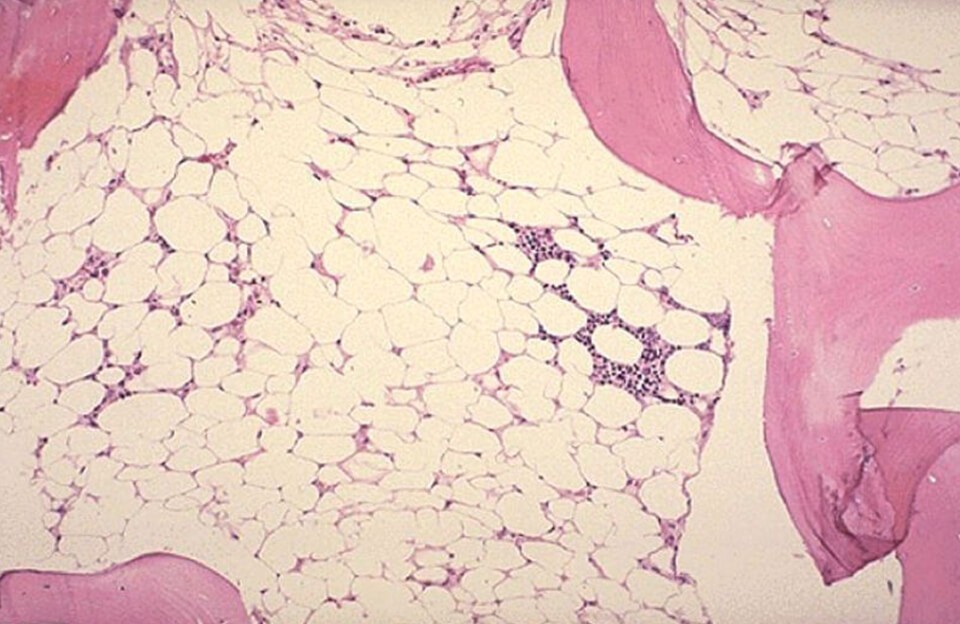
Апластическая анемия – тяжёлое гематологическое заболевание, сопровождающиеся малокровием, резким снижением иммунитета, а также нарушениями процессов свертывания крови. Она возникает вследствие подавления кроветворной функции костного мозг (или аплазии костного мозга).
Болезнь впервые описана известным немецким врачом и ученым Паулем Эрлихом, в 1888 году. Неизвестная ранее патология, обнаруженная у молодой беременной женщины, сопровождалась тяжёлой анемией, снижением числа лейкоцитов, лихорадкой, кровоточивостью и быстро привела к смерти больной. Проведенное патологоанатомическое исследование обнаружило замещение красного костного мозга жировой тканью. Позднее, в 1907 году, Анатоль Шоффар, французский врач, предложил назвать это заболевание апластической анемией.
Апластическая анемия – достаточно редкое заболевание. Средняя заболеваемость – 3-5 на 1 млн. всего населения за год. Большинство больных – дети и молодые люди.
Виды апластических анемий
Различают наследственную (генетически обусловленную) и приобретенную апластическую анемию.
80% случаев заболевания обусловлены приобретенной формой патологии, 20% вызваны генетическими факторами.
Медики пользуются классификацией патологии по МКБ-10 (Международная Классификация Болезней 10 пересмотра). Различают следующие виды апластических анемий:
D61.0 Конституциональная апластическая анемия
D61.1 Медикаментозная апластическая анемия
D61.2 Апластическая анемия, вызванная другими внешними агентами
D61.3 Идиопатическая апластическая анемия
D61.8 Другие уточненные апластические анемии
D61.9 Апластическая анемия неуточненная
Апластическая анемия у детей
У детей в большинстве случаев заболевание носит приобретенный характер. Частота встречаемости составляет 2-3 случая на 1 млн. детей (пик заболеваемости приходится на подростковый возраст). В 70% случаев непосредственную причину болезни установить не удаётся, принято считать, что наибольшее значение имеют вирусные инфекции, химикаты и лекарственные препараты.
Чаще всего диагноз устанавливают случайно, при общем анализе крови. При правильном лечении и своевременной диагностике прогноз благоприятный. Апластическая анемия у детей хорошо лечится. Результаты применения трансплантации костного мозга и иммуносупрессивной терапии примерно одинаковы по эффективности, однако следует отдавать предпочтение пересадке костного мозга от подходящего (в идеале брат или сестра) донора. Современные методы лечения апластической анемии в детском возрасте позволяют сохранить здоровье и не влияют на способность иметь детей в будущем.
Причины и факторы риска возникновения апластических анемий
Генетически обусловленные нарушения кроветворной функции отмечают при некоторых наследственных патологиях, таких как семейная анемия Фанкони, синдром Швахмана-Даймонда, истинная эритроцитарная аплазия, врождённый дискератоз.
Мутации в критически важных генах, отвечающих за регуляцию клеточного цикла, синтез белков, защиту и восстановление повреждений ДНК, ведут к образованию дефектных стволовых (гемопоэтических) клеток. Ошибки в генетическом коде инициируют запуск апоптоза – механизма запрограммированной клеточной смерти. При этом пул стволовых клеток сокращается гораздо быстрее, чем у здоровых людей.
Приобретенная форма патологии возникает в результате прямого токсического воздействия на гемопоэтические клетки. К таким факторам относят:
· Воздействие ионизирующей радиации. От апластической анемии погибла Мария Склодовская-Кюри – физик, дважды лауреат Нобелевской премии, полученной за работы в области исследования радиоактивности и за открытие новых радиоактивных элементов;
· Пестициды, инсектициды, производные бензола, соли тяжёлых металлов, мышьяк обладают прямым токсическим эффектом на костный мозг, угнетают продукцию форменных элементов крови и приводят к гибели стволовых клеток;
· Схожим эффектом обладают некоторые лекарства. Нестероидные противовоспалительные средства, противоопухолевые препараты, анальгин, левомицетин (вызывает наиболее тяжёлую форму заболевания, которая по статистике возникает в 1 из 30 тыс. курсов лечения левомицетином), мерказолил, карбамазепин, хинин способны вызвать апластическую анемию у некоторых людей;
· Пусковым фактором для болезни могут быть вирусы. Вирусные гепатиты, некоторые виды парвовирусов, ЦМВ, вирус Эпштейна-Барр и ВИЧ обладают способностью вызывать сбой в иммунной системе, вследствие чего она начинает атаковать собственные ткани организма. Например, у 2% пациентов с острым вирусным гепатитом – выявляют апластическую анемию;
· Аутоиммунные заболевания (ревматоидный артрит, СКВ) также может сопровождать аплазия костного мозга;
· Апластическая анемия при беременности, предположительно, также возникает из-за нарушений в иммунной системе.
В более 50% случаев непосредственную причину заболевания не находят, тогда говорят об идиопатической апластической анемии.
Что происходит при апластической анемии
Красный костный мозг – основной и самый важный кроветворный орган, в котором происходит образование и созревание элементов крови. Стволовые гемопоэтические клетки в нем дают начало эритроцитам (отвечают за перенос О 2 и СО 2 ), лейкоцитам (обеспечивают иммунитет) и тромбоцитам (участвуют в процессах свёртывания крови). Количество гемопоэтических клеток ограничено и постепенно уменьшается на протяжении всей жизни человека.
При апластической анемии происходит массовая гибель стволовых клеток костного мозга, и, как результат, – резкое снижение содержания эритроцитов, тромбоцитов и лейкоцитов в кровеносном русле больного. Недостаток эритроцитов приводит к малокровию, уменьшение количества лейкоцитов вызывает резкое угнетение иммунной системы, уменьшение числа тромбоцитов – причина кровоточивости и, как следствие, повышенного риска неконтролируемого кровотечения.
Результаты последних исследования дают основание полагать, что приобретенная форма заболевания почти всегда – аутоиммунная патология. Ключевой момент в развитии аплазии красного костного мозга – прямое цитотоксическое действие Т-лимфоцитов. Однако причина, по которой Т-лимфоциты начинают распознавать гемопоэтические стволовые клетки как цели для атаки, до сих пор неизвестна. Пусковым фактором могут служить точечные мутации в генах, кодирующих человеческие лейкоцитарные антигены (HLA система), и объясняющий искажённый иммунный ответ (как и при других аутоиммунных патологиях).
Также полагают, что для развития патологии необходима комбинация нескольких факторов – как внутренних (неизвестные дефекты в ДНК стволовых клеток, мутации генов системы HLA, иммунные нарушения), так и внешних (лекарственные препараты, вирусные инфекции, экзотоксины и антигены).
Как заподозрить апластическую анемию – симптомы и признаки болезни
Симптомы, характерные для заболевания:
· Необъяснимая слабость, утомляемость, сонливость;
· Одышка, возникающая даже при легком физическом напряжении;
· Головокружение, головные боли;
· Перебои в сердце, сердцебиение, тахикардия;
· Удлинение времени свертывания крови, кровоизлияния в мягкие ткани, головной мозг, образование синяков и кровоподтёков при незначительном воздействии, кровотечение из носа, затяжные изнуряющие менструации у женщин;
· Мелкоточечные кровоизлияния в кожу и слизистые оболочки, кровоточивость десен;
· Частые инфекции (дыхательных путей, кожи, слизистых оболочек, мочевыводящих путей), сопровождающиеся лихорадкой;
· Безболезненные язвы на слизистой рта;
· Потеря массы тела, похудание.
Течение болезни может быть постепенным или молниеносным (с быстрым развитием крайне тяжелой анемии, иммунодефицита, нарушениям процессов свертывания крови с соответствующими осложнениями).
Диагностика апластической анемии
Для диагностики используют развернутый анализ крови и гистологическое исследование материала, добытого из костного мозга.
Лабораторные признаки патологии, обнаруживаемые в периферической крови:
· Снижение концентрации эритроцитов и гемоглобина в крови без дефицита железа;
· Снижение концентрации лейкоцитов всех видов в крови больного;
· Низкое количество ретикулоцитов – незрелых форм эритроцитов;
· Увеличение скорости оседания эритроцитов (до 40-60 мм/ч).
В очень тяжелых случаях концентрация гемоглобина падает ниже 20-30 гр/л. Цветовой показатель, уровни сывороточного железа, эритропоэтина обычно в норме или повышены. Количество тромбоцитов ниже нормы, в тяжёлых случаях они полностью отсутствуют.
Диагноз подтверждается с помощью биопсии костного мозга. Гистология пунктата показывает большое содержание жира на фоне снижения количества гемопоэтических клеток. Клеточность (общее содержание гемопоэтических стволовых клеток) – ниже 30%, могут отсутствовать мегакариоциты – клетки-предшественники тромбоцитов.
Степени тяжести апластической анемии
По результатам биопсии различают апластическую анемию лёгкой, тяжёлой и крайне тяжелой степени.
Тяжёлая форма болезни: клеточность – ниже 25%; в периферической крови: нейтрофилов –
Апластическая анемия
 Апластической анемией называют болезнь, при которой нарушается работа кроветворной системы.
Апластической анемией называют болезнь, при которой нарушается работа кроветворной системы.
Можно даже сказать, что это целая группа патологических состояний, которые представляют собой самостоятельную форму заболевания. При апластической анемии костный мозг перестает производить клетки крови в необходимом количестве: лейкоциты, тромбоциты и эритроциты. Различные виды болезни протекают по-разному, некоторые из них дают о себе знать сразу, а остальные проявляются только через время.
Тяжелая апластическая анемия требует обязательной госпитализации, так как она угрожает жизни больного. Критерии тяжелой формы заболевания заключаются в резком понижении уровня тромбоцитов в крови (менее 500/мкл), при этом также отмечается снижение нейтрофилов. Сверхтяжелая форма апластической анемии характеризуется критическим понижением нейтрофилов до 200/мкл.
Апластическая анемия у детей развивается в нескольких формах, которые характеризуются развитием определенных признаков. Самой тяжелой из них считается анемия Фанкони, при которой присутствуют врожденные дефекты развития костей, пороки сердца и почек.
История
Впервые это заболевание было описано Паулем Эрлихом в 1888 году у 21-летней женщины.
Термин «апластическая анемия» был предложен Чауфордом в 1904 году. Апластическая анемия — одно из самых тяжёлых расстройств гемопоэза. Без лечения больные тяжёлыми формами апластической анемии погибают в течение нескольких месяцев. При своевременном адекватном лечении прогноз достаточно хороший. Длительный период времени апластическая (гипопластическая) анемия рассматривалась как синдром, объединяющий патологические состояния костного мозга протекающие с выраженной гипоплазией кроветворения.
В настоящее время заболевание с названием «апластическая анемия» выделяют как самостоятельную нозологическую единицу — и чётко разграничивают его от синдрома гипоплазии кроветворения, являющегося проявлением ряда известных самостоятельных заболеваний костного мозга.
Причины развития
Многих интересует вопрос, что такое апластическая анемия и почему она появляется? К сожалению, современная медицина не может назвать очевидные причины развития апластической анемии у человека. Но известно, что болезнь бывает приобретённая и наследственная.
Существует теория, что развитие патологии связано с особенностями функционирования организма каждого индивида. Тем не менее отмечаются некоторые факторы, которые могут спровоцировать появление болезни. В частности, самым ясным из факторов является воздействие на человека ионизирующей радиации, которая подавляет функции костного мозга и приводит к снижению выработки им эритроцитов, тромбоцитов и лейкоцитов. Также к предрасполагающим факторам можно отнести следующие:
- плохая экологическая ситуация в регионе;
- регулярные контакты человека с вредными химическими веществами;
- некоторые инфекционные патологии, в частности, гепатит, цитомегаловирусная инфекция;
- проблемы с костным мозгом;
- приём некоторых медикаментов, в том числе обычных жаропонижающих и обезболивающих средств типа аспирина;
- частый приём антибиотиков, особенно левомицетина.
Обнаружено, что болезнь наблюдают у пациентов с чрезмерной тягой к алкоголю. Не последнюю роль в развитии болезни играет и генетическая предрасположенность. Апластическая анемия у детей часто развивается вследствие наследственных патологий, в том числе этом может быть анемия Фанкони. Необходимо отметить, что зачастую у детей диагностируется идиопатическая апластическая анемия – то есть патология с неясной этиологией.
Что касается такой патологии, как гипопластическая апластическая анемия – то это ещё более тяжёлая патология, вызывающая серьёзные нарушения в работе всех внутренних органов и приводящая к нарушению работоспособности систем организма.
Также следует сказать, что апластическая анемия бывает трёх форм тяжести:
- очень тяжелая (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелая (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренная (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Апластическую анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией.

Симптомы
Все симптомы апластической анемии объединяются в 3 основных группы синдромов: анемический синдром, геморрагический синдром, синдром инфекционных осложнений.
Анемический синдром характеризуется:
- выраженной общей слабостью;
- быстрой утомляемостью;
- непереносимостью привычных физических нагрузок;
- одышкой и тахикардией при умеренных нагрузках, в тяжелых случаях – в покое, при перемене положения тела;
- головными болями, головокружением, эпизодами обморока;
- шумом, звоном в ушах;
- чувством «несвежей головы»;
- мельканием «мушек», пятен, цветных полос перед глазами;
- болями колющего характера в области сердца;
- снижением концентрации;
- нарушением режима «сон – бодрствование» (сонливость днем, бессонница ночью).
Объективно при обследовании пациентов устанавливаются бледность кожных покровов и видимых слизистых оболочек, приглушенность тонов сердца, учащение пульса, снижение артериального давления.
Выделяют два пика заболеваемости: в 10–25 лет и после 60 лет. Чаще болеют женщины.
Геморрагический синдром проявляется:
- гематомами (синяками) разного размера и точечными кровоизлияниями, возникающими на коже и слизистых оболочках после незначительного воздействия или спонтанно, без причин;
- кровоточивостью десен;
- кровотечением из носа;
- у женщин – маточными межменструальными кровотечениями, длительными обильными менструациями;
- розовым окрашиванием мочи;
- определением следов крови в испражнениях;
- возможными массивными желудочно-кишечными кровотечениями;
- кровоизлияниями в склеру и глазное дно;
- кровоизлияниями в головной мозг и его оболочки;
- легочными кровотечениями.
Объективное подтверждение геморрагического синдрома – точечные кровоизлияния и кровоподтеки на коже и слизистых, множественные гематомы на разных стадиях (от пурпурно-фиолетовых до желтых).
Инфекционные осложнения представлены развивающимися пневмониями, пиелонефритами, фурункулезами, постинъекционными абсцессами или инфильтратами, в тяжелых случаях – сепсисом.
Признаки апластической анемии у детей
В детском возрасте чаще наблюдается врожденная патология, передаваемая от родителей либо приобретенная в период внутриутробного развития. Некоторые признаки такой патологии можно определить даже у новорожденного, другие могут проявиться только через несколько лет. К числу тяжелых симптомов анемии у новорожденных относятся:
- аномалии строения лица (треугольное лицо, маленькие глаза, курносый нос и др.);
- аномалии конечностей (отсутствие большого пальца на руках, отсутствие лучевой кости, шестипалость и др.);
- низкорослость;
- особенности пигментации кожи – это скопления множественных пятен светло-коричневого цвета;
- аномалии внутренних органов, чаще мочеполовой системы;
- деформация и разрушение ногтей;
- отставание в умственном развитии;
Апластическая анемия у детей старше 1 года первоначально определяется по внешнему виду, поведению. Больные дети отличаются от сверстников бледностью кожных покровов и слизистых оболочек, у них наблюдается увеличение размеров лимфатических узлов, случаются частые кровотечения из носа, десен, по утрам появляется кровь в моче. Их поведение характеризуется частой сменой настроения, раздражительностью, они быстро утомляются, теряют аппетит.
Диагностика
Гематологическое обследование включает внимательный клинический осмотр и проведение специальных диагностических исследований: общего и биохимического анализа крови, стернальной пункции, трепанобиопсии. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия.
Для гемограммы при апластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Исследование пунктата костного мозга показывает уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности; в трепанобиоптате обнаруживается замещение красного костного мозга жировым (желтым). В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.
Возможные осложнения и последствия
Апластическая анемия может осложняться:
- тяжелыми жизнеугрожающими кровотечениями;
- бактериальным эндокардитом;
- сепсисом;
- сердечной недостаточностью;
- почечной недостаточностью;
- реакцией отторжения при трансплантации костного мозга.
Лечение апластической анемии
При диагнозе апластическая анемия, лечение подбирается с учетом потенциальной причины, которая могла спровоцировать болезнь. Как только патология выявлена, больного нужно госпитализировать, только в больнице можно провести диагностику, подобрать и провести комплексное лечение, определить дозировку препаратов и курс терапии. Есть три способа лечения болезни:
- трансплантация;
- трансфузия;
- лечение с помощью медикаментов.
Трансплантацию считают одним из успешных способов помощи пациентам при апластической анемии. Суть процедуры заключается в пересадке костного мозга от донора. Прогноз после проведенной в больнице операции зависит от возраста пациента – чем он моложе, тем больше шансы на успех. В качестве донора может выступать близкий родственник пациента, у которого такая же группа крови.
До назначения пересадки, необходимо провести исследование, которое покажет, насколько совместимы будут клетки донора и реципиента. Перед трансплантацией проводится серьезная подготовка пациента, риск отторжения чужеродных тканей высокий. Перед трансплантацией костного мозга переливание крови не делают, проводят облучение, затем назначают химиотерапию.
Такая подготовка нужна, чтобы снизить иммунитет больного, чтобы он не атаковал чужеродные клетки на первых порах. Нужно учесть, что трансплантация мозга – затратная процедура, которая проводится в специализированных медицинских учреждениях.
Трансфузия – процедура, при которой больному переливают кровь. Для переливания используют препараты крови, подготовленные из крови доноров на станциях переливания. Методика дает лишь временный эффект, переливание частично восполняет дефицит клеток крови больного, но патология не лечится, костный мозг также остается неспособным производить собственные кровяные тельца. Недостатком трансфузионной терапии является невозможность проведения у пациентов с аутоиммунной формой патологии. Если трансфузия будет проводится часто, в печени и селезенке скапливается железо, врачи назначают пациентам медикаменты, способствующие его выведению из организма.
Лечение с помощью медикаментов проводится комплексно, пациенту назначают препараты из разных групп:
- иммунодепрессанты (специфические антиглобулины, Циклоспорин и пр.). Такие медикаменты нужны, если нет возможности пересадить костный мозг. Назначают иммуносупрессоры параллельно с гормонами, чтобы исключить анафилактическую реакцию;
- лекарства для стимуляции кроветворения (Филгастрим, Лейкомакс). Медикаменты этой группы активизируют в организме продуцирование лейкоцитов, поэтому целесообразно их назначать только при диагностировании лейкопении;
- андрогеносодержащие медикаменты (Тестостерона пропионат, Сустанон) назначаются мужчинам для подавления апластической анемии;
- гемостатики (аминокапроновая кислота и пр.) назначаются при выраженном геморрагическом синдроме;
- Десферал и его аналоги назначаются в случае необходимости избавиться от излишков железа в организме.
Другим методом лечения апластической анемии является спленэктомия (операция по удалению селезенки). Цель оперативного вмешательства – остановить происходящие в организме аутоиммунные процессы, из-за которых вырабатываются антитела к клеткам собственного костного мозга. У такой методики есть противопоказание – наличие инфекционных осложнений.
Прогноз для жизни
Ремиссию удаётся получить примерно у половины больных. Прогноз несколько лучше у детей, чем у взрослых.
Наличие большого количества жира в костном мозге не говорит о необратимости процесса. Бывают случаи, когда и у таких больных наступает полная ремиссия и полная репарация костномозгового кроветворения. Прогноз лучше, когда увеличено содержание ретикулоцитов, когда в костном мозге имеется более полиморфная картина, когда имеется небольшое увеличение размеров селезёнки и хотя бы небольшой, но чёткий эффект от кортикостероидных гормонов.
В этих случаях спленэктомия оказывает чаще хороший эффект вплоть до полного выздоровления. У части больных апластический синдром является началом острого лейкоза. Иногда признаки гемобластоза выявляются лишь через несколько лет от начала болезни.
Апластическая анемия ( Гипопластическая анемия )
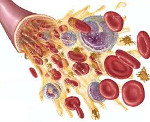
Апластическая анемия – угнетение функции кроветворения красного костного мозга (эритроцитопоэза, лейкопоэза и тромбоцитопоэза), приводящее к пангемоцитопении. К основным клиническим проявлениям гематологического синдрома принадлежат головокружение, слабость, обмороки, одышка, покалывание в груди, кожные геморрагии, кровотечения, склонность к развитию инфекционно-воспалительных и гнойных процессов. Заболевание диагностируется на основании характерных изменений гемограммы, миелограммы и гистологического исследования трепанобиоптата. Лечение патологии включает проведение гемотрансфузий, иммуносупрессивной терапии, миелотрансплантации.
МКБ-10

Общие сведения
Апластическая (гипопластическая) анемия – тяжелое расстройство гемопоэза (чаще всех его звеньев), сопровождающееся развитием анемического, геморрагического синдромов и инфекционных осложнений. Развивается в среднем у 2 человек на 1 млн. населения в год. Приблизительно с одинаковой частотой патология поражает мужчин и женщин. Возрастные пики заболеваемости приходятся на возраст 10–25 и старше 50 лет. При данной патологии в костном мозге чаще нарушается образование всех трех типов клеточных элементов крови (эритроцитов, лейкоцитов и тромбоцитов), иногда – только одних эритроцитов; в зависимости от этого различают истинную и парциальную апластическую анемию. В гематологии данный вид анемии относится к числу потенциально фатальных заболеваний, приводящих к гибели 2/3 заболевших.

Причины
По происхождению апластическая анемия может быть врожденной (связанной с хромосомными аберрациями) и приобретенной (развившейся в течение жизни). Принято считать, что угнетение миелопоэза связано с появлением в красном костном мозге и крови цитотоксических T-лимфоцитов, производящих фактор некроза опухолей и γ-интерферон, которые в свою очередь подавляют ростки кроветворения. Запускать этот механизм могут различные внешнесредовые (химические соединения, физические явления, лекарственные вещества), а также эндогенные факторы (вирусы, аутоиммунные реакции). К числу наиболее значимых причин относят:
- Прием миелотоксических препаратов. Достоверно установлена связь анемии с приемом некоторых противоопухолевых, противосудорожных, антибактериальных, антитиреоидных, противомалярийных препаратов, транквилизаторов, препаратов золота и др., обладающих потенциальным миелотоксическим эффектом. Лекарственные вещества могут вызывать как прямое повреждение стволовых кроветворных клеток, так и опосредованное – через аутоиммунные реакции. Анемии, связанные с таким механизмом развития, называются лекарственными.
- Контакт с химическими и физическими агентами. Супрессию костного мозга может вызывать взаимодействие с органическими растворителями, соединениями мышьяка, бензольными соединениями, пестицидами, облучение всего тела. В некоторых случаях недостаточность гемопоэза является временной и обратимой – главными факторами здесь являются концентрация/доза вещества и время контакта. супрессию костного мозга.
- Вирусные инфекции. Из вирусных агентов наибольшее значение уделяется возбудителям гепатитов В, С и D. В этом случае гипопластическая анемия обычно развивается в течение полугода после перенесенного вирусного гепатита. При изучении патогенеза было замечено, что репликация вируса происходит в мононуклеарах крови и костного мозга, а также в иммунных клетках. Предполагается, что подавление миелопоэза в этом случае является своеобразным иммунным ответом, возникающим против клеток, несущих на своей поверхности вирусные антигены. Такой вид анемии выделяется в отдельную форму – постгепатитную. Среди других вирусных инфекций называются ЦМВ, инфекционный мононуклеоз, грипп.
Также описаны случаи панцитопении, вызванные инфицированием туберкулезом, интоксикацией, лучевой болезнью, лимфопролиферативными заболеваниями (тимомой, лимфомой, хроническим лимфобластным лейкозом), беременностью. Почти в половине наблюдений причину анемии выявить не удается – такие случаи относят к идиопатической форме.
Патогенез
В основе апластической анемии может лежать либо первичное повреждение гемопоэтических стволовых клеток, либо нарушение их эффективной дифференцировки. При наследственных анемиях недостаточность гемопоэза опосредована кариотипическими аберрациями, приводящими к нарушению репарации ДНК и невозможности репликации стволовых клеток костного мозга. В случае приобретенной анемии под влиянием этиофакторов наблюдается активация Т-клеток, которые начинают продуцировать цитокины (интерферон-гамма, ФНО), поражающие клетки-предшественники гемопоэза. В стволовых клетках костного мозга повышается экспрессия генов, отвечающих за апоптоз и активизацию клеточной гибели. Основные клинические проявления обусловлены пангемоцитопенией – снижением в составе крови всех ее форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).
Классификация
Кроме различных этиологических вариантов (лекарственного, постгепатитного, идиопатического), различают острую (до 1 мес. течения), подострую (от 1 до 6 мес.) и хроническую (более 6 мес.) форму заболевания. Анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией. На основании выраженности тромбо- и гранулоцитопении данная форма анемии подразделяется на 3 степени тяжести:
- очень тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренную (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Симптомы апластической анемии
Поражение трех гемопоэтических ростков (эритро-, тромбоцито- и лейкопоэза) обусловливает развитие анемического и геморрагического синдромов, инфекционных осложнений. Дебют апластической анемии обычно происходит остро. Анемический синдром сопровождается общей слабостью и утомляемостью, бледностью кожи и видимых слизистых, шумом в ушах, головокружением, покалыванием в груди, одышкой при нагрузке.
Основным проявлением тромбоцитопении выступает геморрагический синдром. Больные отмечают появление петехий и экхимозов на коже, повышенную кровоточивость десен, спонтанные носовые кровотечения, меноррагии. Возможно возникновение гематурии, маточных и желудочно-кишечных кровотечений. Следствием лейкопении и агранулоцитоза служит частое развитие инфекционных процессов – стоматитов, пневмоний, инфекций кожи и мочевыводящих путей. Для апластической анемий нехарактерны похудание, лимфаденопатия, гепато- и спленомегалия – при этих признаках следует искать другую причину пангемоцитопении.
Врожденная апластическая анемия (синдром Фанкони) обычно развивается у детей в возрасте до 10 лет и кроме аплазии костного мозга характеризуется другими нарушениями: микроцефалией, гипоплазией почек, низкорослостью, аномалиями развития верхних конечностей (гипоплазией первой пястной и лучевой кости), гипоспадией, гиперпигментацией кожи, крайней степенью тугоухости и др. При наследственной анемии Эстрена-Дамешека отмечается тотальное поражение кроветворения и панцитопения при отсутствии врожденных аномалий развития. Для анемии Даймонда-Блекфена или парциальной красноклеточной аплазии характерно только снижение количества эритроцитов.
Осложнения
Летальный исход может быть обусловлен кровоизлияниями во внутренние органы, массивными кровотечениями, инфекционными осложнениями, анемической комой. Наиболее грозное из геморрагических осложнений – кровоизлияние в головной мозг (геморрагический инсульт). Больные склонны к частым и тяжело протекающим вирусным и бактериальным инфекциям респираторного тракта. Значительное или стремительное снижение уровня красных кровяных телец может привести к анемической коме. При молниеносной форме крайне быстро развиваются тяжелейшая анемия, иммунодефицит, коагулопатии, имеющие фатальные последствия.
Диагностика
Оценка гематологического статуса включает внимательный клинический осмотр и проведение тщательной лабораторной диагностики. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия. Основу диагностического алгоритма составляет проведение общего и биохимического анализа крови, стернальной пункции, трепанобиопсии:
- Исследования крови. Для гемограммы при гипопластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Оценка биохимических показателей (печеночных проб, нефрологического комплекса, сывороточного железа, билирубина) информативна для исключения других анемий.
- Исследованиепунктата костного мозга. В миелограмме обнаруживается уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности. В трепанобиоптате определяется замещение красного костного мозга жировым (желтым).
В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.
Лечение апластической анемии
Больные с апластической анемией госпитализируются в специализированные отделения. Им обеспечиваются полная изоляция и асептические условия для предупреждения возможных инфекционных осложнений. Проведение эффективного лечения является сложной проблемой практической гематологии. В зависимости от уровня цитопении используются следующие лечебные подходы:
- Иммуносупрессиная терапия. При умеренной цитопении назначается фармакотерапия, включающая комбинацию антитимоцитарного иммуноглобулина и циклоспорина А. Поддерживающая терапия проводится анаболическими стероидами или их сочетанием с циклоспоринами.
- Гемотрансфузии. В комплексе с курсом иммуносупрессивной терапии при низких показателях красной крови показано проведение заместительной гемотрансфузионной терапии (переливание тромбоцитов и эритроцитарной массы), плазмафереза. Данная мера не оказывает воздействия на патогенетическое звено заболевания, но позволяет восполнить дефицит кровяных телец, не вырабатываемых костным мозгом.
- Трансплантация КМ и СК. Наиболее благоприятные прогнозы на долгосрочную выживаемость оказывает выполнение аллогенной трансплантации костного мозга. Однако ввиду сложности подбора иммунологически совместимого донора процедура используется ограниченно. В качестве экспериментальных подходов рассматриваются аутологичные трансплантации, пересадка стволовых клеток периферической крови. Больным с нетяжелой формой анемии может быть показано проведение спленэктомии, эндоваскулярной окклюзии селезеночной артерии.
Прогноз и профилактика
Прогноз определяется этиологической формой, тяжестью и остротой течения анемии. Критериями неблагоприятного исхода служат быстрое прогрессирование заболевания, тяжелый геморрагический синдром и инфекционные осложнения. После трансплантации костного мозга ремиссии удается достичь у 75–90% пациентов. Первичная профилактика данной разновидности анемии предполагает исключение влияния неблагоприятных внешнесредовых факторов, необоснованного применения лекарственных препаратов, предупреждение инфекционной заболеваемости и др. Пациентам с уже развившимся заболеванием требуется диспансерное наблюдение гематолога, систематическое обследование и длительная поддерживающая терапия.