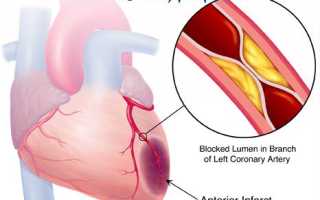
Дисфункция папиллярных мышц митрального клапана при инфаркте. Митрально папиллярная дисфункция Ишемическая дисфункция папиллярных мышц аускультативно
Дисфункция папиллярных мышц митрального клапана при инфаркте. Митрально папиллярная дисфункция Ишемическая дисфункция папиллярных мышц аускультативно
Острая дисфункция сосочковых мышц ЛЖ (вследствие их ишемии и некроза или образования аневризмы) у больных ИМ определяется в 10—50% случаев в течение первых дней (чаще при нижней локализации), когда на верхушке сердца появляется низкий, преходящий систолический шум различной интенсивности, длительности и иррадиации. Он может быть мягким, громким, высоко- и низкочастотным, занимать всю систолу. В первые часы ИМ этот шум можно выслушать у каждого 10-го больного. При митральной регургитации заметно снижается функция ЛЖ. В зависимости от выраженности дисфункции ЛЖ могут развиться проявления застоя крови в малом круге, ОЛ (постоянный или преходящий), гипотензии и КШ. Таким больным назначают вазодилататоры.
Диагностика. Метод выбора — ЭхоКГ
Лечение дисфункции сосочковых мышц. Острая дисфункция сосочковых мышц не требует специфической терапии. При наличии сильной регургитации (недостаточности МК) необходимо оперативное лечение (как при разрыве сосочковых мышц). В промежуточных случаях для снижения постнагрузки назначают ИАПФ
Митральная (ишемическая) регургитация (неблагоприятный прогностический показатель) встречается у 15-40% больных ИМ и в большинстве случаев является мягкой (или бессимптомной), носит транзиторный характер (вследствие динамической ишемии и дисфункции сосочковых мышц) и имеет относительно благоприятное течение. Другие причины митральной регургитации постинфарктное моделирование ЛЖ, приводящее к его дилатации (и соответственно к расширению митрального кольца), различная локальная деформация ЛЖ, способствующая нарушению всего аппарата МК (например, ненормальное движение стенок желудочков вблизи прикрепления задней части сосочковых мышц или частичный или полный разрыв струны, тянущей эти мышцы), и пролапс МК. У небольшого количества больных (4%) развивается значительная (тяжелая) митральная регургитация (обусловленная разрывом сосочковых мышц), приводящая к катастрофическим осложнениям, которые требуют срочного хирургического лечения.
Динамическое сужение путей оттока из ЛЖ — редкое осложнение ИМ, проявляющееся симптоматикой ОДН, повышенной потливостью и периферической гипоперфузией (холодная и влажная кожа конечностей) у больных со значительной выраженностью данной патологии. Возможно развитие КШ с выраженным ортопноэ, одышкой в покое, олигоуриеи, а также изменение социального статуса из-за снижения перфузии мозга.
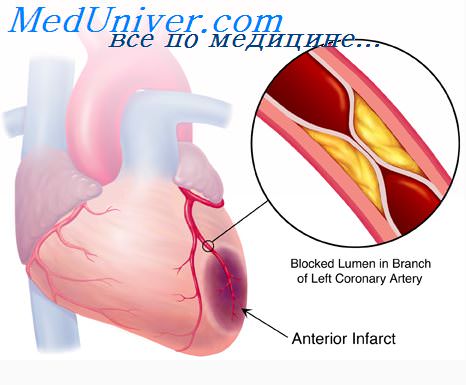
Это осложнение обусловлено гиперкинезией базальных и срединных сегментов ЛЖ. Повышение силы сокращения этих зон приводит к уменьшению площади отверстия оттока из ЛЖ. Результирующий рост скорости потока крови через суженные пути оттока может снижать давление ниже митрального клапана, вызывая смещение его створок вперед (эффект Вентури). Это приводит к дальнейшему сужению пути оттока из ЛЖ и появлению митральной регургитации. Полагают, что данное осложнение ИМ может играть определенную роль в разрыве свободной стенки ЛЖ посредством повышения напряжения стенки (из-за роста позднесистолического давления в камере ЛЖ) в зоне, ослабленной некрозом миокарда.
Объективно отмечаются тахикардия и снижение АД, выслушиваются новый систолический шум (лучше в верхней части тевого края грудины) с иррадиацией в шею и 3-й тон. В результате систолического движения митрального клапана вперед может появиться и систолический шум на верхушке с иррадиацией в подмышечную область.
Диагностика дисфункции сосочковых мышц. Диагностический метод выбора — ЭхоКГ, визуализирующие гиперкинетические сегменты, сужение путей оттока из ЛЖ и движение вперед створок МК.
Лечение дисфункции сосочковых мышц. Консервативное лечение основано на уменьшении ЧСС сократимости миокарда и постнагрузки, а также небольшом увеличении внутрисосудистого объема. Внутривенное вливание жидкости начинают с болюсов малых объемов (250 мл) физиологического раствора в целях повышения преднагрузки, уменьшения сужения путей оттока из ЛЖ и движения вперед створок МК.
Митральная недостаточность
Митральная недостаточность – клапанный порок сердца, характеризующийся неполным смыканием или пролабированием створок левого атриовентрикулярного клапана во время систолы, что сопровождается обратным патологическим током крови из левого желудочка в левое предсердие. Митральная недостаточность приводит к появлению одышки, утомляемости, сердцебиения, кашля, кровохарканья, отеков на ногах, асцита. Диагностический алгоритм выявления митральной недостаточности подразумевает сопоставление данных аускультации, ЭКГ, ФКГ, рентгенографии, эхокардиографии, катетеризации сердца, вентрикулографии. При митральной недостаточности проводится медикаментозная терапия и кардиохирургическое лечение (протезирование или пластика митрального клапана).
Общие сведения
Недостаточность митрального клапана – врожденный или приобретенный порок сердца, обусловленный поражением створок клапана, подклапанных структур, хорд или перерастяжением клапанного кольца, приводящим к митральной регургитации. Изолированная митральная недостаточность в кардиологии диагностируется редко, однако в структуре комбинированных и сочетанных пороков сердца встречается в половине наблюдений.
В большинстве случаев приобретенная митральная недостаточность сочетается с митральным стенозом (комбинированный митральный порок сердца) и аортальными пороками. Изолированная врожденная митральная недостаточность составляет 0,6% всех врожденных пороков сердца; в сложных пороках обычно сочетается с ДМПП, ДМЖП, открытым артериальным протоком, коарктацией аорты. У 5-6% здоровых лиц с помощью ЭхоКГ выявляется та или иная степень митральной регургитации.

Причины
Острая митральная недостаточность может развиваться вследствие разрывов сосочковых мышц, сухожильных хорд, отрыва створок митрального клапана при остром инфаркте миокарда, тупой травме сердца, инфекционном эндокардите. Разрыв сосочковых мышц вследствие инфаркта миокарда сопровождается летальным исходом в 80–90% случаев.
Развитие хронической митральной недостаточности может быть обусловлено поражением клапана при системных заболеваниях: ревматизме, склеродермии, системной красной волчанке, эозинофильном эндокардите Леффлера. Ревматическая болезнь сердца обусловливает около 14% всех случаев изолированной митральной недостаточности.
Ишемическая дисфункция митрального комплекса наблюдается у 10% пациентов с постинфарктным кардиосклерозом. К митральной недостаточности может приводить пролапс митрального клапана, надрыв, укорочение или удлинение сухожильных хорд и папиллярных мышц. В ряде случаев митральная недостаточность является следствием системных дефектов соединительной ткани при синдромах Марфана и Элерса-Данлоса.
Относительная митральная недостаточность развивается в отсутствие повреждения клапанного аппарата при дилатации полости левого желудочка и расширении фиброзного кольца. Такие изменения встречаются при дилатационной кардиомиопатии, прогрессирующем течении артериальной гипертензии и ИБС, миокардитах, аортальных пороках сердца. К более редким причинам развития митральной недостаточности относят кальциноз створок, гипертрофическую кардиомиопатию и др.
Врожденная митральная недостаточность встречается при фенестрации, расщеплении митральных створок, парашютовидной деформации клапана.
Классификация
По течению митральная недостаточность бывает острая и хроническая; по этиологии – ишемическая и неишемическая. Также различают органическую и функциональную (относительную) митральную недостаточность. Органическая недостаточность развивается при структурном изменении самого митрального клапана либо удерживающих его сухожильных нитей. Функциональная митральная недостаточность обычно является следствием расширения (митрализации) полости левого желудочка при его гемодинамической перегрузки, обусловленной заболеваниями миокарда.
С учетом выраженности регургитации выделяют 4 степени митральной недостаточности: с незначительной митральной регургитацией, умеренной, выраженной и тяжелой митральной регургитацией.
В клиническом течении митральной недостаточности выделяют 3 стадии:
I (компенсированная стадия) – незначительная недостаточность митрального клапана; митральная регургитация составляет 20-25% от систолического объема крови. Митральная недостаточность компенсируется за счет гиперфункции левых отделов сердца.
II (субкомпенсированная стадия) – митральная регургитация составляет 25-50% от систолического объема крови. Развивается застой крови в легких и медленное нарастание бивентрикулярной перегрузки.
III (декомпенсированная стадия) – резко выраженная недостаточность митрального клапана. Возврат крови в левое предсердие в систолу составляет 50-90% от систолического объема. Развивается тотальная сердечная недостаточность.
Особенности гемодинамики при митральной недостаточности
Вследствие неполного смыкания створок митрального клапана в период систолы возникает регургитационная волна из левого желудочка в левое предсердие. Если обратный ток крови незначителен, митральная недостаточность компенсируется усилением работы сердца с развитием адаптационной дилатации и гиперфункции левого желудочка и левого предсердия изотонического типа. Этот механизм может достаточно длительно сдерживать повышение давления в малом круге кровообращения.
Компенсированная гемодинамика при митральной недостаточности выражается адекватным увеличением ударного и минутного объемов, уменьшение конечного систолического объема и отсутствием легочной гипертензии.
При тяжелой форме митральной недостаточности объем регургитации преобладает над ударным объемом, минутный объем сердца резко снижен. Правый желудочек, испытывая повышенную нагрузку, быстро гипертрофируется и дилатируется, вследствие чего развивается тяжелая правожелудочковая недостаточность.
При остро возникшей митральной недостаточности адекватная компенсаторная дилатация левых отделов сердца не успевает развиться. При этом быстрое и значительное повышение давления в малом круге кровообращения нередко сопровождается фатальным отеком легких.
Симптомы митральной недостаточности
В периоде компенсации, который может длиться несколько лет, возможно бессимптомное течение митральной недостаточности. В стадии субкомпенсации появляются субъективные симптомы, выражающиеся одышкой, быстрой утомляемостью, тахикардией, ангинозными болями, кашлем, кровохарканьем. При нарастании венозного застоя в малом круге могут возникать приступы ночной сердечной астмы.
Развитие правожелудочковой недостаточности сопровождается появлением акроцианоза, периферических отеков, увеличением печени, набуханием шейных вен, асцитом. При компрессии возвратного гортанного нерва расширенным левым предсердием или легочным стволом возникает осиплость голоса или афония (синдром Ортнера). В стадии декомпенсации более чем у половины пациентов с митральной недостаточностью выявляется мерцательная аритмия.
Диагностика
Основные диагностические данные, свидетельствующие о митральной недостаточности, получают в ходе тщательного физикального обследования, подтвержденного электрокардиографией, фонокардиографией, рентгенографией и рентгеноскопией грудной клетки, ЭхоКГ и допплеровским исследованием сердца.
Вследствие гипертрофии и дилатации левого желудочка у больных с митральной недостаточностью развивается сердечный горб, появляется усиленный разлитой верхушечный толчок в V-VI межреберье от среднеключичной линии, пульсация в эпигастрии. Перкуторно определяется расширение границ сердечной тупости влево, вверх и вправо (при тотальной сердечной недостаточности). Аускультативными признаками митральной недостаточности служат ослабление, иногда полное отсутствие I тона на верхушке, систолический шум над верхушкой сердца, акцент и расщепление II тона над легочной артерией и др.
Информативность фонокардиограммы заключается в возможности подробно охарактеризовать систолический шум. ЭКГ-изменения при митральной недостаточности указывают на гипертрофию левого предсердия и желудочка, при легочной гипертензии – на гипертрофию правого желудочка. На рентгенограммах отмечается увеличение левых контуров сердца, вследствие чего тень сердца приобретает треугольную форму, застойные корни легких.
Эхокардиография позволяет определиться с этиологией митральной недостаточности, оценить ее тяжесть, наличие осложнений. С помощью допплерэхокардиографии выявляется регургитация через митральное отверстие, определяется ее интенсивность и величина, что в совокупности позволяет судить о степени митральной недостаточности. При наличии фибрилляции предсердий прибегают к чреспищеводной ЭхоКГ с целью выявления тромбов в левом предсердии. Для оценки тяжести митральной недостаточности применяется зондирование полостей сердца и левая вентрикулография.
Лечение митральной недостаточности
При острой митральной недостаточности требует введение диуретиков и периферических вазодилататоров. Для стабилизации гемодинамики может выполняться внутриаортальная баллонная контрпульсация. Специального лечения легкой бессимптомной хронической митральной недостаточности не требуется. В субкомпенсированной стадии назначаются ингибиторы АПФ, бета-адреноблокаторы, вазодилататоры, сердечные гликозиды, мочегонные препараты. При развитии фибрилляции предсердий применяются непрямые антикоагулянты.
При митральной недостаточности средней и тяжелой степени выраженности, а также наличии жалоб показано кардиохирургическое вмешательство. Отсутствие кальциноза створок и сохранная подвижность клапанного аппарата позволяет прибегнуть к клапансохраняющим вмешательствам – пластике митрального клапана, аннулопластике, укорачивающей пластика хорд и др. Несмотря на низкий риск развития инфекционного эндокардита и тромбозов, клапансохраняющие операции часто сопровождаются рецидивом митральной недостаточности, что ограничивает их выполнение достаточно узким кругом показаний (пролапс митрального клапана, разрывы клапанных структур, относительная недостаточность клапана, дилатация кольца клапана, планируемая беременность).
При наличии кальцификации клапана, выраженного утолщения хорд показано протезирование митрального клапана биологическим или механическим протезом. Специфическими послеоперационными осложнениями в этих случаях могут служить тромбоэмболии, атриовентрикулярная блокада, вторичный инфекционный эндокардит протезов, дегенеративные изменения биопротезов.
Прогноз и профилактика
Прогрессирование регургитации при митральной недостаточности наблюдается у 5–10% пациентов. Пятилетняя выживаемость составляет 80%, десятилетняя – 60%. Ишемическая природа митральной недостаточности быстро приводит к тяжелому нарушению кровообращения, ухудшает прогноз и выживаемость. Возможны послеоперационные рецидивы митральной недостаточности.
Митральная недостаточность легкой и умеренной степени не является противопоказанием к беременности и родам. При высокой степени недостаточности необходимо дополнительное обследование с всесторонней оценкой риска. Больные с митральной недостаточностью должны наблюдаться у кардиохирурга, кардиолога и ревматолога. Профилактика приобретенной недостаточности митрального клапана заключается в предупреждении заболеваний, приводящих к развитию порока, главным образом, ревматизма.
Митральная недостаточность

Митральная недостаточность – клапанный порок сердца, характеризующийся неполным смыканием или пролабированием створок левого атриовентрикулярного клапана во время систолы, что сопровождается обратным патологическим током крови из левого желудочка в левое предсердие. Митральная недостаточность приводит к появлению одышки, утомляемости, сердцебиения, кашля, кровохарканья, отеков на ногах, асцита. Диагностический алгоритм выявления митральной недостаточности подразумевает сопоставление данных аускультации, ЭКГ, ФКГ, рентгенографии, эхокардиографии, катетеризации сердца, вентрикулографии. При митральной недостаточности проводится медикаментозная терапия и кардиохирургическое лечение (протезирование или пластика митрального клапана).

Общие сведения
Недостаточность митрального клапана – врожденный или приобретенный порок сердца, обусловленный поражением створок клапана, подклапанных структур, хорд или перерастяжением клапанного кольца, приводящим к митральной регургитации. Изолированная митральная недостаточность в кардиологии диагностируется редко, однако в структуре комбинированных и сочетанных пороков сердца встречается в половине наблюдений.
В большинстве случаев приобретенная митральная недостаточность сочетается с митральным стенозом (комбинированный митральный порок сердца) и аортальными пороками. Изолированная врожденная митральная недостаточность составляет 0,6% всех врожденных пороков сердца; в сложных пороках обычно сочетается с ДМПП, ДМЖП, открытым артериальным протоком, коарктацией аорты. У 5-6% здоровых лиц с помощью ЭхоКГ выявляется та или иная степень митральной регургитации.

Причины
Острая митральная недостаточность может развиваться вследствие разрывов сосочковых мышц, сухожильных хорд, отрыва створок митрального клапана при остром инфаркте миокарда, тупой травме сердца, инфекционном эндокардите. Разрыв сосочковых мышц вследствие инфаркта миокарда сопровождается летальным исходом в 80–90% случаев.
Развитие хронической митральной недостаточности может быть обусловлено поражением клапана при системных заболеваниях: ревматизме, склеродермии, системной красной волчанке, эозинофильном эндокардите Леффлера. Ревматическая болезнь сердца обусловливает около 14% всех случаев изолированной митральной недостаточности.
Ишемическая дисфункция митрального комплекса наблюдается у 10% пациентов с постинфарктным кардиосклерозом. К митральной недостаточности может приводить пролапс митрального клапана, надрыв, укорочение или удлинение сухожильных хорд и папиллярных мышц. В ряде случаев митральная недостаточность является следствием системных дефектов соединительной ткани при синдромах Марфана и Элерса-Данлоса.
Относительная митральная недостаточность развивается в отсутствие повреждения клапанного аппарата при дилатации полости левого желудочка и расширении фиброзного кольца. Такие изменения встречаются при дилатационной кардиомиопатии, прогрессирующем течении артериальной гипертензии и ИБС, миокардитах, аортальных пороках сердца. К более редким причинам развития митральной недостаточности относят кальциноз створок, гипертрофическую кардиомиопатию и др.
Врожденная митральная недостаточность встречается при фенестрации, расщеплении митральных створок, парашютовидной деформации клапана.
Классификация
По течению митральная недостаточность бывает острая и хроническая; по этиологии – ишемическая и неишемическая. Также различают органическую и функциональную (относительную) митральную недостаточность. Органическая недостаточность развивается при структурном изменении самого митрального клапана либо удерживающих его сухожильных нитей. Функциональная митральная недостаточность обычно является следствием расширения (митрализации) полости левого желудочка при его гемодинамической перегрузки, обусловленной заболеваниями миокарда.
С учетом выраженности регургитации выделяют 4 степени митральной недостаточности: с незначительной митральной регургитацией, умеренной, выраженной и тяжелой митральной регургитацией.
В клиническом течении митральной недостаточности выделяют 3 стадии:
I (компенсированная стадия) – незначительная недостаточность митрального клапана; митральная регургитация составляет 20-25% от систолического объема крови. Митральная недостаточность компенсируется за счет гиперфункции левых отделов сердца.
II (субкомпенсированная стадия) – митральная регургитация составляет 25-50% от систолического объема крови. Развивается застой крови в легких и медленное нарастание бивентрикулярной перегрузки.
III (декомпенсированная стадия) – резко выраженная недостаточность митрального клапана. Возврат крови в левое предсердие в систолу составляет 50-90% от систолического объема. Развивается тотальная сердечная недостаточность.
Особенности гемодинамики при митральной недостаточности
Вследствие неполного смыкания створок митрального клапана в период систолы возникает регургитационная волна из левого желудочка в левое предсердие. Если обратный ток крови незначителен, митральная недостаточность компенсируется усилением работы сердца с развитием адаптационной дилатации и гиперфункции левого желудочка и левого предсердия изотонического типа. Этот механизм может достаточно длительно сдерживать повышение давления в малом круге кровообращения.
Компенсированная гемодинамика при митральной недостаточности выражается адекватным увеличением ударного и минутного объемов, уменьшение конечного систолического объема и отсутствием легочной гипертензии.
При тяжелой форме митральной недостаточности объем регургитации преобладает над ударным объемом, минутный объем сердца резко снижен. Правый желудочек, испытывая повышенную нагрузку, быстро гипертрофируется и дилатируется, вследствие чего развивается тяжелая правожелудочковая недостаточность.
При остро возникшей митральной недостаточности адекватная компенсаторная дилатация левых отделов сердца не успевает развиться. При этом быстрое и значительное повышение давления в малом круге кровообращения нередко сопровождается фатальным отеком легких.
Симптомы митральной недостаточности
В периоде компенсации, который может длиться несколько лет, возможно бессимптомное течение митральной недостаточности. В стадии субкомпенсации появляются субъективные симптомы, выражающиеся одышкой, быстрой утомляемостью, тахикардией, ангинозными болями, кашлем, кровохарканьем. При нарастании венозного застоя в малом круге могут возникать приступы ночной сердечной астмы.
Развитие правожелудочковой недостаточности сопровождается появлением акроцианоза, периферических отеков, увеличением печени, набуханием шейных вен, асцитом. При компрессии возвратного гортанного нерва расширенным левым предсердием или легочным стволом возникает осиплость голоса или афония (синдром Ортнера). В стадии декомпенсации более чем у половины пациентов с митральной недостаточностью выявляется мерцательная аритмия.
Диагностика
Основные диагностические данные, свидетельствующие о митральной недостаточности, получают в ходе тщательного физикального обследования, подтвержденного электрокардиографией, фонокардиографией, рентгенографией и рентгеноскопией грудной клетки, ЭхоКГ и допплеровским исследованием сердца.
Вследствие гипертрофии и дилатации левого желудочка у больных с митральной недостаточностью развивается сердечный горб, появляется усиленный разлитой верхушечный толчок в V-VI межреберье от среднеключичной линии, пульсация в эпигастрии. Перкуторно определяется расширение границ сердечной тупости влево, вверх и вправо (при тотальной сердечной недостаточности). Аускультативными признаками митральной недостаточности служат ослабление, иногда полное отсутствие I тона на верхушке, систолический шум над верхушкой сердца, акцент и расщепление II тона над легочной артерией и др.
Информативность фонокардиограммы заключается в возможности подробно охарактеризовать систолический шум. ЭКГ-изменения при митральной недостаточности указывают на гипертрофию левого предсердия и желудочка, при легочной гипертензии – на гипертрофию правого желудочка. На рентгенограммах отмечается увеличение левых контуров сердца, вследствие чего тень сердца приобретает треугольную форму, застойные корни легких.
Эхокардиография позволяет определиться с этиологией митральной недостаточности, оценить ее тяжесть, наличие осложнений. С помощью допплерэхокардиографии выявляется регургитация через митральное отверстие, определяется ее интенсивность и величина, что в совокупности позволяет судить о степени митральной недостаточности. При наличии фибрилляции предсердий прибегают к чреспищеводной ЭхоКГ с целью выявления тромбов в левом предсердии. Для оценки тяжести митральной недостаточности применяется зондирование полостей сердца и левая вентрикулография.
Лечение митральной недостаточности
При острой митральной недостаточности требует введение диуретиков и периферических вазодилататоров. Для стабилизации гемодинамики может выполняться внутриаортальная баллонная контрпульсация. Специального лечения легкой бессимптомной хронической митральной недостаточности не требуется. В субкомпенсированной стадии назначаются ингибиторы АПФ, бета-адреноблокаторы, вазодилататоры, сердечные гликозиды, мочегонные препараты. При развитии фибрилляции предсердий применяются непрямые антикоагулянты.
При митральной недостаточности средней и тяжелой степени выраженности, а также наличии жалоб показано кардиохирургическое вмешательство. Отсутствие кальциноза створок и сохранная подвижность клапанного аппарата позволяет прибегнуть к клапансохраняющим вмешательствам – пластике митрального клапана, аннулопластике, укорачивающей пластика хорд и др. Несмотря на низкий риск развития инфекционного эндокардита и тромбозов, клапансохраняющие операции часто сопровождаются рецидивом митральной недостаточности, что ограничивает их выполнение достаточно узким кругом показаний (пролапс митрального клапана, разрывы клапанных структур, относительная недостаточность клапана, дилатация кольца клапана, планируемая беременность).
При наличии кальцификации клапана, выраженного утолщения хорд показано протезирование митрального клапана биологическим или механическим протезом. Специфическими послеоперационными осложнениями в этих случаях могут служить тромбоэмболии, атриовентрикулярная блокада, вторичный инфекционный эндокардит протезов, дегенеративные изменения биопротезов.
Прогноз и профилактика
Прогрессирование регургитации при митральной недостаточности наблюдается у 5–10% пациентов. Пятилетняя выживаемость составляет 80%, десятилетняя – 60%. Ишемическая природа митральной недостаточности быстро приводит к тяжелому нарушению кровообращения, ухудшает прогноз и выживаемость. Возможны послеоперационные рецидивы митральной недостаточности.
Митральная недостаточность легкой и умеренной степени не является противопоказанием к беременности и родам. При высокой степени недостаточности необходимо дополнительное обследование с всесторонней оценкой риска. Больные с митральной недостаточностью должны наблюдаться у кардиохирурга, кардиолога и ревматолога. Профилактика приобретенной недостаточности митрального клапана заключается в предупреждении заболеваний, приводящих к развитию порока, главным образом, ревматизма.
Сосочковые мышцы сердца: для чего они нужны и за что отвечают?
Сосочковые мышцы входят в структуру клапанного аппарата и расположены в левом и правом желудочках сердца. Все их волокна сокращаются синхронно с систолой, регулируя закрытие клапанов.
Нарушение целостности папиллярных мышц относится к разновидности внутренних разрывов сердца. Такое состояние чаще всего развивается при расстройствах кровообращения в венечных артериях, как последствие острого инфаркта миокарда. Летальность от разрыва сосочковых мышц достигает 1% в течение первых двух недель.
Что представляют собой сосочковые мышцы сердца?
 Сосочковые мышцы (папиллярные) – продолжение внутреннего слоя сердечной мускулатуры, которое выступает в полость желудочков, и с помощью прикрепленных к верхушке хорд обеспечивает однонаправленный ток крови по камерам.
Сосочковые мышцы (папиллярные) – продолжение внутреннего слоя сердечной мускулатуры, которое выступает в полость желудочков, и с помощью прикрепленных к верхушке хорд обеспечивает однонаправленный ток крови по камерам.
Анатомическая классификация сосочковых мышц (СМ):
- Правого желудочка:
- Передняя.
- Задняя.
- Перегородочная.
- Левого желудочка:
- Передняя.
- Задняя.
Названия мышц соответствуют створкам клапана, к которым они крепятся при помощи хорд (тонких сухожильных нитей).
Схема папиллярных мышц у каждого человека индивидуальная:
- общее основание и несколько верхушек;
- 1 основание и заканчивается 1 верхушкой;
- несколько оснований, которые в апикальной части сливаются в 1 верхушку.
Следовательно, выделяют три вида СМ:
Форма папиллярных мышц также варьируется:
- цилиндрическая;
- коническая;
- четырехгранная пирамида с усеченной верхушкой.
Колеблется и общее количество сосочковых мышц у каждого индивидуума (от 2 до 6), поэтому створку клапана могут удерживать сразу несколько СМ.
Количество элементов связано с шириной сердца (чем уже – тем меньше папиллярных мускулов, и наоборот).
Высота мышц напрямую зависит от длины полости камеры. Толщина СМ колеблется от 0,75 до 2,6 см в левом желудочке, и 0,85-2,9 см – в правом. Эти два показателя пребывают в обратно пропорциональной зависимости (чем длинней мышца, тем она уже, и наоборот). Длина папиллярных мышц у мужчин на 1-5 мм больше, чем у женщин.
Основные функции
Конечная цель работы сосочковых мышц – обеспечение однонаправленного тока крови из предсердия в желудочек.
Во время систолы желудочков СМ сокращаются синхронно с миокардом и регулируют натяжение сухожильных хорд, крепящихся к краям атриовентрикулярных клапанов. Они натягивают створки на себя, не давая вернуться крови внутрь предсердий во время систолы. Тем самым, при помощи папиллярных мышц создается достаточный градиент давления на легочном и аортальном клапанах.
В начальной стадии систолы желудочков полулунные (аортальный и легочной) клапаны еще закрыты, а кровь по пути наименьшего сопротивления направляется обратно в предсердия. Но этому препятствует сокращение сосочковых мышц и быстрое смыкание створок клапана. На некоторое время создаются замкнутые полости желудочков, необходимые для нагнетания достаточного давления открытия полулунных клапанов.
Сосочковые мышцы обеспечивают правильное функционирование клапанной системы сердца. СМ не крепятся к створкам аортального и клапана легочной артерии, поскольку для их пассивного смыкания не требуется резкого перепада градиента давления.
Клапаны атриовентрикулярных соединений более массивны и требуют для эффективного закрытия быстрого и сильного давления обратного тока крови на протяжении нескольких миллисекунд.
Патологии
Патологические изменения в папиллярных мышцах могут возникать как первично, так и вследствие заболеваний других частей сердца.
Первичное поражение СМ в виде гипоплазии или аплазии встречается при:
- врожденной регургитации на митральном клапане;
- синдроме трисомии-18 (Эдвардса);
- аномалии Эбштейна – формировании створок из мышечной ткани желудочков.
Врожденные пороки митрального клапана (МК), которые служат основанием для дефекта папиллярных мышц:
- Добавочный МК – имеется дополнительный элемент с нетипичным креплением.
- Аркадный митральный клапан – СМ имеют аномальное строение, зачастую слиты в одну и гипертрофированы.
- Дополнительные створки (трех-, четырехстворчатый МК) – обнаруживаются добавочные группы сосочковых мышц.
- Парашютообразный МК – на ЭхоКГ определяется увеличенная папиллярная мышца, которая «связывает» одновременно две створки МК.
Во всех вышеперечисленных случаях неполноценные сосочковые мышцы усугубляют клинические проявления клапанной недостаточности.
Ткани СМ могут поражаться опухолевым процессом (чаще всего – лимфомой). Также папиллярные мышцы нередко подвергаются повреждению вследствие инфекционных заболеваний (эндокардита, ревматизма).
После перенесенной язвенного варианта инфекционного эндокардита наблюдается сращение между собой соседних сосочковых мышц с формированием клапанного порока с преобладанием недостаточности.
Изменения папиллярных мышц при пороках трикуспидального клапана:
- притупление верхушек СМ (в особенности передних);
- сращение передних папиллярных мышц с краевой зоной створок трикуспидального клапана;
- краевое срастание СМ со стенкой правого желудочка.
Изменения структуры сосочковых мышц при приобретенном стенозе митрального клапана:
- утолщение и удлинение СМ;
- срастание папиллярных мышц в единый конгломерат;
- припаивание краев СМ к поверхности левого желудочка;
- верхушки мышц припаяны к створкам митрального клапана.
Увеличение в размере СМ наблюдается при гипертрофической кардиомиопатии, поскольку папиллярные мышцы – продолжение внутреннего слоя миокарда желудочков. Увеличенные в размерах СМ сокращают полезный объем левых отделов, что снижает фракцию выброса и усугубляет гемодинамические расстройства.
В последние 70 лет появился термин «цирротическая кардиомиопатия» – изменение структуры и функционирования миокарда вследствие метаболических и гемодинамических расстройств, вызванных циррозом печени. Нарушение сократительной функции папиллярных мышц у таких пациентов ведет к формированию митральной и трикуспидальной недостаточности при интактной (неповрежденной) ткани клапана.
Разрыв сосочковых мышц
Разрыв сосочковой мышцы – тяжелое состояние, вызванное травмой или инфарктом миокарда с последующим «растворением» волокон. Такое осложнение в 5% случаев становится причиной смерти пациента.
Чаще некрозу подвергается задняя папиллярная мышца, что объясняется более скудным кровоснабжением в сравнении с передней.
Вследствие разрыва СМ во время систолы желудочка одна из створок митрального клапана (МК) проваливается в полость левого предсердия. Несостоятельность МК способствует перемещению крови в обратном направлении, что вызывает тяжелую недостаточность. Нарушение оттока жидкости ведет к повышению давления в легочных венах (кардиогенный отек) и падению показателей системной гемодинамики.
Основные симптомы и параклинические признаки разрыва:
- внезапное начало – боль в грудной клетке, учащенное сердцебиение, тяжелая одышка, выделение пенистой мокроты;
- аускультативно: мягкий шум в IV межреберье слева, усиливающийся во время систолы и проводится в подмышечную область;
- ослабление I тона на верхушке сердца;
- ЭхоКГ – М-образная хлопающая створка митрального клапана, которая при сокращении желудочков открывается в полость предсердия;
- допплерография – разной степени регургитация с турбулентным током крови.
Лечение разрывов сосочковых мышц – исключительно хирургическое, после предварительной медикаментозной стабилизации показателей. Суть вмешательства в постановке искусственного МК или удалении части створки с пластикой атриовентрикулярного отверстия. Ранняя летальность достигает 50% после ургентных кардиохирургических операций.
Также при Q-инфаркте миокарда у большинства пациентов к концу первой недели развивается дисфункция СМ, обусловленная ишемией и ремоделированием (перестройкой) мышечного «каркаса». Хирургического лечения это состояние не требует, симптомы уменьшаются на фоне интенсивной терапии инфаркта.
Выводы
Полный разрыв папиллярной мышцы сопровождается высоким риском смерти в течение суток. Надрыв СМ или повреждение одной из нескольких головок приводит к менее выраженной митральной регургитации с возможностью экстренного вмешательства и коррекции состояния. Острый инфаркт миокарда – опасная патология, которая угрожает жизни пациента даже после восстановления основной функции сердца. Необходимость длительного наблюдения в условиях кардиоцентра продиктована риском ранних осложнений, в том числе разрыва папиллярных мышц.
Для подготовки материала использовались следующие источники информации.