Какие этапы проходит лекарственное вещество в организме. Фармакокинетика лекарственных средств! Смотреть что такое “Фармакокинетика” в других словарях
Фармакокинетика лекарственных веществ
Всасывание(абсорбция) – есть преодоление барьеров, разделяющих место введения лекарства и кровяное русло.
Для каждого лекарственного вещества определяется специальный показатель – биодоступность. Она выражается в процентах и характеризует скорость и степень всасывания ЛС с места введения в системный кровоток и накопление в крови в терапевтической концентрации.
В фармакокинетике лекарственных препаратов выделяют четыре основных этапа.
Этап — всасывание.
В основе всасывания лежат следующие основные механизмы:
1. Пассивная диффузия молекул, которая идет в основном по градиенту концентрации. Интенсивность и полнота всасывания прямо пропорциональны липофильности, то есть, чем больше липофильность, тем выше способность вещества всасываться.
2. Фильтрациячерез поры клеточных мембран. Этот механизм задействован только при всасывании низкомолекулярных соединений, размер которых не превышает размер клеточных пор (вода, многие катионы). Зависит от гидростатического давления.
3. Активный транспорт обычно осуществляется с помощью специальных транспортных систем, идет с затратой энергии, против градиента концентрации.
4. Пиноцитоз характерен лишь для высокомолекулярных соединений (полимеров, полипептидов). Происходит с образованием и прохождением везикул через клеточные мембраны.
Всасывание лекарственных веществ может осуществляться этими механизмами при различных путях введения (энтеральных и парентеральных), кроме внутривенного, при котором препарат сразу поступает в кровоток. Кроме того, перечисленные механизмы участвуют в распределении и выведении лекарств.
Этап – распределение.
После попадания лекарственного вещества в кровь, оно разносится по всему организму и распределяется в соответствии со своими физико-химическими и биологическими свойствами.
В организме есть определенные барьеры, регулирующие проникновение веществ в органы и ткани: гематоэнцефалический (ГЭБ), гематоплацентарный (ГПБ), гематоофтальмологический (ГОБ) барьеры.
3 этап – метаболизм (превращение). Существуют два основных пути метаболизма лекарственных веществ:
ü биотрансформация, происходит под действием ферментов – окисление, восстановление, гидролиз.
ü конъюгация, при которой происходит присоединение к молекуле вещества остатков других молекул, с образованием неактивного комплекса, легко выводимого из организма с мочой или калом.
Эти процессы влекут за собой инактивацию или разрушение лекарственных веществ (детоксикацию), образование менее активных соединений, гидрофильных и легко выводимых из организма.
В ряде случаев лекарственный препарат становится активным лишь после реакций метаболизма в организме, то есть он является пролекарством, превращающимся в лекарство только в организме.
Главная роль в биотрансформации принадлежит микросомальным ферментам печени.
4 этап – выведение (экскреция). Лекарственные вещества через определенное время выводятся из организма в неизмененном виде или в виде метаболитов.
Гидрофильные веществавыделяются почками. Таким способом выделяется большинство ЛС.
Многие липофильные лекарственные веществавыводятся через печень в составе желчи, поступающей в кишечник. Выделившиеся в кишечник с желчью ЛС и их метаболиты могут выделиться с калом, повторно всосаться в кровь и снова через печень выделится с желчью в кишечник (энтерогепатическая циркуляция).
Лекарственные вещества могут выводиться через потовые и сальные железы (йод, бром, салицилаты). Летучие лекарственные вещества выделяются через легкие с выдыхаемым воздухом. Молочные железы выделяют с молоком различные соединения (снотворные, спирт, антибиотики, сульфаниламиды), что следует учитывать при назначении лекарственного средства кормящим женщинам.
Элиминация – процесс освобождения организма от лекарственного вещества в результате инактивации и выведения.
Общий клиренс ЛС(от англ. сlearance – очистка) – объем плазмы крови, очищаемый от ЛС за единицу времени (мл/мин) за счет выведения почками, печенью и другими путями.
Период полувыведения (Т0,5) – время, в течение которого концентрация активного лекарственного вещества в крови снижается в два раза.
Фармакодинамика
изучает локализацию, механизмы действия ЛС, а также изменения в деятельности органов и систем организма под влиянием лекарственного вещества, т.е. фармакологические эффекты.
Механизмы действия ЛС
Фармакологический эффект – воздействие лекарственного вещества на организм, вызывающее изменения в деятельности определенных органов, тканей и систем (усиление работы сердца, устранение спазма бронхов, понижение или повышение артериального давления и т.д.).
Способы, которыми лекарственные вещества вызывают фармакологические эффекты, определяются как механизмы действия лекарственных веществ.
Лекарственные вещества взаимодействуют со специфическими рецепторами клеточных мембран, через которые осуществляется регуляция деятельности органов и систем. Рецепторы – это активные участки макромолекул, с которыми специфически взаимодействуют медиаторы или гормоны.
Для характеристики связывания вещества с рецептором используется термин аффинитет.
Аффинитет определяется как способность вещества связываться с рецептором, в результате чего происходит образование комплекса «вещество-рецептор».
Лекарственные вещества, стимулирующие (возбуждающие) эти рецепторы и вызывающие такие эффекты, как и эндогенные вещества (медиаторы), получили название миметиков, стимуляторов или агонистов. Агонисты благодаря сходству с естественными медиаторами стимулируют рецепторы, но действуют более продолжительно в связи с их большей устойчивостью к разрушению.
Вещества, связывающиеся с рецепторами и препятствующие действию эндогенных веществ (нейромедиаторов, гормонов) называются блокаторами, ингибиторами или антагонистами.
Во многих случаях действие ЛС связано с их влияниями на ферментные системы или отдельные ферменты;
Иногда лекарственные средства угнетают транспорт ионов через клеточные мембраны или стабилизируют клеточные мембраны.
Ряд веществ влияют на метаболические процессы внутри клетки, а также проявляют другие механизмы действия.
Фармакологическая активность ЛС – способность вещества или комбинации нескольких веществ изменять состояние и функции живого организма.
Эффективность ЛС – характеристика степени положительного влияния ЛС на течение или продолжительность заболевания, предотвращение беременности, реабилитацию больных путем внутреннего или внешнего применения.
Фармакокинетика и её этапы.
Фармакокинетика(«человек – лекарство») — изучает влияние организма на лекарственное вещество, пути его поступления, распределения, биотрансформации и выведения лекарств из организма. Физиологические системы организма в зависимости от их врожденных и приобретенных свойств, а также способов и путей введения лекарственных препаратов будут в разной степени изменять судьбу лекарственного вещества. Фармакокинетика лекарственного вещества зависит от пола, возраста и характера заболевания.
Основным интегральным показателем для суждения о судьбе лекарственных веществ в организме является определение концентрации этих веществ и их метаболитов в жидкостях, тканях, клетках и клеточных органеллах.
Длительность действия препаратов зависит от его фармакокинетических свойств. Период полувыведения — время, необходимое для очищения плазмы крови от лекарственного вещества на 50%.
Этапы (фазы) фармакокинетики. Движение лекарственного вещества и изменение его молекулы в организме представляет собой ряд последовательных процессов всасывания, распределения, метаболизма и экскреции (выведения) лекарственных средств. Для всех этих процессов необходимым условием служит их проникновение через клеточные оболочки.
Прохождение лекарственных веществ через клеточные оболочки.
Проникновение лекарственных веществ через оболочки клеток регулируется естественными процессами диффузии, фильтрации и активного транспорта.
Диффузия основана на естественном стремлении любого вещества двигаться из области высокой концентрации в направлении к области более низкой концентрации.
Фильтрация. Водные каналы в местах тесного соединения прилегающих эпителиальных клеток пропускают через поры только некоторые водорастворимые вещества. Нейтральные или незаряженные (т. е. неполярные) молекулы проникают быстрее, так как поры обладают электрическим зарядом.
Активный транспорт – этот механизм регулирует движение некоторых лекарственных веществ в клетки или из них против концентрационного градиента. Для реализации этого процесса требуется энергия, и он происходит быстрее, чем перенос веществ путем диффузии. Молекулы со сходным строением конкурируют за молекулы-переносчики. Механизм активного транспорта высокоспецифичен для определенных веществ.
Некоторые органные особенности клеточных мембран.
Мозг и спинномозговая жидкость. Капилляры в мозге отличаются от большинства капилляров других участков организма тем, что их эндотелиальные клетки не имеют пространств, через которые вещества проникают во внеклеточную жидкость. Тесно примыкающие друг к другу эндотелиальные клетки капилляров, соединенные с базальной мембраной, а также тонкий слой отростков астроцитов препятствуют контакту крови с мозговой тканью. Этот гематоэнцефалический барьер предотвращает проникновение некоторых веществ из крови в мозг и спинномозговую жидкость (СМЖ). Жиронерастворимые вещества через этот барьер не проникают. Напротив, жирорастворимые вещества легко проникают через гематоэнцефалический барьер.
Плацента. Хорионические ворсины, состоящие из слоя трофобластов, т.е. клеток, окружающих капилляры плода, погружены в материнскую кровь. Кровоток беременной и плода разделены барьером, особенности которого те же, что у всех липидных мембран организма, т.е. он проницаем только для жирорастворимых веществ и непроницаем для веществ, растворимых в воде (особенно если их относительная молекулярная масса (ОММ) превышает 600). Кроме того, плацента содержит моноаминоксидазу, холинэстеразу и систему микросомальных ферментов (сходную с таковой в печени) способную метаболизировать лекарственные вещества и реагирующую на препараты, которые принимает беременная.
Всасывание — процесс поступления лекарства из места введения в кровеносное русло. Независимо от пути введения скорость всасывания препарата определяется тремя факторами: а) лекарственной формой (таблетки, свечи, аэрозоли); б) растворимостью в тканях; в) кровотоком в месте введения.
Существует ряд последовательных этапов всасывания лекарственных средств через биологические барьеры:
1) Пассивная диффузия. Таким путем проникают хорошо растворимые в липоидах лекарственные вещества. Скорость всасывания определяется разностью его концентрации с внешней и внутренней стороны мембраны;
2) Активный транспорт. В этом случае перемещение веществ через мембраны происходит с помощью транспортных систем, содержащихся в самих мембранах;
3) Фильтрация. Вследствие фильтрации лекарства проникают через поры, имеющиеся в мембранах (вода, некоторые ионы и мелкие гидрофильные молекулы лекарственных веществ). Интенсивность фильтрации зависит от гидростатического и осмотического давления;
4) Пиноцитоз. Процесс транспорта осуществляется посредством образования из структур клеточных мембран специальных пузырьков, в которых заключены частицы лекарственного вещества. Пузырьки перемещаются к противоположной стороне мембраны и высвобождают свое содержимое.
Распределение. После введения в кровеносное русло лекарственное вещество распределяется по всем тканям организма. Распределение лекарственного вещества определяется его растворимостью в липидах, качеством связи с белками плазмы крови, интенсивностью регионарного кровотока и другими факторами.
Значительная часть лекарства в первое время после всасывания попадает в те органы и ткани, которые наиболее активно кровоснабжаются (сердце, печень, легкие, почки).
Многие естественные вещества циркулируют в плазме частично в свободном виде, а частично в связанном состоянии с белками плазмы. Лекарственные средства также циркулируют как в связанном, так и в свободном состоянии. Важно, что фармакологически активна только свободная, несвязанная фракция препарата, а связанная с протеином представляет собой биологически неактивное соединение. Соединение и распад комплекса препарата с белком плазмы происходят как правило быстро.
Метаболизм (биотрансформация) — это комплекс физико-химических и биохимических превращений, которым подвергаются лекарственные вещества в организме. В результате образуются метаболиты (водорастворимые вещества), которые легко выводятся из организма.
В результате биотрансформации вещества приобретают большой заряд (становятся более полярными) и как следствие большую гидрофильность, т. е. растворимость в воде. Подобное изменение химической структуры влечет за собой изменение фармакологических свойств (как правило, уменьшение активности), скорости выделения из организма.
Это происходит по двум основным направлениям: а) снижение растворимости препаратов в жирах и б) снижение их биологической активности.
Этапы метаболизма:Гидроксилирование. Диметилирование. Окисление. Образование сульфоксидов.
Выделяют два типа метаболизма лекарственных препаратов в организме:
Несинтетические реакции метаболизма лекарств, осуществляемые ферментами. К несинтетическим реакциям относится окисление, восстановление и гидролиз. Они разделяют на катализируемые ферментами лизосом клеток (микросомальные) и катализируемые ферментами другой локализации (немикросомальные).
Синтетические реакции, которые реализуются с помощью эндогенных субстратов. В основе этих реакций лежит конъюгация лекарственных препаратов с эндогенными субстратами (глюкуроновая кислота, глицин, сульфаты, вода и др.).
Биотрансформация препаратов происходит главным образом в печени, однако она осуществляется также в плазме крови и в других тканях. Интенсивные и многочисленные реакции метаболизма протекают уже в стенке кишечника.
На биотрансформацию влияют заболевания печени, характер питания, половые особенности, возраст и ряд других факторов. При поражении печени усиливается токсическое действие многих лекарственных веществ на центральную нервную систему и резко возрастает частота развития энцефалопатии. В зависимости от тяжести заболевания печени, некоторые лекарственные препараты применяются с осторожностью или они вовсе противопоказаны (барбитураты, наркотические анальгетики, фенотиазины, андрогенные стероиды и др.).
Клинические наблюдения показали, что эффективность и переносимость одних и тех же лекарственных веществ у различных больных неодинакова. Эти отличия определяются генетическими факторами, детерминирующими процессы метаболизма, рецепции, иммунного ответа и др. Изучение генетических основ чувствительности организма человека к лекарственным веществам составляет предмет фармакогенетики. Проявляется это чаще всего недостаточностью ферментов, катализирующих биотрансформацию препаратов. Атипичные реакции могут проявляться и при наследственных нарушениях обмена веществ.
Синтез ферментов находится под строгим генетическим контролем. При мутации соответствующих генов возникают наследственные нарушения структуры и свойств ферментов — ферментопатии. В зависимости от характера мутации гена изменяется скорость синтеза фермента или синтезируется атипичный фермент.
Среди наследственных дефектов ферментных систем часто встречается недостаточность глюкозо-6-фосфатдегидрогенезы (Г-6-ФДГ). Она проявляется массивным разрушением эритроцитов (гемолитические кризы) при применении сульфаниламидов, фуразолидона и других препаратов. Кроме того, люди с недостаточностью Г-6-ФДР-чувствительны к пищевым продуктам, содержащим конские бобы, крыжовник, красную смородину. Существуют больные с недостаточностью ацетилтрансферазы, каталазы и других ферментов в организме. Атипичные реакции на лекарственные средства при наследственных нарушениях обмена веществ встречаются при врожденной метгемоглобинемии, порфирии, наследственных негемолитических желтухах.
Элиминация. Различают несколько путей выведения (экскреции) лекарственных веществ и их метаболитов из организма: с калом, мочой, выдыхаемым воздухом, слюнными, потовыми, слезными и молочными железами.
Элиминация почками. Экскреция лекарственных веществ и их метаболитов почками происходит с участием нескольких физиологических процессов:
Клубочковая фильтрация. Скорость, с которой вещество переходит в клубочковый фильтрат, зависит от его концентрации в плазме, ОММ и заряда. Вещества с ОММ более 50 000 не попадают в клубочковый фильтрат, а с ОММ менее 10 000 (т. е. практически большинство лекарственных веществ) фильтруются в почечных клубочках.
Экскреция в почечных канальцах. К важным механизмам экскреторной функции почек относится способность клеток проксимальных почечных канальцев активно переносить заряженные (катионы и анионы) молекулы из плазмы в канальцевую жидкость.
Почечная канальцевая реабсорбция. В клубочковом фильтрате концентрация лекарственных веществ та же, что и в плазме, но по мере продвижения по нефрону он концентрируется с увеличением концентрационного градиента, поэтому концентрация препарата в фильтрате превышает его концентрацию в крови, проходящей через нефрон.
Элиминация через кишечник.
После приема препарата внутрь для системного действия часть его, не абсорбируясь, может экскретироваться с каловыми массами. Иногда внутрь принимают лекарственные средства, специально не предназначенные для абсорбции в кишечнике (например, неомицин). Под влиянием ферментов и бактериальной микрофлоры желудочно-кишечного тракта лекарственные препараты могут превращаться в другие соединения, которые вновь могут доставляться в печень, где и проходит новый цикл.
К важнейшим механизмам, способствующим активному транспорту препарата в кишечник, относится билиарная экскреция (печенью). Из печени с помощью активных транспортных систем лекарственные вещества в виде метаболитов или, не изменяясь, поступают в желчь, затем в кишечник, где и выводятся с калом.
Степень выведения лекарственных веществ печенью следует учитывать при лечении больных, страдающих болезнями печени и воспалительными заболеваниями желчных путей.
Элиминация через легкие. Легкие служат основным путем введения и элиминации летучих анестезирующих средств. В других случаях медикаментозной терапии их роль в элиминации невелика.
Элиминация лекарственных веществ грудным молоком. Лекарственные вещества, содержащиеся в плазме кормящих женщин, экскретируются с молоком; их количества в нем слишком малы для того, чтобы существенным образом влиять на их элиминацию. Однако иногда лекарственные средства, попадающие в организм грудного ребенка, могут оказывать на него существенное воздействие (снотворные, анальгетики и др.).
Клиренс позволяет определить выведение лекарственного вещества из организма. Термином «почечный клиренс креатинина» определяют выведение эндогенного креатинина из плазмы. Большинство лекарственных веществ элиминируется либо через почки, либо через печень. В связи с этим общий клиренс в организме представляет собой сумму печеночного и почечного клиренса, причем печеночный клиренс рассчитывают путем вычитания значения почечного клиренса из общего клиренса организма (снотворные, анальгетики и др.).
Фармакокинетика
I
Фармакокинетика (греч. pharmakon лекарство kinētikos относящийся к движению)
раздел фармакологии, изучающий закономерности всасывания, распределения, метаболизма и выделения лекарственных средств. Исследование этих закономерностей основано на математическом моделировании указанных процессов. Определение фармакокинетических характеристик новых лекарственных веществ является важной частью их доклинического и клинического испытания.
Каждое лекарственное вещество подвергается в организме всасыванию, распределению и выделению (элиминации). Подавляющее большинство лекарственных веществ подвержено в организме также метаболическим превращениям.
Всасывание лекарственных веществ осуществляется за счет разных механизмов. Так, липофильные вещества всасываются главным образом путем пассивной диффузии через мембраны. Гидрофильные вещества с невысоким молекулярным весом (массой) проникают путем фильтрации через поры биологических мембран. Многие вещества всасываются за счет активного транспорта их молекул с помощью транспортных систем клеточных мембран. Вещества белковой природы всасываются, очевидно, путем пиноцитоза.
Распределение лекарственных веществ оценивается фармакокинетическими методами преимущественно по экстрацеллюлярной жидкости, включающей плазму крови, цереброспинальную жидкость, внутриглазную жидкость и жидкое содержимое желудочно-кишечного тракта. В норме объем экстрацеллюлярной жидкости у человека массой 70 кг принимается равным 15 л при общем количестве воды в организме около 40 л. Общий объем экстрацеллюлярной жидкости увеличивается при выпотах в брюшную и грудную полость и, отеках и т.п., что может отражаться на распределении лекарств в организме.
Распределение лекарственных средств в организме обеспечивается системой кровообращения. Равномерному распределению лекарств препятствуют мембраны органов, клеток и клеточных органелл. При переносе лекарственного средства через мембраны возможно его частичное связывание с ингредиентами биологических жидкостей по обе стороны мембраны. Существуют разные типы связывания лекарственных средств, отличающиеся по степени специфичности. Наиболее универсально связывание лекарств на поверхности белковых молекул, главным образом альбуминов крови. Оно происходит за счет гидрофобного взаимодействия и характеризуется быстрой обратимостью. В картине общего распределения препаратов их связывание с белками крови имеет двоякое значение. С одной стороны, оно может сопровождаться понижением концентрации активного препарата и в соответствии с этим ослаблением эффекта; с другой стороны, связывание способствует депонированию препарата и тем самым продлевает его пребывание в организме. Так, медленное выведение и значительная продолжительность эффекта сульфаниламидов длительного действия и доксициклина во многом обусловлены высокой степенью связывания этих препаратов с белками крови.
Известно также специфическое связывание лекарств некоторыми тканями. Так, хорошо растворимые в липидах вещества, например барбитураты, депонируются в жировой ткани. При выходе из наркоза или при диализе по поводу отравления барбитуратами проявляется феномен так называемого вторичного сна, развивающийся вследствие мобилизации этих веществ из жировых депо. Другим примером специфического депонирования лекарств у человека является накопление тетрациклинов в растущей костной ткани и дентине зубов.
Наиболее важным участком связывания лекарственных веществ являются специфические рецепторы. В области специфического рецептора концентрация лекарственного средства значительно превышает его концентрацию в окружающей биологической жидкости, но ввиду относительно малого размера рецептора это связывание обычно практически не отражается на общей картине распределения препарата в организме.
Лекарственные средства могут выделяться из организма в неизмененном виде или в виде метаболитов. Препараты, слаборастворимые в липидах, выделяются преимущественно почками в неизмененном виде. Препараты, относительно хорошо растворимые в липидах, подвергаются в почках обратному всасыванию эпителием канальцев и поступают вновь в систему кровообращения. Такие вещества выделяются почками лишь после того, как они путем метаболических превращений образуют хорошо растворимые в воде (полярные) соединения. Метаболические превращения лекарств в организме условно делят на два вида процессов — биотрансформацию и конъюгацию. Под биотрансформацией подразумевают реакции (окисление, восстановление, гидролиз), при которых одна функциональная группа молекулы лекарственного средства превращается в другую или в неполярное соединение вводится полярная группа. К реакциям конъюгации относятся биосинтетические процессы соединения лекарственных средств с эндогенными веществами, например с глюкуроновой, серной и уксусной кислотами, а также с α-аминокислотами или метильным радикалом.
Биотрансформация осуществляется в эндоплазматическом ретикулуме гепатоцитов и катализируется системой оксидаз. Конъюгация происходит также преимущественно в печени, но вне эндоплазматического ретикулума — в митохондриях или в растворимой фазе. Благодаря биотрансформации и конъюгации повышается гидрофильность лекарственных средств, в результате чего понижается степень их реабсорбции эпителием извитых канальцев почек. Глюкурониды, кроме того, могут секретироваться желчью и кишечным эпителием. Т.о., биологическое значение биотрансформации и конъюгации заключается в подготовке липидорастворимых лекарственных веществ к выведению из организма. При этом обычно происходит ослабление или наступает полная утрата фармакологической активности лекарственных веществ. Однако в процессе биотрансформации метаболиты некоторых препаратов могут становиться активнее исходных лекарств. Так, фтазин и фталазол в процессе метаболизма в организме образуют более активные молекулы норсульфазола и сульфапиридазина. В ряде случаев в результате метаболизма лекарств могут образовываться и токсические продукты. Выведение лекарств из организма происходит не только через почки, но также со слюной и через легкие.
Выведете препаратов с желчью или через стенку желудочно-кишечного тракта можно рассматривать в качестве экскреции или инкреции в зависимости от того, выводится ли препарат с фекалиями или всасывается в кишечнике вновь. В последнем случае существует возможность того, что при вторичном прохождении через печень с кровью воротной вены некоторая часть препарата будет вновь выделяться с желчью (образуется так называемый печеночно-кишечный круг обращения препарата). Такой особенностью Ф. отличаются дигитоксин, рифампицин и ряд других препаратов.
Фармакокинетические параметры зависят от состояния организма. На них влияет характер питания, климат, курение и другие факторы. Некоторые значения параметров генетически детерминированы, например скорость ацетилирования изониазида. Выведение препаратов у новорожденных происходит значительно медленнее, чем у взрослых. Но в течение первых лет жизни скорость элиминации резко возрастает, превышая скорость элиминации у взрослых. В пожилом возрасте скорость элиминации замедляется. Среди различных факторов, влияющих на процессы Ф., можно назвать и биоритмы.
Среди патологических состояний, влияющих на Ф. лекарственных средств, прежде всего следует отметить нарушение выделительной функции почек (Почки). Для многих лекарственных средств найдены эмпирические коэффициенты зависимости между показателем выделительной функции почек, с одной стороны, и величиной дозы и интервалов ее введения — с другой.
Значение Ф. для клинической медицины определяется ее практическими приложениями, важнейшими из которых являются: установление зависимости между степенью эффективности препарата и уровнем его в крови и основанная на этом оптимизация режима лечения; определение биологической доступности лекарственных средств из готовых форм; изучение взаимодействия лекарственных средств на путях их всасывания, распределения и элиминации (см. Несовместимость лекарственных средств). Знание Ф. каждого из применяемых я клинике лекарственных средств является одной из основ рациональной тактики лекарственного лечения.
Библиогр.: Лакин К.М. и Крылов Ю.Ф. Биотрансформация лекарственных веществ, М., 1981; Соловьев В.Н., Фирсов А.А. и Филов В.А. Фармакокинетика, М., 1980, библиогр.; Холодов Л.Е. и Яковлев В.П. Клиническая фармакокинетика. М., 1985, библиогр.
II
Фармакокинетика (Фармако- + греч. kinētikos относящийся к движению)
раздел фармакологии, изучающий пути поступления, распределение и метаболизм лекарственных веществ в организме, а также их выведение.
Фармакокинетика и фармакодинамика

Целью любого лечения является достижение желаемого терапевтического эффекта с минимальными побочными эффектами. При выборе подходящего лекарства для пациента, врач должен определить подходящую дозу для достижения своей терапевтической цели. А для этого, однако, нужно иметь базовые представления о фармакокинетике и фармакодинамике данного препарата.
Что такое фармакокинетика и фармакодинамика
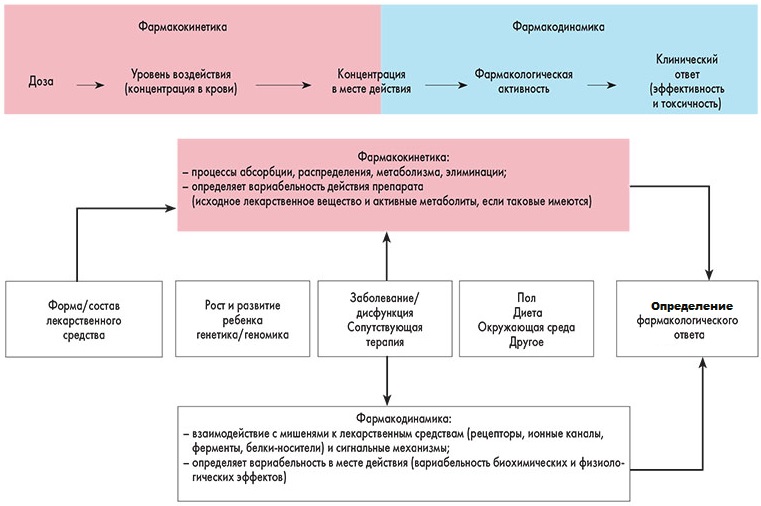
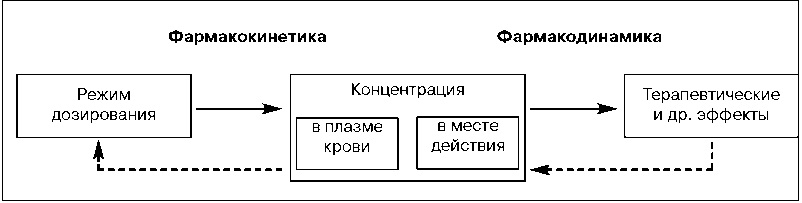
В общем смысле фармакодинамика охватывает эффект «концентрация-действие» препарата, а фармакокинетика отражает взаимодействие «доза-концентрация».
Фармакокинетические процессы включают процессы абсорбции, распределения и элиминации лекарственного средства и определяют, как быстро лекарство достигнет целевого органа и как долго оно будет в нем сохраняться.
Фармакокинетика – часть фармакологии, которая изучает «судьбу» лекарственного средства в организме после его введения: всасывание, распределение, метаболизм и выведение. Кроме того, фармакокинетика учитывает корреляцию между фармакокинетическими параметрами (пиковая концентрация, время, необходимое для достижения этого, объем распределения лекарственного средства, время полу-абсорбции, время полувыведения) и фармакологическими эффектами (желательным и нежелательным) для разработки безопасного и эффективного лекарственного средства, которое имеет постоянное начало и продолжительность действия.

Это тесно связано с биодоступностью (количество лекарственного средства, которое поступает в системную циркуляцию от использованного состава) и биоэквивалентностью (сравнение биодоступности двух составов). Чтобы достичь этого, фармакокинетика работает на основе фармакокинетических моделей, которые имитируют «судьбу» лекарственного средства в организме. Следовательно, существуют единичные или множественные (открытые или закрытые) системы, стационарные или динамические системы, кинетика линейных и нелинейных процессов с постоянными или переменными скоростями.
Стандартная доза каждого препарата определяется тщательным титрованием в процессе тестирования лекарств, но даже люди без медицинского образования понимают, что эта начальная доза подходит не каждому человеку. Физиологические процессы (такие как незрелость органов у новорожденного), а также патологические процессы (сердечная и / или почечная недостаточность) требуют введения отдельных доз препарата определенным категориям пациентов.
Особенности фармакокинетики
Существует пять основных фармакокинетических параметров:
- Очистка от препаратов – способность организма выводить лекарственные вещества.
- Объем распределения – измеряется пространство, доступное в организме, в котором будет «храниться» лекарство и которое будет служить резервуаром.
- Период полувыведения из плазмы – это время, которое требуется для выведения лекарственного средства из организма, чтобы в нем оставалась только половина первоначально введенной дозы.
- Лекарственное накопление – когда препарат вводится в многократных дозах, он накапливается в различной степени, пока не прекратится дозирование (его прием). Накопление зависит от конкретной дозы препарата, которая размывается между отдельными дозами препарата.
- Биодоступность – определяется как количество неизмененного лекарственного средства, которое достигает системного кровообращения, независимо от того, как вводится лекарственное средство: перорально, ректально или парентерально. Здесь следует упомянуть элиминацию, которая описывает и отражает процесс начального метаболизма лекарственного средства в основном в печени, но этот метаболизм может также происходить в кишечнике, а также в портальном кровотоке. Системная очистка лекарств не зависит от их биодоступности, но обратный процесс заключается в том, что очистка влияет на биодоступность, и это факт. Например, лидокаин не вводят перорально, поскольку биопродукты, полученные в результате его метаболизма, очень токсичны для нервной системы. Как можно видеть, метаболическое состояние печени играет важную роль в действии препарата. Люди делятся на «быстрых» и «медленных» метаболизаторов лекарственных препаратов, с соотношением от 15% до 85%. Кроме того, цирроз печени может вызвать резкое изменение общей кинетики данного препарата, равно как и наличие почечной недостаточности.
Терапевтическое и токсическое воздействие медсредств является результатом их взаимодействия, во-первых, с организмом пациента и, во-вторых, с другими лекарственными средствами. Большинство медпрепаратов действуют путем взаимодействия с определенными макромолекулами с последующей активацией различных биохимических каскадов в организме. Эти макромолекулы называются лекарственными рецепторами (ЛР).
Лекарственные рецепторы являются основным направлением в исследовании действия лекарств (фармакодинамика). Многие ЛР являются изолированными, и их структура известна в деталях. Модель присутствия ЛР также играет важную роль в создании и исследовании новых лекарств. Таким образом, современные знания о ЛР таковы:
- ЛР определяют качественные взаимодействия между дозой или концентрацией медсредства и его фармакологическим воздействием.
- ЛР ответственны за селективность действия препарата. Размер молекулы и электрическая нагрузка молекулы лекарственного средства определяет, будет ли молекула лекарственного средства связываться с рецептором медпрепарата.
- ЛР опосредуют действие фармакологических агонистов и антагонистов. Некоторые лекарства и природные лиганды, такие как нейротрансмиттеры, регулируют действие лекарственных рецепторов (действуют как агонисты). Другие лекарства действуют как антагонисты, то есть они связываются с рецептором, не генерирующим сигнал (как у агонистов). Другие антагонисты подавляют когда-то генерируемые сигналы от рецепторов (рестриктивная активность агонистов).
Особенности фармакокинетики и фармакодинамики
Целевая концентрация препарата
Рациональный режим дозирования лекарств основан на предположении, что он имеет целевую концентрацию, которая дает желаемый терапевтический эффект. Целевая концентрация напрямую связана с другой концепцией, а именно с «терапевтической шириной» лекарственного средства, то есть с разницей в концентрациях между самой низкой эффективной и концентрацией, при которой проявляются токсические эффекты препарата. Начальная целевая концентрация начинается с самой низкой эффективной концентрации препарата. Целевая концентрация также зависит от терапевтической цели, которую врачи ставят перед собой. Так, например, для контроля мерцательной аритмии требуется более высокая концентрация дигоксина – около 2 нанограмм / мл, а для лечения сердечной недостаточности требуются концентрации около 1 нанограмма / мл.
Поддерживающая доза препарата
В большинстве случаев препарат вводится таким образом, чтобы поддерживать его постоянную концентрацию. При каждом приеме достаточное количество лекарственного средства назначается для ликвидации его полного выведения из организма. Важным фактором также является последующая очистка организма от него.
Начальная доза препарата
Когда время для достижения поддерживающей дозы препарата относительно велико, используется вводная (восполняющая) доза препарата, которая быстро увеличивает концентрацию препарата до нужного количества.
Фармакокинетическая всасываемость
Количество лекарства, которое попадает в кровоток перорально, зависит от степени его перорального / желудочно-кишечного всасывания. То же относится и к трансдермально вводимым лекарствам.
Фармакодинамическая изменчивость
Для каждого фармакологического ответа также существует максимальный эффект, который часто представляет собой определенное количество, которое не изменяется с увеличением дозы (что объясняется количеством ЛР, содержащихся в организме).
Восприимчивость
Чувствительность органа-мишени к концентрации препарата определяется концентрацией, необходимой для воспроизведения 50% максимального эффекта препарата. Пониженная чувствительность может быть вызвана ненормальными физиологическими причинами.
Период полураспада
На это влияет как тип препарата, так и возраст пациента. Например, период полувыведения диазепама из плазмы увеличивается с возрастом (с 36 лет).