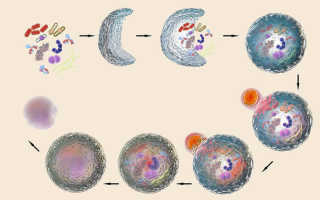
Механизм аутофагии. Аутофагия: что это такое и как она работает
Аутофагия для чайников: Как ускорить метаболическую аутофагию и почему вам стоит это сделать
Аутофагия – это биологический процесс, при котором части клеток перерабатываются и превращаются в запасные клетки. Это механизм утилизации, который предотвращает накопление старых и изношенных органелл. Аутофагия активируется во время голодания и недостатка энергии. Всякий раз, когда вашему организму не хватает жизненно важных питательных веществ, активируется аутофагия, позволяющая ему перерабатывать компоненты. Вы можете получить аналогичные результаты с помощью периодического и обычного голодания.
Сийм Лэнд, социокультурный антрополог, предприниматель и тренер высокой эффективности, который также является автором превосходной книги «Метаболическая аутофагия: практикуйте периодическое голодание и тренировки сопротивления для наращивания мышечной массы и повышения продолжительности жизни (Книга о диете спомощью метаболической аутофагии)».
Джозеф Меркола: Аутофагия и метаболизм
Я встретился с Лэндом на мероприятии Дейва Аспри в 2019 году в Upgrade Labs, формально известном как Пуленепробиваемая конференция, и был впечатлен глубиной его познаний. «Метаболическая аутофагия» – замечательное дополнение к книге «Жир в качестве топлива: революционная диета для борьбы с раком, ускорения работы мозга и повышения энергии».
Тем не менее, она хороша и сама по себе, так как она в деталях описывает конкретные протоколы, которым вы должны следовать. Важно отметить, что она проясняет одно из основных заблуждений относительно аутофагии о том, что, поскольку она полезна, вы должны активировать ее постоянно. Это не соответствует действительности и может иметь неприятные последствия, особенно если вы – человек в возрасте.
Один из способов оставаться в аутофагии – свести к минимуму количество белка, и если вы находитесь на постоянной диете с низким содержанием белка, вы никогда не активируете анаболизм, т.е. строительство мышечной ткани. Лэнд великолепно расправляется с этой путаницей и предоставляет конкретные протоколы цикличности, которые помогут вам поддерживать вашу мышечную массу и получить все преимущества аутофагии.
Аутофагия для чайников
Вкратце, аутофагия переводится как «самопоедание». Это биологический процесс, в котором части ваших клеток перерабатываются.
«Проще говоря, это механизм переработки, который предотвращает накопление старых и изношенных органелл, будь то расщепленные митохондрии, активные формы кислорода [или] воспалительные цитокины», – объясняет Лэнд.
«Аутофагия — это процесс, через который проходит ваше тело, когда оно хочет, или когда ему нужно восстановить и излечить себя. Он играет важную роль во многих заболеваниях, от которых мы страдаем. Аутофагия может принести пользу при таких состояниях, как резистентность к инсулину [и] заболевания печени.
Даже болезнь Альцгеймера и сердечная недостаточность в некоторой степени связаны с процессами аутофагии. Ее дефицит, как было показано, является причинным и способствует развитию этих заболеваний».
Как активировать аутофагию
Аутофагия активируется во время голодания и недостатка энергии. Всякий раз, когда ваше тело испытывает недостаток важных питательных веществ, таких как аминокислоты, белки, карбид, глюкоза или углерод, а это неполный список, активируется аутофагия, позволяющая вашему организму перерабатывать эти компоненты.
Также в игру вступают другие нижестоящие пути, такие как сиртуины, АМФ-активируемая протеинкиназа (АМФК) и FOX-белки, чтобы поддержать этот омолаживающий процесс. «Все они оказались центральными компонентами долголетия, когда речь идет о таких вещах, как ограничение калорий и физические упражнения», – говорит Лэнд.
Хорошей новостью является то, что ограничение калорий не является необходимым. Вы можете получить те же результаты с помощью периодического и обычного голодания. Ограничение калорий также имеет недостатки, такие как, например, дефицит питательных веществ, слабость, потеря мышечной массы и плотности костей, которые обходятся стороной при периодическом голодании.
Как и я, Лэнд использует ограниченное время приема пищи, съедая все в течение четырех часов каждый день. Я использую окно от четырех до пяти часов. Важно отметить, что это не то же самое, что ограничение калорий. Вы не ограничиваете количество потребляемых калорий; вы просто ограничиваете время, в которое вы их едите, и, таким образом, вы можете активировать аутофагию.
Аутофагия легко нарушается едой
Как объясняет Лэнд, даже небольшое количество пищи будет препятствовать аутофагии. «Съешьте бейгл – и это остановит аутофагию. А это буквально то, что едят на завтрак большинство людей в мире», говорит он. «Они немедленно ингибируют пользу ограничения калорий и прерывистого голодания, если нарушают аутофагию первым делом с утра».
Важно поддерживать близкое к нулю количество калорий, которое не повысит ваш инсулин и не переведет вас в анаболическое состояние (то есть в состоянии сытости). Другими словами, голодание позволяет вашему телу оставаться в аутофагии. Конечно, есть степени ингибирования в зависимости от типа питательных веществ, которые вы едите. Лэнд объясняет:
«Статус питательных веществ постоянно контролируется цензорами топлива, такими как mTOR, основной путь роста. Противоположностью этому является АМФК. Они, как инь и ян вашего метаболизма, постоянно следят за тем, какое топливо сгорает в крови.
Основываясь на этой информации, они решают, будут ли они расти или активировать аутофагию, чтобы перерабатывать себя. В течение дня эти топливные датчики уравновешивают друг друга, поэтому они не могут сосуществовать.
Всякий раз, когда вы съедаете бейгл, он повышает уровень инсулина и активирует путь mTOR, что переводит вас в состояние насыщения и препятствует аутофагии.
Но в то же время, если вы едите что-то более кетогенное, это приведет к значительно более низкому анаболическому ответу, потому что инсулин не повышается и в организм не поступают лишние аминокислоты.
Таким образом, есть определенная степень [ингибирования аутофагии], при том, что большое количество углеводов и белка являются более анаболическими и сильнее стимулирующими mTOR. Пища с низким содержанием углеводов, умеренным – белков и высоким – жира, будет сильнее стимулировать АМФК, [таким образом] она может поддерживать аутофагию дольше или намного легче».
Конечно, от продолжительности голодания также будет многое зависеть. Например, после 24- или 48-часового поста ваш АМФК будет намного выше, а mTOR значительно сильнее подавлен, чем после 16-часового голодания. В этом случае ваша буферная зона будет больше, а это означает, что определенные продукты не окажут столь сильного влияния на аутофагию.
Персональная программа Лэнда
Лэнд, который имеет телосложение опытного гимнаста, является отличным примером для подражания, и показывает, как хорошо спланированная программа, которая циклично проходит через аутофагию и анаболизм, может преобразить ваше тело. Его собственная программа, как правило, состоит из 20 часов голодания в день и еды в течение четырех часов.
Когда он перестает голодать раньше, скажем, через 16 или 18 часов вместо 20, он делает это, выпивая костный бульон или что-то подобное. Это нарушает пост, но не полностью. «Я по-прежнему буду поддерживать состояние полу-голодания до тех пор, пока у меня не останется калорий», – говорит он. Он также рассеивает опасения по поводу потери мышечной массы в результате голодания.
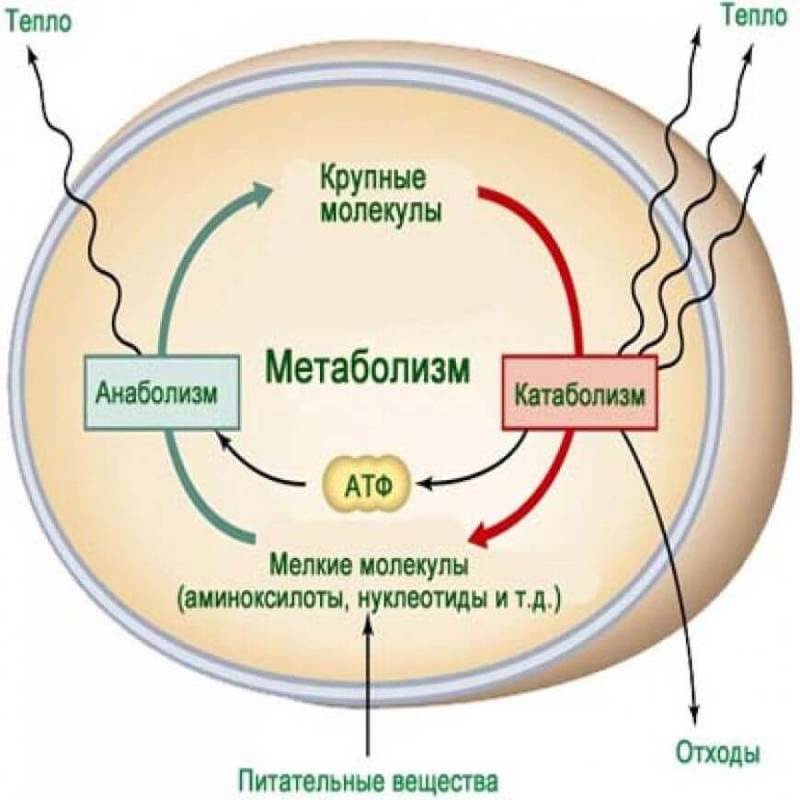
Катаболизм / анаболизм – вам нужны оба, но не одновременно
Вы можете активировать два различных метаболических пути: аутофагия (катаболизм, разрушение или восстановление ваших тканей) и mTOR (анаболизм, который является процессом восстановления). Путь mTOR по существу является чувствующим белки путем, который активируется белком и инсулином.
Раньше я был чрезмерно обеспокоен активацией mTOR, думая, что, вероятно, лучше ее избегать по максимуму, так как он является основной движущей силой хронических заболеваний и старения. Это не совсем верно, и книга Лэнда отлично рассеивает это распространенное заблуждение.
Как и в случае с аутофагией, нужно, чтобы mTOR был активирован не постоянно, но периодически.
Если вы проходите двухдневное голодание, это не время для тяжелых тренировок с нагрузкой, потому что это приведет к попытке активировать анаболизм и аутофагию одновременно. Это похоже на одновременное нажатие на педаль тормоза и газа, а это не очень хорошая идея. Итак, во время голодания помните, почему вы это делаете. Лэнд объясняет:
«Вы не можете нарастить мышечную массу с помощью длительного голодания. Его цель – углубиться в аутофагию и, по сути, способствовать клеточному очищению [и] исцелить себя.
В этот момент я не вижу смысла в попытках проводить напряженную тренировку с отягощениями, потому что, во-первых, у вас недостаточно энергии, чтобы достичь личного рекорда. Во-вторых, ваше тело не будет реагировать на это так же положительно. Скорее всего вы просто добавите дополнительную нагрузку на тело.
Во время продолжительного голодания я люблю проводить несколько более легких тренировок с массой тела или фитнес-резинками, просто чтобы стимулировать мышцы. Это сигнализирует организму о том, что ему по-прежнему необходимо сохранять больше мышечной ткани.
Если я буду выполнять утомительную тренировку, а потом ничего не буду есть, я настрою себя на провал. Это неизбежно приведет к усилению катаболизма мышц».
Выбор времени и польза анаболизма
Когда дело доходит до наращивания мышечной массы, время активации анаболизма может иметь большое значение. Чтобы его оптимизировать, нужно выполнять тяжелую тренировку с отягощениями, находясь в голодном состоянии, а затем заново наполнить организм пищей сразу после этого.
Как отмечает Лэнд, тренировка на голодный желудок может немного снизить вашу максимальную производительность, но вам не нужно тренироваться на максимуме, чтобы улучшить силу и мышечное развитие.
Тем не менее, есть некоторая польза от потребления небольшого количества белка прямо перед тренировкой. После этого обсуждения в книге Лэнда я начал есть два сырых яйца до начала упражнений.
«Для роста и сохранения мышц определенно стоит иметь некоторые аминокислоты и белок в системе, пока вы тренируетесь. Много не нужно. Вероятно, хватит и 10 грамм. Этого будет достаточно, и это не вызовет резкий всплеск инсулина. Это не выбьет вас из голодного состояния полностью», – говорит Лэнд.
Основы гормезиса
Лэнд также отлично справляется с определением гормезиса в своей книге. Это важная концепция, которую можно сформулировать так: «Все, что не убивает вас, делает вас сильнее». Это биологическая стратегия, которая позволяет вашему организму адаптироваться к стрессовым воздействиям окружающей среды, например, к ограничению калорий, к голоданию, холоду или жаре.
Гормезис также производит эффекты, подобные аутофагии, потому что он стимулируется аналогичными путями, включая АМФК, FOX-белки и сиртуины. Например, прерывистое голодание – это мягкий стрессор, который активирует гормезис. Высокоинтенсивное упражнение – другой, более интенсивный активатор.
В нашем интервью мы также обсудим другие преимущества саун ближнего инфракрасного диапазона и белков теплового шока, которые являются следствием аутофагии. Таким образом, основная функция белков теплового шока заключается в правильном фолдинге белков, что является одной из причин, почему сауна-терапия так полезна для общего состояния здоровья. Тепло также стимулирует аутофагию.
Подберите стратегию для своего возраста
Мы также обсуждаем важность никотинамидадениндинуклеотида (NAD+), кофермента, обнаруженного во всех клетках, который необходим для биологических процессов, включая энергетический гомеостаз. В молодости прием добавки NAD не обязателен, но с возрастом его уровень начинает снижаться.
Одним из крупнейших потребителей молекулы NAD+ является поли(АДФ-рибоза)-полимеразы (PARP), фермент восстановления ДНК. В настоящее время я исследую эту проблему, и кажется, что доза при терапии повышения уровня NAD сильно зависит от вашего возраста.
Людям до 30 или 40 лет, скорее всего, она не понадобится, если нет хронической проблемы со здоровьем. Однако, когда вам за 40, повышение уровня NAD становится важной стратегией.
Хорошей новостью является то, что есть много способов естественного повышения уровня NAD, таких как физические упражнения, которые резко увеличивают ограничивающий скорость образования фермент NAD, называемый никотинамидфосфорибозилтрансферазой или NAMPT. Голодание также увеличит уровень NAD, что является еще одним из его преимуществ.
Проблема, с которой сталкивается большинство людей, заключается в том, что они прекращают или радикально сокращают физические нагрузки, когда становятся старше. Хрупкость, которая ассоциируется со старостью, отчасти связана с накоплением никотинамида, который не превращается обратно в NAD. Он также ингибирует важные для долголетия белки сиртуины. Как только вы перестаете получать преимущества сиртуинов и NAD, продолжительность жизни сокращается.
Потребность в белке увеличивается с возрастом
Это важный момент, о котором Лэнд подробно рассказывает в своей книге. Уровень белка, в частности, меняется с возрастом, и для поддержания мышечной массы потребуются разные стратегии в зависимости от вашего возраста. По мере старения, наряду со снижением уровня НАД, вы также заметите снижение уровня гормона роста, а также способности синтезировать белок и строить ткани.
Лэнд также рекомендует циклически менять количество белка, которое вы потребляете. Например, в день голодания количество белка может быть небольшим, потому что он не нужен для восстановления мышц, тогда как более высокое потребление белка принесет вам наибольшую пользу в дни, когда вы выполняете силовые тренировки.
Лэнд рекомендует потребление минимум 0,6 г и максимум 0,8-1,0 г белка на фунт мышечной массы.
Чтобы рассчитать мышечную массу тела, определите процент жира в организме и вычтите его из общего веса. Итак, если у вас 20% жира, то ваша мышечная масса будет составлять 80% от общего веса. Затем умножьте это на, скажем, 0,8 грамма, чтобы рассчитать потребность в белке.опубликовано econet.ru.
Автор Джозеф Меркола
P.S. И помните, всего лишь изменяя свое сознание – мы вместе изменяем мир! © econet
Понравилась статья? Напишите свое мнение в комментариях.
Подпишитесь на наш ФБ:
Аутофагия: что это такое и как открытие нобелевского лауреата может хакнуть нашу жизнь
Японский учёный Ёсинори Осуми (Yoshinori Ohsumi) получил Нобелевскую премию по медицине за открытие механизмов аутофагии — процесса, в ходе которого клетки частично «поедают» себя, чтобы оставаться здоровыми. Открытия Осуми проливают свет на возможности использования аутофагии при лечении самых различных заболеваний.
Аутофагия — естественный процесс жизнедеятельности организма. Все клетки могут частично «поедать» себя, избавляясь от старых или повреждённых участков. Перерабатывая таким образом собственный материал, клетка получает новые ресурсы для восстановления и дальнейшего функционирования.
Аутофагия вовлечена в различные процессы: от борьбы с бактериальными и вирусными инфекциями до обновления клеток в развивающемся эмбрионе.
Ёсинори Осуми, специалист по клеточной биологии из Технологического университета Токио, начал изучать явление аутофагии ещё в 1992 году. Изначально он рассматривал гены, отвечающие за «самопоедание» в клетках дрожжей. Позже выяснилось, что процессы аутофагии оказывают влияние на различные болезни человека, среди которых рак, диабет, нейродегенеративные и инфекционные заболевания.
Сейчас учёные тестируют лекарства, которые смогут направленно воздействовать на процессы аутофагии. Это фундаментальным образом изменит наш подход к борьбе с раковыми опухолями, а также способы лечения психических расстройств, связанных с ухудшением когнитивных функций.
Контроль процессов аутофагии поможет в лечении рака и заболеваний мозга
Если процессы аутофагии замедляются или нарушаются, клетка теряет способность разрушать аномальные белки, отслужившие клеточные структуры и вредоносные микробы. Пока ещё не совсем ясна очерёдность событий: ведут ли нарушенные процессы аутофагии к возникновению болезни, или же болезнь вызывает сбой в работе механизмов аутофагии.
Тем не менее связь аутофагии с нейродегенеративными расстройствами не подвергается сомнению. Проявляется она, например, при болезни Паркинсона Melinda A. Lynch-Day, Kai Mao, Ke Wang. The Role of Autophagy in Parkinson’s Disease. . Для этого заболевания характерно наличие ненормальных белковых образований, телец Леви, которые распространяются в мозге. Учёные считают, что нарушенные процессы аутофагии как раз и приводят к тому, что клетки мозга прекращают «поедать» данные аномальные белки M. Xilouri M., O. R. Brekk OR, L. Stefanis. Autophagy and Alpha-Synuclein: Relevance to Parkinson’s Disease and Related Synucleopathies. .
Подобным образом в мозге могут образовываться и скопления амилоидов. Это вредный белок, который, по мнению учёных, вызывает болезнь Альцгеймера.
Возможность заново запустить процессы аутофагии у людей с нейродегенеративными заболеваниями позволит замедлить или даже полностью прекратить накопление в мозге вредных белков.
Это подтвердилось в первой фазе одного исследования, в ходе которого пациенты с болезнью Паркинсона и деменцией с тельцами Леви ежедневно получали небольшие дозы лекарства от лейкемии, стимулирующего процессы аутофагии. В течение шести месяцев пациенты заметили улучшение своих моторных навыков и мыслительной деятельности Cancer drug improved cognition and motor skills in small Parkinson’s clinical trial. .
Исследователи также рассматривают возможность того, что слишком активные процессы аутофагии могут способствовать развитию и распространению раковых клеток. Вероятнее всего, ускоренная аутофагия позволяет клеткам опухоли регенерировать быстрее обычного.
Сейчас проводятся клинические исследования, которые должны найти ответ на вопрос, действительно ли замедление процессов аутофагии поможет повысить эффективность таких традиционных методов лечения рака, как химиотерапия и облучение.
Хотя клеточные процессы, изучаемые Осуми, были уже известны учёным, до сих пор никто не видел их ценности для здоровья человека. Открытия Осуми проливают свет на возможности использования этих процессов при лечении различных заболеваний.
Узнав о присуждении ему Нобелевской премии, Осуми призвал молодых учёных присоединиться к нему в дальнейших исследованиях аутофагии.
В науке нет финишной черты. Когда находишь ответ на один вопрос, тут же возникает другой. Я никогда не считал, что ответил на все вопросы. Потому-то и продолжаю спрашивать у дрожжей.
Аутофагия, протофагия и остальные
- 4629
- 3,5
- 4
- 4
Протофагия концептуально является аналогом аутофагии в мире микробов
Автор
Редакторы
Аутофагия — это процесс, с помощью которого эукариотические клетки утилизируют свои внутренние компоненты, «переваривая» их ферментами лизосом. Это непрерывный процесс, поддерживающий баланс между синтезом и деградацией и обеспечивающий необходимые условия для нормального клеточного роста, развития и смерти. В этой статье мы обобщаем понятие аутофагии до общего принципа работы живых систем и предлагаем термин протофагия для обозначения прокариотических процессов, подобных аутофагии.
Аутофагия (от греч. αυτος — «само» и φαγειν — «есть»: самопоедание) является клеточным механизмом утилизации избыточных или поврежденных белков, белковых комплексов и клеточных органелл, осуществляемый лизосомами той же клетки. Такая утилизация выполняет несколько важных функций, в том числе — получение питательных веществ при голодании, поддержку клеточного гомеостаза и клеточного иммунитета, осуществление апоптоза и т.п. [1].
Как правило, термин аутофагия применяется для описания внутриклеточных процессов. Однако в определенном смысле ее можно рассматривать и как общий принцип, работающий не только на уровне клеток эукариот, но и в биосистемах других уровней, таких как организм, популяция или даже биосфера в целом. И на всех уровнях организации живого с принципом аутофагии можно соотнести многие известные процессы, — в частности, регуляцию жизнедеятельности бактериальных колоний. Здесь же мы рассмотрим аутофагию в более широком смысле — как процесс поглощения биологической системой своей части для поддержания собственной структуры и жизнедеятельности. Действительно: процессы, аналогичные аутофагии, появляются на разных «этажах» живой материи (см. примеры в таблице 1):
- в эукариотических клетках (как сообществах органелл);
- в организмах (как сообществах клеток и тканей);
- в экосистемах (как сообществах живых организмов), и наконец;
- во всей биосфере (как совокупности экосистем).
Например, на уровне организма одним из проявлений аутофагии является метаболизм подкожного жира, когда организм при голодании потребляет свою часть (жировую ткань) с перераспределением высвобожденной энергии. Другим примером служит апоптоз — регулируемое «самоубийство» клеток, необходимое для правильного развития любого растительного или животного организма [2].
Аутофагия присутствует и на уровне экосистем. Так же, как эукариотическая клетка постоянно утилизирует старые или дефектные органеллы, в экосистемах одни организмы «поглощаются» и служат источником энергии для других. Такой круговорот энергии и вещества в биосфере известен под термином «трофические цепи», которые можно определить как постоянное перераспределение биологического материала внутри экосистем.
Приведенные выше примеры аналогичны аутофагии в том, что в них для поддержания стабильности целого в жертву приносится часть системы. Так же, как аутофагия требуется эукариотической клетке для поддержания жизнедеятельности во время нехватки питательных веществ, сжигание жира организмом и экосистемные трофические цепи необходимы для адаптации к периодической нехватке энергии и стабилизации энергетического обмена.
Еще одна принципиальная функция процессов, подобных аутофагии, — обновление частей системы с целью поддержания ее стабильности как целого (гомеостаза). Время существования любого дифференцированного сообщества намного больше, нежели время жизни отдельных его частей, — вот тут-то и требуется механизм поддержания стабильности. Стабильность биосистем достигается путем постоянного обновления компонентов через аутофагию. Непрерывная утилизация старых компонентов обновляет биосистему, а также позволяет пополнить энергетические запасы. Этот же принцип используется и на других уровнях: в эукариотической клетке отработавшие свой ресурс органеллы перевариваются лизосомами, уступая место новым. На уровне организма поврежденные клетки элиминируются апоптозом или иммунной системой. В экосистемах отношения хищник–жертва не только поддерживают численность хищных видов, но и регулируют гомеостаз всей экосистемы, очищая ее от слабых и больных животных и предохраняя виды от вырождения.
Аутофагия является распространенным механизмом, используемым на различных уровнях биосферы. Почти любая живая система использует процессы, аналогичные аутофагии, для выживания и саморегуляции. Здесь мы использовали слово «почти», так как аутофагия до сих пор не была описана у прокариот [3]. Принимая во внимание роль аутофагии во всех других биосистемах, отсутствие ее у прокариот выглядит, по меньшей мере, странным. В этой статье мы попытаемся показать, что прокариоты не являются исключением, и аналог аутофагии у них также присутствует, — но обнаружить его можно лишь, если рассматривать прокариотические сообщества не как единичные клетки, а как мультиклеточные «организмы».
Прокариоты как многоклеточные организмы
На сегодня собрано достаточно данных о том, что в природе прокариоты существуют не в виде изолированных клеток, а в виде сложных микробных сообществ [4]. Впервые эта смелая идея была выдвинуты в 80-х годах ХХ века, а сегодня она подкреплена солидной экспериментальной базой. Природные колонии прокариот имеют аналог эндокринной сигнализации внутри сообщества (например, чувство кворума [5]), дифференциацию клеток на специализированные подвиды, а также сложные паттерны коллективного поведения (совместная охота, коллективное переваривание добычи, коллективная устойчивость к антибиотикам [4] и т.п.). Аутофагия как характеристика дифференцированных сообществ вполне может стать еще одним пунктом в этом списке.
Если бактериальная колония — это единая биосистема, то элементом ее будет служить единичная бактерия. Аналогично эукариотической органелле, прокариотическая клетка может рассматриваться как простейший элемент бактериального сообщества, окаймленный мембраной (и клеточной стенкой). Такое предположение ведет к интересному выводу: аутофагию нужно искать не внутри бактериальной клетки, а внутри бактериальной колонии. Действительно, «аутофагические» процессы хорошо известны у прокариотических колоний, правда под другими названиями — бактериальный каннибализм, бактериальный альтруизм, аутолиз или запрограммированная клеточная смерть [6–8]. Бактериальный каннибализм впервые был описан как ответ бактериальной колонии на нехватку питательных веществ (см. врезку). Биологический механизм, запускающий аутофагию в этом случае, обнаружен у многих видов бактерий — это так называемая токсин-антитоксиновая система. Суть ее состоит в том, что при голодании колония лизирует («переваривает») часть своих клеток для того, чтобы остальные бактерии получили достаточно пищи для выживания. Таким образом колония переживает нехватку ресурсов или внешние неблагоприятные условия.
«Аутофагия» у бактерий
Типичные аутофагические модели описаны на молекулярном уровне у многих бактерий. Например, при нехватке пищи часть бактерий в колонии выделяет в окружающую среду токсин. При этом только некоторые из них способны производить молекулу антитоксина — белка, который обезвреживает токсин при его попадании в клетку. Такие клетки выживают и поглощают остальные, погибшие и лизированные под действием токсина. Это дает оставшимся в живых энергию, необходимую для споруляции [6], [7]. Подобные процессы обнаружены у многих видов бактерий.
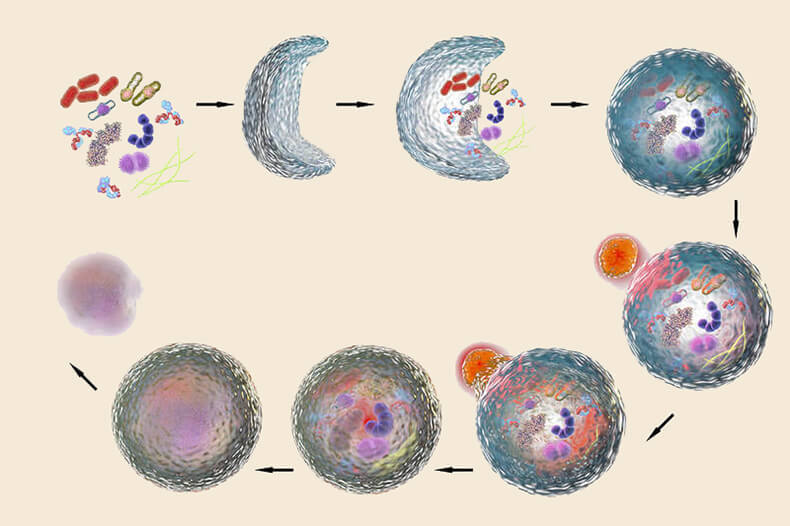
Для простоты описания мы введем термин протофагия как собирательный синоним процессов бактериального каннибализма, альтруизма, аутолиза и запрограммированной клеточной смерти. Прокариотическое сообщество представляет собой целостную биосистему, которая в случае необходимости перерабатывает часть себя для поддержания стабильности. При протофагии аутофагосомой (мембранной везикулы с продуктами деградации) служит сама прокариотическая клетка. Протофагия во многом схожа с аутофагией у эукариот (рис. 1):
- оба процесса оперируют «везикулами» аналогичного размера (размер бактерии примерно равен размеру митохондрии или пероксисомы);
- и про-, и аутофагия активируются подобными сигналами (голодание или стресс);
- оба процесса осуществляются по одному и тому же принципу (регулируемое потребление биосистемой своей части);
- оба процесса служат общей цели (выживание биосистемы в условиях стресса и поддержание ее гомеостаза).
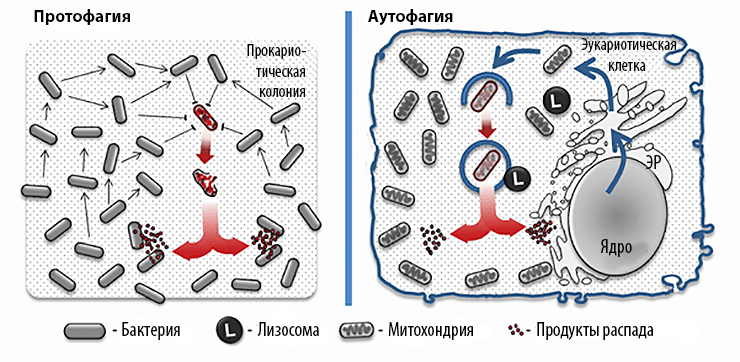
Рисунок 1. Принципиальная похожесть протофагии и аутофагии.
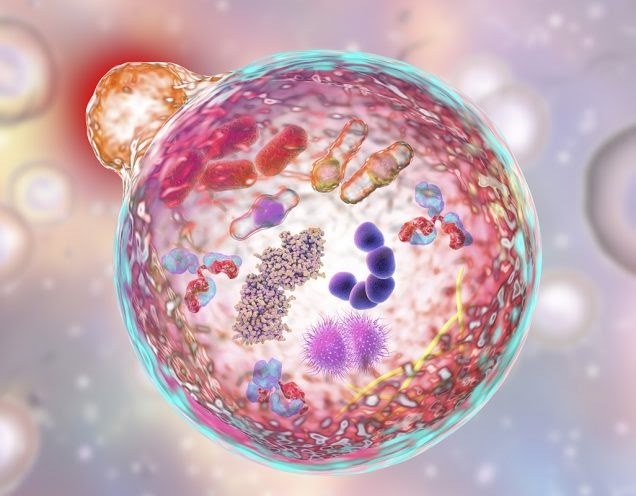
Как и эукариотическая аутофагия, протофагия используется не только для получения пищи. Например, протофагия служит патогенным бактериям для инвазии организма-хозяина (рис. 2). Известно, что микрофлора хозяина (симбионты) может эффективно сдерживать рост патогенных микроорганизмов. С целью подавления конкуренции некоторые патогенные бактерии с помощью протофагии активируют антибактериальный иммунный ответ организма-хозяина. Для этого часть патогенной популяции индуцированно самолизируется, высвобождая токсины, что вызывает локальное воспаление. В итоге иммунная система организма уничтожает большую часть бактерий-симбионтов, в то время как патогенные бактерии избегают обнаружения и после окончания воспалительной реакции беспрепятственно размножаются в тканях хозяина [9]. Интересно, что в отсутствие симбионтной микрофлоры (например, при экспериментальном заражении специальных линий стерильных мышей) такие патогенные бактерии заселяют кишечник без индукции воспаления. Это говорит о том, что протофагия тут является специфическим механизмом выживания патогенных организмов, который активируется только при неблагоприятных условиях.
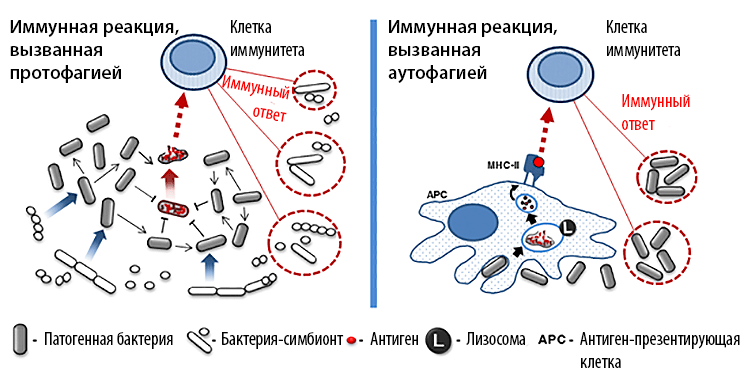
Рисунок 2. Аналогичная роль протофагии и аутофагии в активации иммунного ответа.
Что дает нам концепция протофагии
Введенное понятие протофагии интересно не только как голая теория, но может быть полезно и на практике. Например, в биотехнологии сегодня широко используют бактерии, и манипуляция процессами протофагии может подсказать способ поддержания стабильности бактериальной культуры в промышленных масштабах. Так, активаторы протофагии должны повысить качество культур путем активации естественных механизмов устранения ослабленных и поврежденных микроорганизмов.
Другой важной областью применения протофагии может стать медицина. На сегодняшний день резистентность бактерий к антибиотикам является одной из ключевых фармакологических проблем. Вместо того, чтобы убивать отдельные бактериальные клетки (как это делают сегодня с помощью антибиотиков), можно сконцентрироваться на дезорганизации бактериальных сообществ как единого целого. Такие методы уже разрабатываются — это, например, блокаторы бактериального «чувства кворума», которые нацелены именно на нарушение межклеточной сигнализации в бактериальных колониях, чтобы сделать их уязвимыми для иммунной системы человека [10], [11]. И хотя эта тема только развивается, и вопросов пока больше чем ответов, общий вектор работ показывает, что нарушение коммуникации между отдельными бактериями имеет все шансы стать терапией завтрашнего дня. В этом контексте активаторы протофагии помогут разрушить защитные барьеры бактериальной колонии и сделать ее уязвимой для иммунной системы организма хозяина.
Послесловие
Главный вопрос, который может возникнуть после прочтения этой статьи — а так ли необходимо введение нового термина — протофагия — для описания хорошо известных фактов? На наш взгляд, расширение понятия аутофагии и введение термина «протофагия» необходимо и полезно.
Биосфера в определенном смысле напоминает фрактал, где каждый последующий уровень повторяет предыдущий. Аналогичные процессы похожи между собой не только внешне — все они имеют сходные причины и принципы регуляции. Понятие протофагии, объединяющее разрозненные процессы прокариот вместе, позволяет обобщить и лучше понять глубинные механизмы, регулирующие жизнь прокариотических колоний. Это дает несомненные выгоды для биотехнологии и медицины завтрашнего дня.
Приживется ли термин «протофагия» и найдут ли его полезным другие ученые — покажет время. То, что нам показалось важным, мы изложили в статье, вышедшей в журнале Autophagy [12]. Если микробиологи воспримут эти обобщения и найдут их полезными для себя — нам будет очень приятно. Если же цитируемость нашей статьи не будет бить рекордов — значит, мы ударились в средневековую схоластику и переоценили значимость собственных измышлений. В любом случае, представить данную работу на суд почтенной публике стоило — ведь протофагия является частным случаем аутофагии в бактериальном мире и следует тем же законам, что и остальные ее проявления — будь то аутофагия в эукариотической клетке, трофические цепи в биосфере или голодание по модной методике перед пляжным сезоном, который, кстати, уже на носу.
Написано по материалам оригинального эссе в Autophagy [12].
Аутофагия, что это такое?
Аутофагия (или аутофагоцитоз) — это адаптационный механизм клетки, позволяющий переваривать собственные компоненты, чтобы повторно использовать их материал. Адаптация может противостоять широкому спектру неблагоприятных условий, в том числе гипогликемии, гипоксии, дефициту незаменимых аминокислот или факторов роста.
При недостатке питательных веществ или факторов роста возникает клеточный стресс, который приводит к усилению аутофагии. Таким образом, обеспечивается альтернативный источник внутриклеточных строительных блоков и субстратов, а также энергия для обеспечения непрерывного выживания клеток.
Этот процесс наблюдается во всех эукариотических системах, включая грибы, растения, плесень, нематод, насекомых, грызунов и других млекопитающих.
Аутофагия и гибель клеток
Аутофагия позволяет клеткам не только переживать стресс из внешней среды, но также противостоит внутренним стрессам, таким как накопление поврежденных органелл и проникновение патогенов или инфекционных организмов.
При определенных условиях аутофагия может убить клетку. Это относят к второму типу запрограммированной гибели клеток (ПКГ), называемым «аутофагической гибелью клеток». Другие виды запрограммированной гибели клеток включают апоптоз и некроз.
Далеко не все согласны с тем, что аутофагия может быть нацелена на смерть клетки. Есть множество исследований, которые говорят, что она является защитным механизмом, направленным на спасение клетки.
Однако этот процесс «спасения» часто ведет к аутофагической гибели клетки, когда все ее содержимое переваривается и остается лишь клеточный дебрис, который поглощают макрофаги.
Виды аутофагии
Существует несколько видов аутофагии, каждый из которых имеет свои особенности:
- Микроаутофагия. В этом процессе цитозольные компоненты непосредственно поглощаются самой лизосомой через лизосомальную мембрану. Это позволяет клетке переваривать белки при нехватке материала или энергии (например, при голодании)
- Макроаутофагия включает отделение участка клетки двойным мембраносвязанным пузырьком (аутофагосома), в котором содержатся удаляемые органеллы и цитоплазма. Этот пузырек сливается с лизосомой, образуя аутофаголизосому, где происходит переваривание органелл и остального содержимого
- Шапероновая аутофагия. В этом процессе целевые белки перемещаются из цитоплазмы в лизосому. Процесс проходит при участии шапероновых белков (таких как Hsc-70) и гликопротеина LAMP-2
- Митофагия — это избирательная деградация митохондрий. Митофагия предотвращает накопление дисфункциональных митохондрий, которые могут привести к клеточной дегенерации, а также способствует их обновлению
- Липофагия — это деградация липидов аутофагией. Мишенью являются липидные структуры, называемые липидными каплями (LDs). Липидные капли — это сферические «органеллы» с ядром, состоящим в основном из триацилглицеринов (TAG) и однослойных фосфолипидов и мембранных белков
Термин «аутофагия» обычно обозначает макроаутофагию, если не указано иное.
Что вызывает аутофагию
Аутофагия состоит из нескольких последовательных этапов:
- Секвестрация
- Деградация
- Генерация аминокислот и пептидов.
На каждом этапе, выполняются определённые функции, в зависимости от обстоятельств. Это делает аутофагию многофункциональной.
Наиболее типичным спусковым механизмом, вызывающим аутофагию, является голодание клетки, при котором обнаруживается недостаток какого-либо питательного вещества. Например, у дрожжей, наиболее мощным стимулом служит азотное голодание, но и нехватка других важных веществ, таких как углерод, ауксотрофные аминокислоты, нуклеиновые кислоты, тоже может вызвать аутофагию, хотя и менее эффективно (Takeshige et al. 1992). Азотное или углеродное голодание также вызывает аутофагию в растительных клетках.
У млекопитающих процесс аутофагии довольно сложен. Истощение общих аминокислот сильно индуцирует аутофагию во многих типах культивируемых клеток, но эффекты отдельных аминокислот различаются. Leu, Tyr, Phe, Gln, Pro, His, Trp, Met и Ala подавляют аутофагию в перфузированной печени ex vivo (Mortimore and Poso 1987). Однако есть зависимость от типа клеток, поскольку метаболизм аминокислот сильно различается в разных тканях. Например, лейцин оказывает доминирующее влияние на скелетные мышцы и сердце.
На сегодняшний день не выявлено, как именно клетки чувствуют концентрацию аминокислот. Одним из сенсоров-кандидатов является GCN2 тРНК-связывающая протеинкиназа, а также другие аминокислотные сигнальные пути, включающие фосфатидилинозитол-3-киназу (PI3) и Beclin 1.
Считается, что сигналы аминокислот, инсулина и факторов роста сходятся на mTOR (мишень рапамицина), который является основным регулятором передачи сигналов питательных веществ. Действительно, лечение ингибиторами TOR, такими как рапамицин и CCI-779, вызывает аутофагию у дрожжей (Noda и Ohsumi 1998) и животных (Ravikumar et al. 2004). Однако не все сигналы аутофагии передаются через mTOR, некоторые аминокислотные сигналы могут подавлять аутофагию mTOR-независимым образом (Mordier et al. 2000 и Kanazawa et al. 2004).
Селективность аутофагии
Аутофагию обычно считают неселективной системой деградации. Эта особенность резко контрастирует с системой убиквитин-протеасома, которая специфически распознает только убиквитинированные белки для протеасомной деградации. Убиквитин-протеасома имеет множество специфических функций, поскольку она может избирательно разрушать тысячи субстратов.
При нормальных условиях и в течение очень коротких периодов голодания, поддержание аминокислотного пула, по-видимому, зависит главным образом от системы убиквитин-протеасома, а не от аутофагии (Vabulas и Hartl 2005). Однако во время голодания, которое продолжается в течение нескольких часов, необходимые аминокислоты вырабатываются за счет аутофагии, которая активируется как адаптивный ответ.

Могут ли антациды повысить риск аллергии?

Космический корабль, плавающий на солнечном ветре, действительно работает