Воспалительный процесс. Макрофаги. Макрофагально-моноцитарная система Основные этапы развития, фенотипические характеристики, свойства апк. Современные методы выявления Вызывают макрофаги клетки захватывающие
Одураченные макрофаги, или Несколько слов о том, как злокачественные опухоли обманывают иммунитет
- 9216
- 7,9
- 5
- 4
Макрофаг атакует раковую клетку
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Иммунная система — это мощная многослойная защита нашего организма, которая потрясающе эффективна против вирусов, бактерий, грибов и других патогенов извне. Кроме того, иммунитет способен эффективно распознавать и уничтожать трансформированные собственные клетки, которые могут перерождаться в злокачественные опухоли. Однако сбои в работе иммунной системы (по генетическим либо другим причинам) приводят к тому, что однажды злокачественные клетки берут верх. Разросшаяся опухоль становится нечувствительной к атакам организма и не только успешно избегает уничтожения, но и активно «перепрограммирует» защитные клетки для обеспечения собственных нужд. Поняв механизмы, которые опухоль использует для подавления иммунного ответа, мы сможем разработать контрмеры и попытаться сдвинуть баланс в сторону активации собственных защитных сил организма для борьбы с болезнью.

Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».

Главный спонсор конкурса — дальновидная компания Генотек.
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Опухоль и иммунитет — драматический диалог в трех частях с прологом
Долгое время считалось, что причина низкой эффективности иммунного ответа при раке — то, что опухолевые клетки слишком похожи на нормальные, здоровые, чтобы иммунная система, настроенная на поиск «чужаков», могла их как следует распознавать. Этим как раз и объясняется тот факт, что иммунная система успешнее всего противостоит опухолям вирусной природы (их частота резко возрастает у людей, страдающих иммунодефицитом). Однако позже стало ясно, что это не единственная причина.
Если в этой статье речь идет про иммунные аспекты рака, то в работе «Страшней клешней на свете нет. » [1] можно прочесть про особенности ракового метаболизма. — Ред.
Оказалось, что взаимодействие раковых клеток с иммунной системой носит гораздо более разносторонний характер. Опухоль не просто «прячется» от атак, она умеет активно подавлять местный иммунный ответ и перепрограммировать иммунные клетки, заставляя их обслуживать собственные злокачественные нужды.
«Диалог» между переродившейся, вышедшей из-под контроля клеткой с ее потомством (то есть будущей опухолью) и организмом развивается в несколько стадий, и если вначале инициатива почти всецело находится на стороне защитных сил организма, то в конце (в случае развития болезни) — переходит на сторону опухоли. Несколько лет назад учеными-онкоиммунологами была сформулирована концепция «иммуноредактирования» (immunoediting), описывающая основные этапы этого процесса (рис. 1) [2].
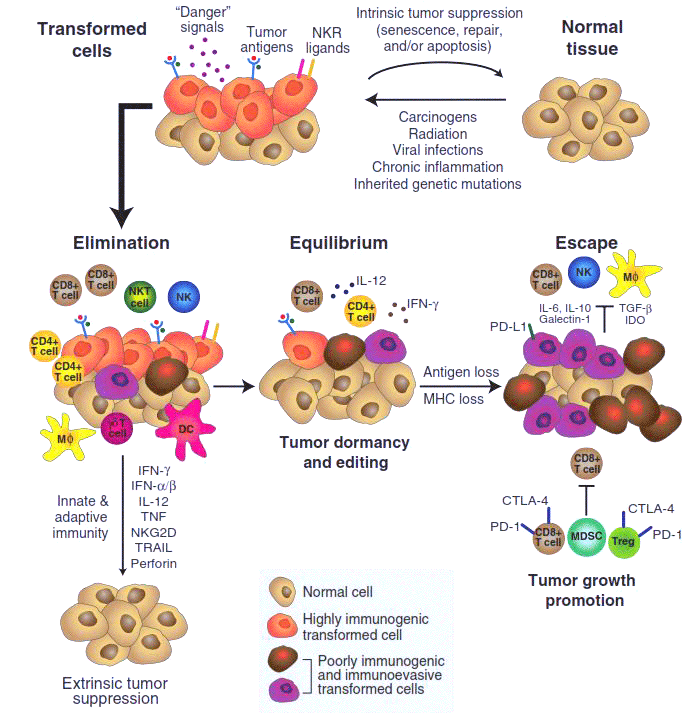
Рисунок 1. Иммуноредактирование (immunoediting) в процессе развития злокачественной опухоли.
Первая стадия иммуноредактирования — процесс устранения (elimination). Под действием внешних канцерогенных факторов или в результате мутаций нормальная клетка «трансформируется» — приобретает способность неограниченно делиться и не отвечать на регуляторные сигналы организма. Но при этом она, как правило, начинает синтезировать на своей поверхности особые «опухолевые антигены» и «сигналы опасности». Эти сигналы привлекают клетки иммунной системы, прежде всего макрофаги, натуральные киллеры и Т-клетки. В большинстве случаев они успешно уничтожают «испортившиеся» клетки, прерывая развитие опухоли. Однако иногда среди таких «предраковых» клеток оказывается несколько таких, у которых иммунореактивность — способность вызывать иммунный ответ — по каким-то причинам оказывается ослабленной, они синтезируют меньше опухолевых антигенов, хуже распознаются иммунной системой и, пережив первую волну иммунного ответа, продолжают делиться.
В этом случае взаимодействие опухоли с организмом выходит на вторую стадию, стадию равновесия (equilibrium). Здесь иммунная система уже не может полностью уничтожить опухоль, но еще в состоянии эффективно ограничивать ее рост. В таком «равновесном» (и не обнаруживаемом обычными методами диагностики) состоянии микроопухоли могут существовать в организме годами. Однако такие затаившиеся опухоли не статичны — свойства составляющих их клеток постепенно меняются под действием мутаций и последующего отбора: преимущество среди делящихся опухолевых клеток получают такие, которые способны лучше противостоять иммунной системе, и в конце концов в опухоли появляются клетки-иммуносупрессоры. Они в состоянии не только пассивно избегать уничтожения, но и активно подавлять иммунный ответ. По сути, это эволюционный процесс, в котором организм невольно «выводит» именно тот вид рака, который его убьет.
Этот драматический момент знаменует собой переход опухоли к третьей стадии развития — избегания (escape), — на которой опухоль уже малочувствительна к активности клеток иммунной системы, более того — обращает их активность себе на пользу. Она принимается расти и метастазировать. Именно такая опухоль обычно диагностируется медиками и изучается учеными — две предыдущие стадии протекают скрыто, и наши представления о них основаны главным образом на интерпретации целого ряда косвенных данных.
Дуализм иммунного ответа и его значение в канцерогенезе
Существует множество научных статей, описывающих, как иммунная система борется с опухолевыми клетками, но не меньшее количество публикаций демонстрирует, что присутствие клеток иммунной системы в ближайшем опухолевом окружении является негативным фактором, коррелирующим с ускоренным ростом и метастазированием рака [2], [3]. В рамках концепции иммуноредактирования, описывающей, как изменяется характер иммунного ответа по мере развития опухоли, подобное двойственное поведение наших защитников получило, наконец, свое объяснение.
Переориентирование иммунной системы от борьбы с опухолью на ее защиту возможно благодаря пластичности клеток этой системы. Говоря об иммунном ответе, мы, как правило, используем «воинственные» метафоры — «борьба», «уничтожение», «подавление». Но мало уничтожить врага, будь то вирус, бактерия или другой паразит. Организм должен еще и исправить причиненные им повреждения. Регенерация поврежденных тканей и заживление ран тоже находятся под контролем клеток иммунной системы: она не только «воин», но еще и «целитель». Коварство рака заключается в том, что, будучи по сути «чужеродным агентом» в организме, он выделяет специальные вещества, которые подавляют активный иммунный ответ и побуждают лейкоциты воспринимать опухоль не как врага, требующего уничтожения, а как рану, требующую помощи, защиты и исцеления.
Мы рассмотрим некоторые механизмы того, как это происходит, на примере макрофагов. Похожие приемы опухоль использует и для того, чтобы обманывать другие клетки врожденного и приобретенного иммунитета.
Макрофаги — «клетки-воины» и «клетки-целители»
Макрофаги, пожалуй, самые знаменитые клетки врожденного иммунитета — именно с изучения их способностей к фагоцитозу Мечниковым и началась классическая клеточная иммунология. В организме млекопитающих макрофаги — боевой авангард: первыми обнаруживая врага, они не только пытаются уничтожить его собственными силами, но также привлекают к месту сражения другие клетки иммунной системы, активируя их. А после уничтожения чужеродных агентов принимаются активно участвовать в ликвидации причиненных повреждений, вырабатывая факторы, способствующие заживлению ран. Эту двойственную природу макрофагов опухоли используют себе на пользу.
В зависимости от преобладающей активности различают две группы макрофагов: М1 и М2. М1-макрофаги (их еще называют классически активированными макрофагами) — «воины» — отвечают за уничтожение чужеродных агентов (в том числе и опухолевых клеток), как напрямую, так и за счет привлечения и активации других клеток иммунной системы (например, Т-киллеров). М2 макрофаги — «целители» — ускоряют регенерацию тканей и обеспечивают заживление ран [4], [8].
Присутствие в опухоли большого количества М1-макрофагов тормозит ее рост [5], а в некоторых случаях может вызвать даже практически полную ремиссию (уничтожение). И наоборот: М2-макрофаги выделяют молекулы — факторы роста, которые дополнительно стимулируют деление опухолевых клеток, то есть благоприятствуют развитию злокачественного образования. Экспериментально было показано, что в опухолевом окружении обычно преобладают именно М2-клетки («целители»). Хуже того: под действием веществ, выделяемых опухолевыми клетками, активные М1-макрофаги «перепрограммируются» в М2-тип [6], перестают синтезировать антиопухолевые цитокины, такие как интерлейкин-12 (IL12) или фактор некроза опухолей (TNF) и начинают выделять в окружающую среду молекулы, ускоряющие рост опухоли и прорастание кровеносных сосудов, которые будут обеспечивать ее питание, например фактор роста опухолей (TGFb) и фактор роста сосудов (VGF). Они перестают привлекать и инициировать другие клетки иммунной системы и начинают блокировать местный (противоопухолевый) иммунный ответ (рис. 2).
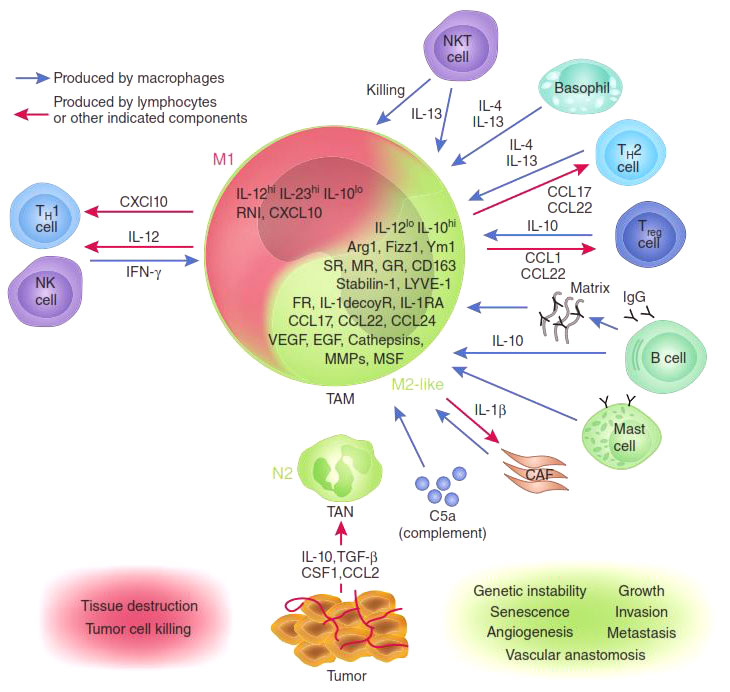
Рисунок 2. М1- и М2-макрофаги: их взаимодействие с опухолью и другими клетками иммунной системы.
Ключевую роль в этом перепрограммировании играют белки семейства NF-kB [7]. Эти белки являются транскрипционными факторами, контролирующими активность множества генов, необходимых для М1 активации макрофагов. Наиболее важные представители этого семейства — р65 и р50, вместе образующие гетеродимер р65/р50, который в макрофагах активирует множество генов, связанных с острым воспалительным ответом, таких как TNF, многие интерлейкины, хемокины и цитокины. Экспрессия этих генов привлекает все новые и новые иммунные клетки, «подсвечивая» для них район воспаления. В то же время другой гомодимер семейства NF-kB — р50/р50 — обладает противоположной активностью: связываясь с теми же самыми промоторами, он блокирует их экспрессию, снижая градус воспаления.
И та, и другая активность NF-kB транскрипционных факторов очень важна, но еще важнее равновесие между ними. Было показано, что опухоли целенаправленно выделяют вещества, которые нарушают синтез p65 белка в макрофагах и стимулируют накопление ингибиторного комплекса р50/р50 [7]. Таким способом (помимо еще ряда других) опухоль превращает агрессивных М1-макрофагов в невольных пособников своего собственного развития: М2-тип макрофагов, воспринимая опухоль как поврежденный участок ткани, включают программу восстановления, однако секретируемые ими факторы роста только добавляют ресурсы для роста опухоли. На этом цикл замыкается — растущая опухоль привлекает новые макрофаги, которые перепрограммируются и стимулируют ее рост вместо уничтожения.
Реактивация иммунного ответа — актуальное направление антираковой терапии
Таким образом, в ближайшем окружении опухолей присутствует сложная смесь молекул: как активирующих, так и ингибирующих иммунный ответ. Перспективы развития опухоли (а значит, перспективы выживания организма) зависят от баланса ингредиентов этого «коктейля». Если будут преобладать иммуноактиваторы — значит, опухоль не справилась с задачей и будет уничтожена или ее рост сильно затормозится. Если же преобладают иммуносупрессорные молекулы — это значит, что опухоль смогла подобрать ключ и начнет быстро прогрессировать. Понимая механизмы, которые позволяют опухолям подавлять наш иммунитет, мы сможем разработать контрмеры и сдвинуть баланс в сторону уничтожения опухолей [8].
Как показывают эксперименты, «перепрограммирование» макрофагов (и других клеток иммунной системы) обратимо. Поэтому одним из перспективных направлений онко-иммунологии на сегодняшний день является идея «реактивации» собственных клеток иммунной системы пациента с целью усиления эффективности других методов лечения. Для некоторых разновидностей опухолей (например, меланом) это позволяет добиться впечатляющих результатов. Другой пример, обнаруженный группой Меджитова [9], — обычный лактат, молекула, которая производится при недостатке кислорода в быстрорастущих опухолях за счет эффекта Варбурга [10]. Эта простая молекула стимулирует перепрограммирование макрофагов, заставляя их поддерживать рост опухоли. Лактат транспортируется внутрь макрофагов через мембранные каналы, и потенциальная терапия заключается в блокировке этих каналов.
Развитие методов антираковой терапии в настоящее время идет по нескольким направлениям сразу , и все они важны. Ведь научившись управлять иммунным ответом так же эффективно, как это делают злокачественные опухоли, мы сумеем окончательно «переиграть» эту болезнь, которая остается одной из главных причин смертности в России и в мире.
Биомаркеры [11] и биоинформатический анализ [12] — лишь некоторые из таких методов. — Ред.
Макрофаги
В буквальном переводе определение «макрофаг» имеет довольно зловещий и пугающий смысл: «макрос» на греческом обозначает «большой», а «фагос» – пожиратель. «Большой пожиратель»… Воображение рисует какого-нибудь монстра, но речь идет всего лишь о клетках крови. Впрочем, если судить о макрофагах на клеточном уровне, то свое название они вполне оправдывают.
Что такое клетки макрофаги и откуда они берутся?
 Все начинается в костном мозге, где из делящихся стволовых клеток образуется клетка под названием монобласт. В результате ее деления «рождается» промоноцит, его прямым потомком является моноцит – одна из разновидностей белых кровяных клеток. Моноцит переходит из костного мозга в клетки крови и там находится на протяжении 12-24 часов, после чего выходит из кровеносного русла и перемещается в ткани. В этот момент из моноцита и образуется макрофаг.
Все начинается в костном мозге, где из делящихся стволовых клеток образуется клетка под названием монобласт. В результате ее деления «рождается» промоноцит, его прямым потомком является моноцит – одна из разновидностей белых кровяных клеток. Моноцит переходит из костного мозга в клетки крови и там находится на протяжении 12-24 часов, после чего выходит из кровеносного русла и перемещается в ткани. В этот момент из моноцита и образуется макрофаг.
Клетки макрофаги в самом деле большие: хотя их размер составляет всего 15-80 мкм, и человеческому глазу они не видны, однако они гораздо больше их предшественников: максимальный размер моноцита составляет всего 20 мкм. У них неправильная, «плавающая», меняющаяся форма, а их мембрана может образовывать ложноножки. Внутри макрофага находится ядро, а еще в нем обнаруживаются «осколки» эритроцитов и других клеток, жировые капельки, фрагменты бактерий и прочий «мусор». Как все это туда попадает? Очень просто, ведь макрофаги – это клетки, которые осуществляют процесс фагоцитоза.
Функции макрофагов:
При попадании в тело чужеродного объекта, будь то микроб или инородное тело, иммунная система сразу «спускает на него собак»: его атакуют фагоциты. Эти клетки, среди которых и макрофаги, распознают, улавливают и пожирают чужаков, угрожающих благополучию внутренней среды организма.
Кроме того, макрофаги уничтожают погибшие клетки, которые завершили свое существование процессом апоптоза (запрограммированная, естественная, нормальная гибель клеток). Также функции макрофагов заключаются в обеспечении противоопухолевого иммунитета: зафиксировав появление в организме атипичных, раковых клеток, макрофаги нападают на них и поедают.
Виды макрофагов:
Макрофаги – тканевые фагоциты, и в разных типах тканей нередко  живут свои собственные виды этих клеток. Вот несколько примеров их разновидностей, в зависимости от локализации.
живут свои собственные виды этих клеток. Вот несколько примеров их разновидностей, в зависимости от локализации.
1. Альвеолярные макрофаги – находятся в стенках альвеол легких, очищают вдыхаемый воздух от различных загрязняющих и вредоносных частиц.
2. Купферовские клетки – в печени. Их назначение в основном заключается в уничтожении старых клеток крови.
3. Гистиоциты – распространенная разновидность макрофагов, которые встречаются во всех органах. Дело в том, что это – клетки соединительной ткани: волокон, образующих строму (каркас) большинства структур тела. Иногда гистиоциты превращаются в «настоящие» макрофаги.
4. Селезеночные макрофаги – располагаются в синусоидных сосудах этого органа. Как и у клеток Купфера, их задача заключается в том, чтобы вылавливать из крови и уничтожать отжившие клетки крови. Недаром селезенка называется кладбищем погибших эритроцитов!
5. Дендритные клетки – макрофаги, находящиеся под слизистыми оболочками и в коже, то есть фактически на границе с внешней средой.
6. Перитонеальные макрофаги – фагоциты, «живущие» в брюшине.
7. Где находятся макрофаги лимфатических узлов, понятно по названию. Это благодаря им лимфоузлы известны в качестве фильтров, очищающих лимфу.
Макрофаги и иммунная система:
Клетки макрофаги не просто бездумно уничтожают вредоносные объекты: расщепляя их на фрагменты, они осуществляют процесс презентации их антигенов. Антигены – это молекулы вредоносных частиц, которые говорят об их генетической чужеродности и вызывают соответствующую защитную реакцию со стороны иммунитета. Сами по себе они не представляют угрозы заражения или иного негативного воздействия, но это – метка чужака, поэтому организм реагирует на их присутствие защитной реакцией, как на полноценных агрессоров.
В процессе фагоцитоза макрофаги презентируют антигены убитых «врагов» – выставляют их на поверхность своих мембран. Также они образуют цитокины – информационные молекулы, которые несут в себе данные о побежденном агрессоре.
 С этим бесценным грузом макрофаги направляются к представителям другого звена иммунитета – лимфоцитам. Они передают им информацию и учат, как поступать, если в организм когда-нибудь еще раз проникнет носитель того же антигена. В результате иммунитет сохраняет по отношению к нему полную боеготовность.
С этим бесценным грузом макрофаги направляются к представителям другого звена иммунитета – лимфоцитам. Они передают им информацию и учат, как поступать, если в организм когда-нибудь еще раз проникнет носитель того же антигена. В результате иммунитет сохраняет по отношению к нему полную боеготовность.
К сожалению, иногда личного опыта наших макрофагов или других фагоцитов недостаточно для того, чтобы иммунная система работала должным образом и правильно реагировала на вредоносные объекты. Чтобы повысить ее эффективность и заодно улучшить состояние здоровья в целом, рекомендуется принимать препарат Трансфер Фактор. Он содержит цитокины, несущие в себе данные о всевозможных возбудителях заболеваний, токсинах и прочих вредоносных агентах. Препарат обучает иммунитет полноценной работе, что немедленно и благоприятным образом отражается на течении имеющихся заболеваний, состоянии обмена веществ и функции органов. Средство можно использовать в лечебных и профилактических целях.
Воспалительный процесс. Макрофаги
Основная роль в развитии и поддержании хронического воспаления принадлежит системе фагоцитирующих макрофагов (это понятие заменило широко применявшийся ранее, но по существу недостаточно обоснованный термин «ретикулоэндотелиальная система»). Основная клетка этой системы—макрофаг, развившийся из моноцита крови. Моноциты, происходящие из стволовой клетки костного мозга, поступают вначале в периферическую кровь, а из нее в ткани, где под влиянием различных местных стимулов превращаются в макрофаги.
Последние имеют чрезвычайно большое значение в осуществлении адаптивных реакций организма — иммунных, воспалительных и репаративных. Участию в подобных реакциях способствуют такие биологические свойства макрофагов, как способность мигрировать в очаги воспаления, возможность быстрого и стойкого увеличения продукции клеток костным мозгом, активный фагоцитоз чужеродного материала с быстрым расщеплением последнего, активация под действием чужеродных стимулов, секреция ряда биологически активных веществ, способность «обрабатывать» проникший в организм антиген с последующей индукцией иммунного процесса.
Принципиально важно также, что макрофаги являются долгоживущими клетками, способными длительно функционировать в воспаленных тканях. Существенно, что они способны пролиферировать в очагах воспаления; при этом возможна трансформация макрофагов в эпителиоидные и гигантские многоядерные клетки.
Не обладая иммунологической специфичностью (как Т- и В-лимфоциты), макрофаг действует в качестве неспецифической вспомогательной клетки, обладающей уникальной способностью не только захватывать антиген, но и обрабатывать его так, что последующее распознавание этого антигена лимфоцитами значительно облегчается. Этот этап особенно необходим для активации Т-лимфоцитов (для развития иммунных реакций замедленного типа и для продукции антител к тимусзависимым антигенам).
Кроме участия в иммунных реакциях за счет предварительной обработки антигена и его последующего «представления» лимфоцитам, макрофаги осуществляют защитные функции и более непосредственно, уничтожая некоторые микроорганизмы, грибы и клетки опухолей.
Таким образом, при ревматических заболеваниях в клеточных реакциях иммунного воспаления участвуют не только специфически иммунизированные лимфоциты, но и не имеющие иммунологической специфичности моноциты и макрофаги.
Эти клетки привлекаются моноцитарными хемотаксическими веществами, вырабатываемыми в очагах воспаления. К ним относятся С5а, частично денатурированные белки, калликреин, активатор плазминогена, основные белки из лизосом нейтрофилов Т-лимфоциты вырабатывают подобный фактор при контакте ее специфическим антигеном, В-лимфоциты — с иммунными комплексами.
Кроме того, лимфоциты продуцируют также факторы угнетающие миграцию макрофагов (т. е. фиксирующие их в очаге воспаления) и активирующие их функцию. В воспалительных очагах в отличие от нормальных условий наблюдаются митозы макрофагов и таким образом количество этих клеток нарастает также за счет местной пролиферации.
Значение макрофагов в поддержании воспалительного процесса определяется рассматриваемыми ниже противовоспалительными агентами, освобождаемыми из этих клеток.
2. Лизосомные ферменты (в частности, при фагоцитозе комплексов антиген — антитело, причем клетка при их выделении не разрушается).
3. Нейтральные протеазы (активатор плазминогена, коллагеназа, эластаза). В норме их количество ничтожно, но при чужеродной стимуляции (при фагоцитозе) продукция данных ферментов индуцируется и они выделяются в значительных количествах. Продукция нейтральных протеаз угнетается ингибиторами белкового синтеза, в том числе глюкокортикостероидами. Выработка активатора плазминогена и коллагеназы стимулируется также факторами, секретируемыми активированными лимфоцитами.
4. Фосфолипаза Аз, освобождающая из более сложных комплексов арахидоновую кислоту — основной предшественник простагландинов. Активность этого фермента тормозится глюкокортикостероидами.
5. Фактор, стимулирующий освобождение из костей как минеральных солей, так и органической основы костного матрикса. Этот фактор реализует свое влияние на костную ткань за счет прямого воздействия, не требуя присутствия остеокластов.
6. Ряд компонентов комплемента, которые активно синтезируются и выделяются макрофагами: С3, С4, С2 и, по-видимому, также С1 и фактор В, необходимый для альтернативного пути активирования комплемента. Синтез этих компонентов повышается при активировании макрофагов и тормозится ингибиторами белкового синтеза.
7. Интерлейкин-1, который является типичным представителем цитокинов — биологически активных веществ полипептидной природы, вырабатываемых клетками (прежде всего клетками иммунной системы). В зависимости от источников продукции этих веществ (лимфоциты или моноциты) нередко применяются термины «лимфокины» и «монокины». Название «интерлейкин» с соответствующим номером используется для обозначения конкретных цитокинов — особенно тех, которые опосредуют клеточное взаимодействие. Пока не вполне ясно, представляет ли интерлейкин-1, являющийся наиболее важным монокином, одно вещество или семейство полипептидов, обладающих очень близкими свойствами.
К этим свойствам относятся следующие:
- стимуляция В-клеток, ускоряющих их трансформацию в плазматические клетки;
- стимуляция активности фибробластов и синовиоцитов с повышенной выработкой ими простагландинов и коллагеназы;
- пирогенное влияние, реализующееся в развитии лихорадки;
- активирование синтеза в печени острофазовых белков, в частности сывороточного предшественника амилоида (этот эффект, возможно, является опосредованным — благодаря стимуляции выработки интерлейкина-6).
Среди системных эффектов интерлейкина-1, помимо лихорадки, могут быть отмечены также нейтрофилез и протеолиз скелетных мышц.
8. Интерлейкин-6, который также активирует В-клетки, стимулирует гепатоциты к выработке острофазовых белков и обладает свойствами b-интерферона.
9. Колониестимулирующие факторы, способствующие образованию в костном мозге гранулоцитов и моноцитов.
10. Фактор некроза опухолей (ФНО), который не только действительно способен вызывать некроз опухолей, но и играет заметную роль в развитии воспаления. Этот полипептид, состоящий из 157 аминокислот, в раннюю фазу воспалительной реакции способствует прилипанию нейтрофилов к эндотелию и способствует тем самым их проникновению в очаг воспаления. Он служит также мощным сигналом к выработке токсичных кислородных радикалов и является стимулятором В-клеток, фибробластов и эндотелия (2 последних типа клеток при этом вырабатывают колониестимулирующие факторы).
Клинически важно, что ФНО, так же как интерлейкин-1 и интерферон, подавляют активность липопротеинлипазы, которая обеспечивает отложение жира в организме. Именно поэтому при воспалительных заболеваниях часто отмечается выраженное похудание, не соответствующее калорийному питанию и сохранившемуся аппетиту. Отсюда второе название ФНО — кахектин.
Активация макрофагов, проявляющаяся увеличением их размера, большим содержанием ферментов, нарастанием способстности к фагоцитозу и уничтожению микробов и опухолевых клеток, может быть и неспецифичной: за счет стимуляции иными (не относящимися к имеющемуся патологическому процессу) микроорганизмами, минеральным маслом, лимфокинами, продуцируемыми Т-лимфоцитами, в меньшей степени — В-лимфоцитами.
Макрофаги активно участвуют в резорбции кости и хряща. При электронномикроскопическом исследовании на границе паннуса и суставного хряща обнаружены макрофаги, тесно связанные с частичками переваренных коллагеновьгх волокон. То же явление отмечено и при контакте макрофагов с резорбируемой костью.
Таким образом, макрофаги играют важную роль в развитии воспалительного процесса, его поддержании и хронизации и уже априорно могут рассматриваться как одна из главных «мишеней» антиревматической терапии.
Одураченные макрофаги, или Несколько слов о том, как злокачественные опухоли обманывают иммунитет
- 9216
- 7,9
- 5
- 4
Макрофаг атакует раковую клетку
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Иммунная система — это мощная многослойная защита нашего организма, которая потрясающе эффективна против вирусов, бактерий, грибов и других патогенов извне. Кроме того, иммунитет способен эффективно распознавать и уничтожать трансформированные собственные клетки, которые могут перерождаться в злокачественные опухоли. Однако сбои в работе иммунной системы (по генетическим либо другим причинам) приводят к тому, что однажды злокачественные клетки берут верх. Разросшаяся опухоль становится нечувствительной к атакам организма и не только успешно избегает уничтожения, но и активно «перепрограммирует» защитные клетки для обеспечения собственных нужд. Поняв механизмы, которые опухоль использует для подавления иммунного ответа, мы сможем разработать контрмеры и попытаться сдвинуть баланс в сторону активации собственных защитных сил организма для борьбы с болезнью.

Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».

Главный спонсор конкурса — дальновидная компания Генотек.
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Опухоль и иммунитет — драматический диалог в трех частях с прологом
Долгое время считалось, что причина низкой эффективности иммунного ответа при раке — то, что опухолевые клетки слишком похожи на нормальные, здоровые, чтобы иммунная система, настроенная на поиск «чужаков», могла их как следует распознавать. Этим как раз и объясняется тот факт, что иммунная система успешнее всего противостоит опухолям вирусной природы (их частота резко возрастает у людей, страдающих иммунодефицитом). Однако позже стало ясно, что это не единственная причина.
Если в этой статье речь идет про иммунные аспекты рака, то в работе «Страшней клешней на свете нет. » [1] можно прочесть про особенности ракового метаболизма. — Ред.
Оказалось, что взаимодействие раковых клеток с иммунной системой носит гораздо более разносторонний характер. Опухоль не просто «прячется» от атак, она умеет активно подавлять местный иммунный ответ и перепрограммировать иммунные клетки, заставляя их обслуживать собственные злокачественные нужды.
«Диалог» между переродившейся, вышедшей из-под контроля клеткой с ее потомством (то есть будущей опухолью) и организмом развивается в несколько стадий, и если вначале инициатива почти всецело находится на стороне защитных сил организма, то в конце (в случае развития болезни) — переходит на сторону опухоли. Несколько лет назад учеными-онкоиммунологами была сформулирована концепция «иммуноредактирования» (immunoediting), описывающая основные этапы этого процесса (рис. 1) [2].

Рисунок 1. Иммуноредактирование (immunoediting) в процессе развития злокачественной опухоли.
Первая стадия иммуноредактирования — процесс устранения (elimination). Под действием внешних канцерогенных факторов или в результате мутаций нормальная клетка «трансформируется» — приобретает способность неограниченно делиться и не отвечать на регуляторные сигналы организма. Но при этом она, как правило, начинает синтезировать на своей поверхности особые «опухолевые антигены» и «сигналы опасности». Эти сигналы привлекают клетки иммунной системы, прежде всего макрофаги, натуральные киллеры и Т-клетки. В большинстве случаев они успешно уничтожают «испортившиеся» клетки, прерывая развитие опухоли. Однако иногда среди таких «предраковых» клеток оказывается несколько таких, у которых иммунореактивность — способность вызывать иммунный ответ — по каким-то причинам оказывается ослабленной, они синтезируют меньше опухолевых антигенов, хуже распознаются иммунной системой и, пережив первую волну иммунного ответа, продолжают делиться.
В этом случае взаимодействие опухоли с организмом выходит на вторую стадию, стадию равновесия (equilibrium). Здесь иммунная система уже не может полностью уничтожить опухоль, но еще в состоянии эффективно ограничивать ее рост. В таком «равновесном» (и не обнаруживаемом обычными методами диагностики) состоянии микроопухоли могут существовать в организме годами. Однако такие затаившиеся опухоли не статичны — свойства составляющих их клеток постепенно меняются под действием мутаций и последующего отбора: преимущество среди делящихся опухолевых клеток получают такие, которые способны лучше противостоять иммунной системе, и в конце концов в опухоли появляются клетки-иммуносупрессоры. Они в состоянии не только пассивно избегать уничтожения, но и активно подавлять иммунный ответ. По сути, это эволюционный процесс, в котором организм невольно «выводит» именно тот вид рака, который его убьет.
Этот драматический момент знаменует собой переход опухоли к третьей стадии развития — избегания (escape), — на которой опухоль уже малочувствительна к активности клеток иммунной системы, более того — обращает их активность себе на пользу. Она принимается расти и метастазировать. Именно такая опухоль обычно диагностируется медиками и изучается учеными — две предыдущие стадии протекают скрыто, и наши представления о них основаны главным образом на интерпретации целого ряда косвенных данных.
Дуализм иммунного ответа и его значение в канцерогенезе
Существует множество научных статей, описывающих, как иммунная система борется с опухолевыми клетками, но не меньшее количество публикаций демонстрирует, что присутствие клеток иммунной системы в ближайшем опухолевом окружении является негативным фактором, коррелирующим с ускоренным ростом и метастазированием рака [2], [3]. В рамках концепции иммуноредактирования, описывающей, как изменяется характер иммунного ответа по мере развития опухоли, подобное двойственное поведение наших защитников получило, наконец, свое объяснение.
Переориентирование иммунной системы от борьбы с опухолью на ее защиту возможно благодаря пластичности клеток этой системы. Говоря об иммунном ответе, мы, как правило, используем «воинственные» метафоры — «борьба», «уничтожение», «подавление». Но мало уничтожить врага, будь то вирус, бактерия или другой паразит. Организм должен еще и исправить причиненные им повреждения. Регенерация поврежденных тканей и заживление ран тоже находятся под контролем клеток иммунной системы: она не только «воин», но еще и «целитель». Коварство рака заключается в том, что, будучи по сути «чужеродным агентом» в организме, он выделяет специальные вещества, которые подавляют активный иммунный ответ и побуждают лейкоциты воспринимать опухоль не как врага, требующего уничтожения, а как рану, требующую помощи, защиты и исцеления.
Мы рассмотрим некоторые механизмы того, как это происходит, на примере макрофагов. Похожие приемы опухоль использует и для того, чтобы обманывать другие клетки врожденного и приобретенного иммунитета.
Макрофаги — «клетки-воины» и «клетки-целители»
Макрофаги, пожалуй, самые знаменитые клетки врожденного иммунитета — именно с изучения их способностей к фагоцитозу Мечниковым и началась классическая клеточная иммунология. В организме млекопитающих макрофаги — боевой авангард: первыми обнаруживая врага, они не только пытаются уничтожить его собственными силами, но также привлекают к месту сражения другие клетки иммунной системы, активируя их. А после уничтожения чужеродных агентов принимаются активно участвовать в ликвидации причиненных повреждений, вырабатывая факторы, способствующие заживлению ран. Эту двойственную природу макрофагов опухоли используют себе на пользу.
В зависимости от преобладающей активности различают две группы макрофагов: М1 и М2. М1-макрофаги (их еще называют классически активированными макрофагами) — «воины» — отвечают за уничтожение чужеродных агентов (в том числе и опухолевых клеток), как напрямую, так и за счет привлечения и активации других клеток иммунной системы (например, Т-киллеров). М2 макрофаги — «целители» — ускоряют регенерацию тканей и обеспечивают заживление ран [4], [8].
Присутствие в опухоли большого количества М1-макрофагов тормозит ее рост [5], а в некоторых случаях может вызвать даже практически полную ремиссию (уничтожение). И наоборот: М2-макрофаги выделяют молекулы — факторы роста, которые дополнительно стимулируют деление опухолевых клеток, то есть благоприятствуют развитию злокачественного образования. Экспериментально было показано, что в опухолевом окружении обычно преобладают именно М2-клетки («целители»). Хуже того: под действием веществ, выделяемых опухолевыми клетками, активные М1-макрофаги «перепрограммируются» в М2-тип [6], перестают синтезировать антиопухолевые цитокины, такие как интерлейкин-12 (IL12) или фактор некроза опухолей (TNF) и начинают выделять в окружающую среду молекулы, ускоряющие рост опухоли и прорастание кровеносных сосудов, которые будут обеспечивать ее питание, например фактор роста опухолей (TGFb) и фактор роста сосудов (VGF). Они перестают привлекать и инициировать другие клетки иммунной системы и начинают блокировать местный (противоопухолевый) иммунный ответ (рис. 2).

Рисунок 2. М1- и М2-макрофаги: их взаимодействие с опухолью и другими клетками иммунной системы.
Ключевую роль в этом перепрограммировании играют белки семейства NF-kB [7]. Эти белки являются транскрипционными факторами, контролирующими активность множества генов, необходимых для М1 активации макрофагов. Наиболее важные представители этого семейства — р65 и р50, вместе образующие гетеродимер р65/р50, который в макрофагах активирует множество генов, связанных с острым воспалительным ответом, таких как TNF, многие интерлейкины, хемокины и цитокины. Экспрессия этих генов привлекает все новые и новые иммунные клетки, «подсвечивая» для них район воспаления. В то же время другой гомодимер семейства NF-kB — р50/р50 — обладает противоположной активностью: связываясь с теми же самыми промоторами, он блокирует их экспрессию, снижая градус воспаления.
И та, и другая активность NF-kB транскрипционных факторов очень важна, но еще важнее равновесие между ними. Было показано, что опухоли целенаправленно выделяют вещества, которые нарушают синтез p65 белка в макрофагах и стимулируют накопление ингибиторного комплекса р50/р50 [7]. Таким способом (помимо еще ряда других) опухоль превращает агрессивных М1-макрофагов в невольных пособников своего собственного развития: М2-тип макрофагов, воспринимая опухоль как поврежденный участок ткани, включают программу восстановления, однако секретируемые ими факторы роста только добавляют ресурсы для роста опухоли. На этом цикл замыкается — растущая опухоль привлекает новые макрофаги, которые перепрограммируются и стимулируют ее рост вместо уничтожения.
Реактивация иммунного ответа — актуальное направление антираковой терапии
Таким образом, в ближайшем окружении опухолей присутствует сложная смесь молекул: как активирующих, так и ингибирующих иммунный ответ. Перспективы развития опухоли (а значит, перспективы выживания организма) зависят от баланса ингредиентов этого «коктейля». Если будут преобладать иммуноактиваторы — значит, опухоль не справилась с задачей и будет уничтожена или ее рост сильно затормозится. Если же преобладают иммуносупрессорные молекулы — это значит, что опухоль смогла подобрать ключ и начнет быстро прогрессировать. Понимая механизмы, которые позволяют опухолям подавлять наш иммунитет, мы сможем разработать контрмеры и сдвинуть баланс в сторону уничтожения опухолей [8].
Как показывают эксперименты, «перепрограммирование» макрофагов (и других клеток иммунной системы) обратимо. Поэтому одним из перспективных направлений онко-иммунологии на сегодняшний день является идея «реактивации» собственных клеток иммунной системы пациента с целью усиления эффективности других методов лечения. Для некоторых разновидностей опухолей (например, меланом) это позволяет добиться впечатляющих результатов. Другой пример, обнаруженный группой Меджитова [9], — обычный лактат, молекула, которая производится при недостатке кислорода в быстрорастущих опухолях за счет эффекта Варбурга [10]. Эта простая молекула стимулирует перепрограммирование макрофагов, заставляя их поддерживать рост опухоли. Лактат транспортируется внутрь макрофагов через мембранные каналы, и потенциальная терапия заключается в блокировке этих каналов.
Развитие методов антираковой терапии в настоящее время идет по нескольким направлениям сразу , и все они важны. Ведь научившись управлять иммунным ответом так же эффективно, как это делают злокачественные опухоли, мы сумеем окончательно «переиграть» эту болезнь, которая остается одной из главных причин смертности в России и в мире.
Биомаркеры [11] и биоинформатический анализ [12] — лишь некоторые из таких методов. — Ред.



