Гемохроматоз 1 типа. Гемохроматоз-генетическое заболевание печени с серьезными осложнениями, лечение и прогноз. Причины наследственного гемохроматоза
Гемохроматоз печени: причины, симптомы, диагностика и лечение
В любом организме железо, как и многие другие микроэлементы, занимает значимое место. Но из-за избытка этого вещества в теле оно оказывает совершенно противоположное влияние на здоровье. Состояние, при котором количество железа в организме существенно превышает положенную норму, именуется гемохроматозом печени.
Описание патологии
Что собой представляет данное заболевание? Гемохроматозом печени называется генетическое рецессивное патологическое состояние, которое характеризуется чрезмерным всасыванием и отложением железа в печени и прочих органах. Это наследственное заболевание, которое может привести к развитию таких сопутствующих проблем, как цирроз, эндокринные сбои, гиперпигментация кожи. Несмотря на системную патологическую анатомию при гемохроматозе печени, больше всех от происходящих в организме изменений страдает именно этот орган.
Риски и возможные последствия
На фоне этого заболевания может развиться сахарный диабет, возникнуть сильные боли в суставах, состояние в целом значительно ухудшается. Избыток железа связан с чрезмерным всасыванием в пищеварительном тракте. Через какое-то время микроэлемент накапливается в других тканях, вызывая перегрузку. Признаками этого состояния первым делом выступают боли в суставах, общая слабость, ненормальное изменение оттенка кожи, различные нарушения сексуальных функций, сердечная недостаточность и травмирование самой печени. В некоторых случаях все это приводит к проявлению проблем со щитовидной железой и даже к раку. Раннее выявление причин и лечение гемохроматоза печени позволяет предотвратить развитие всяческих осложнений.
Кстати, название этой патологии не является единственным. Многие медики именуют это заболевание также пигментным циррозом, бронзовым диабетом и сидерофилией. В научной литературе зачастую гемохроматоз печени называют синдромом Труазье-Ано-Шоффара.
Распространенность
Чаще всего бронзовый диабет оказывается именно наследственной болезнью. Так что, если кто-либо из ваших родственников столкнулся с этим заболеванием или на одном из обследований в вашей семье был выявлен мутирующий ген, есть смысл в том, чтобы пройти проверку. У многих людей гемохроматоз можно с легкостью выявить при помощи простого анализа крови либо особого тестирования. К слову, мутирующий ген, являющийся причиной развития заболевания, рецессивный, а это означает, что для появления клинической патологии наличие его должно быть у обоих родителей.
Последняя статистическая информация свидетельствует о том, что в США приблизительно миллион людей предрасположены к этому заболеванию. Из них всего 150 тысяч человек имеют подтвержденный диагноз. В результате можно сказать, что риск развития гемохроматоза печени составляет лишь 0,33 %. К слову, сейчас приблизительно 10 % населения планеты имеют в своем ДНК патологические гены. Чаще всего заболевание встречается у представителей светлой расы. А более подвержены ему оказались представители сильного пола: у них заболевание развивается примерно в 10 раз чаще.
Причины гемохроматоза печени
Самой распространенной предпосылкой к заболеванию является именно наследственность. Патологический ген перестает контролировать обмен железа в организме и передается детям от родителей. Но помимо этого, следует сказать о еще нескольких причинах гемохроматоза печени, которые намного реже провоцирует развитие болезни.
- Инфекционные формы гепатита В и С хронического характера.
- Стеатогепатит неалкогольного вида, который приводит к возникновению жира в печени.
- Отказ от работы протоки поджелудочной железы.
- Всевозможные злокачественные образования, из которых чаще всего проявляется рак и лейкоз.
- Оперативное вмешательство при циррозе тоже способно привести к нарушениям нормального метаболизма. Чаще всего такие манипуляции производятся для возобновления кровообращения в главном сосуде печени при запущенной форме заболевания.
За счет особенностей патологии, чаще всего она встречается в семье. Но все же начинать диагностику гемохроматоза печени следует именно с определения причины, которая привела к зарождению болезни. Если же виной патологическому состоянию вовсе не мутирующий ген, лечение необходимо начать с ликвидации фактора, провоцирующего сбои в метаболизме железа.
Разновидности
Сегодня известно только два вида бронзового диабета, немного различающихся между собой:
- Первичный гемохроматоз печени, который представляет собой патологию, передающуюся по наследству в виде мутирующего гена. А за счет того, что именно он контролирует обменные процессы железа в организме, в дальнейшем проявляются всяческие нарушения.
- Неонатальный гемохроматоз печени – довольно-таки редкое заболевание, возникающее у младенцев практически сразу после рождения. Этой патологии свойственно быстрое прогрессирование. Возможные причины такого явления пока еще не выявлены.
Формы клинической картины
Существует также несколько различных стадий гемохроматоза печени.
- Первая – характеризуется допустимым количеством железа в организме, несмотря на нарушения обменных процессов.
- Вторая – переизбыток микроэлемента в таком случае пока еще не приводит к отчетливым проявлениям симптоматики заболевания.
- Третья – характеризуется четкой клинической картиной, свойственной этому заболеванию.
Какой-либо прогноз без дальнейшего лечения – одна из самых неблагоприятных ситуаций для любого пациента. В таком случае больной, скорее всего, вряд ли проживет больше 5 лет с момента постановки диагноза. Обычно причиной гибели становится острая недостаточность самой печени, почек или даже сердца.
При отсутствии должной терапии у пациента вполне вероятно даже возникновение кровотечения в пищеварительном тракте. Пожилые люди, столкнувшиеся с таким диагнозом, в большей степени подвержены образованию рака печени.
Симптоматика
Всевозможные признаки гемохроматоза печени в большей или меньшей степени выражены, в зависимости от стадии болезни. Чем больше времени проходит с момента заболевания, тем более выразительной становится клиническая картина. Основные симптомы гемохроматоза печени, как правило, более заметны именно на третьей стадии:
- Ощутимая слабость и заметная утомляемость.
- Постоянное низкое артериальное давление.
- Быстрая потеря массы тела.
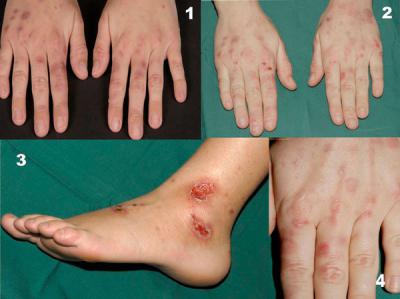
- Гиперпигментация, которая заключается в сильном потемнении кожи, слизистых и глазных склер. Этот признак проявляется в 70 % всех случаев заболевания.
- Развитие сахарного диабета.
- Отечность и боли в суставах, из-за чего движения постепенно становятся скованными или даже ограниченными.
- Полное отсутствие либо медленное понижение сексуальных функций.
- Развитие различных болезней: в особенности часто почечная, сердечная, печеночная недостаточность и цирроз.
Ввиду того что гемохроматоз может провоцировать большое количество других патологий, можно говорить и о вероятности проявления вторичных признаков болезни.
Постановка диагноза
Для того чтобы убедиться в наличии у пациента именно этого заболевания, необходимо произвести тщательную всестороннюю диагностику. Установить такой диагноз можно на основании определенных обследований:
- Диагностика гемохроматоза печени должна начинаться со сбора и анализов анамнеза больного. Наиболее важен период возникновения первой симптоматики.
- Необходим также сбор и анализ анамнеза ближайших родственников для выявления вероятности развития наследственного гемохроматоза печени.
- Осуществление генетического обследования ради обнаружения мутирующего гена.
- Исследование параметров метаболизма в организме, которое дает общие сведения о количестве железа.
- Пункционная биопсия печени для обнаружения избытка микроэлементов.
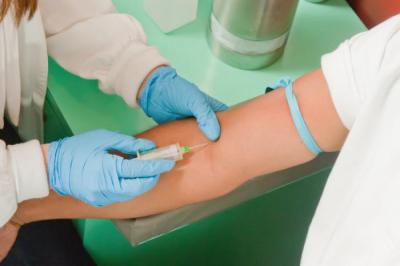
Зачастую пациенту также требуется консультация других специалистов, поскольку бронзовый диабет провоцирует развитие множества сопутствующих заболеваний. Первоначально человек, заподозривший возникновение этой болезни, должен прибегнуть к услугам гепатолога либо гастроэнтеролога – эти врачи решат необходимость дальнейшего обследования и консультаций с другими медиками.
Лечение гемохроматоза печени
Ввиду того что эта патология является генетической, по-настоящему эффективных способов терапии не существует. Лечение нацелено на защиту внутренних систем от травмирования, а также очищение всего организма от пагубных токсинов. На качество и длительность жизни пациента с таким диагнозом существенно влияет питание больного и его привычки.
Методы терапии
Терапия при этом заболевании направлена прежде всего на прекращение процесса накопления железа в организме, а также вывод его. Кроме того, очень важно поддерживать полноценную функциональность всех систем, не допуская развития осложнений.
- Соблюдение специальной диеты, которая направлена на уменьшение количества пищи с высоким содержанием железа и белков.
- Прием лекарственных средств, необходимых для принудительного связывания избыточных микроэлементов для последующего их вывода из организма.
- Кровопускание, при котором выпускается примерно 0,5 литра жидкости из поверхностных сосудов для улучшения общего состояния организма. Благодаря этой процедуре существенно снижаются проявления пигментации.
- Симптоматическое лечение, необходимое для предотвращения сильных последствий патологии и поддержания тела в том состоянии, которое было ему свойственно на момент постановки диагноза.
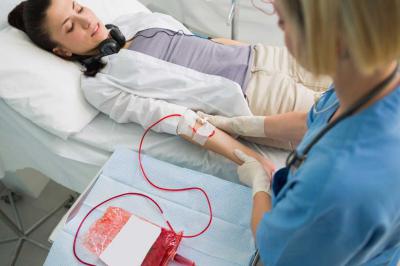
Лечение проводится исключительно в стационаре, в том числе и многие процедуры, например кровопускание. А вот прием назначенных медикаментов и соблюдение определенного рациона пациент контролирует самостоятельно.
Диета
Соблюдение специального меню при лечении гемохроматоза печени – обязательное условие оздоровления. Эта методика направлена в первую очередь на сокращение количества в рационе продуктов, содержащих железо. Пациенты с подтвержденным диагнозом должны придерживаться нескольких правил, касающихся питания:
- В первую очередь больному следует отказаться от употребления всевозможных спиртных напитков. Ведь алкоголь способствует тому, что пищеварительный тракт всасывает большее количество железа. К тому же спирт является токсичным и отправляет весь организм.
- Необходимо отказаться от сигарет, а также избегать пассивного курения, поскольку из-за этого нарушается метаболизм, а это усложняет течение терапии.
- Следует также сократить количество в меню мучных изделий. Очень важно первым делом отказаться от черных разновидностей хлеба.
- Необходимо перестать употреблять деликатесы, сделанные из животных почек и печени.
- Нужно сократить в своем рационе продукты, содержащие большое количество витамина С. Этот элемент тоже способствует повышенному всасыванию железа.
- Очень важно исключить из меню морепродукты, из которых самыми опасными для пациентов с диагнозом “гемохроматоз” считаются омары, водоросли, креветки и крабы.
- А вот употребление кофе и крепкого чая черных сортов нужно, напротив, активизировать. Ведь эти напитки включают в свой состав танины, которые удачно замедляют усваивание железа организмом.

Вредные и полезные продукты
В случае установления гемохроматоза печени пациенту необходимо в обязательном порядке пересмотреть собственный рацион и скорректировать способ своего питания.
При этом следует иметь в виду, что больше всего железа содержится в таких продуктах:
- яичный желток;
- куриные сердца;
- крольчатина;
- говяжий и свиной язык;
- перепелиные яйца;
- патока;
- тыквенные семечки;
- черная икра;
- красное мясо;
- белые грибы;
- пивные дрожжи;
- яблоки;
- кунжут;
- халва;
- черная смородина;
- бананы;
- всевозможные бобовые;
- гречневая крупа.

Таким людям следует обратить особое внимание:
- на картофель;
- свеклу;
- капусту;
- морковку;
- огурцы;
- тыкву;
- репчатый и зеленый лук;
- томаты;
- клюкву;
- сельдерей;
- мед;
- вишню;
- виноград;
- разнообразные кисломолочные продукты;
- цитрусовые фрукты.
Заключение
Гемохроматоз печени нуждается в незамедлительном всестороннем лечении и правильном диагностировании. Только так пациент может значительно увеличить срок собственной жизни, а также предотвратить развитие и усугубление всевозможных проблем. А возникают они обычно при отсутствии дальнейшей комплексной терапии.
Наследственный гемохроматоз – симптомы, диагностика и лечение

Наследственный гемохроматоз – это генетическое заболевание, при котором в организме человека накапливается железо. Это довольно частое наследственное заболевание среди европейцев. По данным американских экспертов, наследственным гемохроматозом страдает 1 из 240-300 жителей региона.
Больные гемохроматозом могут не иметь никаких жалоб, а продолжительность их жизни может не отличаться от таковой у здоровых людей. У других же больных развиваются тяжелые симптомы перегрузки железом, включая сексуальную дисфункцию, сердечную недостаточность, боли в суставах, цирроз печени, сахарный диабет, общую слабость и потемнение кожи.
Нормальное содержание железа в организме должно составлять от 3 до 4 граммов. Общее количество железа в теле регулируется особыми механизмами всасывания. Наш организм ежедневно теряет около 1 миллиграмма железа с потом и отмершими клетками кожи и кишечника. Женщины теряют в среднем на 1 миллиграмм больше за счет менструаций. Кишечник здорового взрослого человека ежедневно компенсирует эту потерю, усваивая железо из пищи. Когда человек теряет много железа с кровью, усвоение его в кишечнике усиливается. В норме поддерживается баланс, поэтому больших отложений железа в организме не бывает.
У людей с наследственным гемохроматозом ежедневная абсорбция железа из кишечника больше той нормы, которая нужна организму. А так как человеческое тело не может быстро выделять железо, то это приводит к накоплению и отложению железа в органах и тканях. При наследственном гемохроматозе к 40-50 годам в организме больного накапливается до 20 граммов железа – в пять раз больше нормы!
Избыток железа откладывается в суставах, печени, яичках, сердце, что приводит к повреждению этих органов и вызывает симптомы гемохроматоза. У женщин железо может накапливаться медленнее, потому что они испытывают потери железа во время месячных, беременности и лактации. Таким образом, у женщин симптомы поражения органов развиваются в среднем на 10 лет позднее, чем у мужчин.
Наследственная природа гемохроматоза
Наследственный гемохроматоз – аутосомно-рецессивное заболевание. Это означает, что у ребенка есть вероятность развития гемохроматоза, только если у обоих его родителей был ген этой болезни. В отличие от этого типа наследования, при аутосомно-доминантых болезнях ребенок может унаследовать болезнь даже от одного из родителей.
Человеческое тело состоит из триллионов клеток. Внутри каждой клетки имеется ядро, содержащее наш генетический материал – хромосомы. У каждого человека есть 23 пары хромосом – всего 46 хромосом. Этот материал мы наследуем от обоих наших родителей. Хромосомы содержат ДНК, которые кодируют все наши обменные процессы, внешний облик, рост, цвет глаз и волос, интеллект и другие особенности. Дефекты в ДНК, называемые мутациями, могут приводить к болезни, причем они «запоминаются» на уровне молекул и передаются новым поколениям – в этом и заключается природа генетических болезней.
Существует два основных типа мутаций, связанных с наследственным гемохроматозом – C282Y и H63D. Числа 282 и 63 обозначают расположение дефектов в HFE-гене, которой находится в 6-й хромосоме.
Люди, которые наследуют две мутации C282Y от каждого из родителей, имеют очень высокий шанс развития гемохроматоза. По сути, такие люди составляют 95% всех больных наследственным гемохроматозом. Пациенты, которые унаследовали одну мутацию C282Y от одного родителя и одну мутацию H63D от другого родителя, составляют еще 3% больных гемохроматозом.
Симптомы наследственного гемохроматоза
На ранней стадии болезни у больных нет никаких симптомов, которые позволяют заподозрить гемохроматоз и пройти анализ ДНК. Позднее можно выявить высокий уровень сывороточного железа крови, который обнаруживается случайно, при анализах по другому поводу.
У мужчин симптомы гемохроматоза могут не проявляться до 40-50 лет. У женщин первые симптомы могут проявляться на 10, а то и на 15-20 лет позднее, чем у мужчин.
Отложения железа в коже вызывают потемнение кожных покровов, на которое иногда просто не обращают внимания. Отложения железа в гипофизе и яичках вызывают «усыхание» яичек и импотенцию. Железо в поджелудочной железе вызывает снижение выработки инсулина и сахарный диабет. Отложения в сердечной мышце приводят к сердечной недостаточности и аритмии. Поражение печени вызывает рубцовые изменения (цирроз) и повышенный риск развития рака печени. Железо в суставах вызывает болезненность при движениях и ограничение подвижности.
Диагностика гемохроматоза
Как уже говорилось, у большинства больных подозрительное повышение уровня железа в крови обнаруживается случайно. У некоторых больных сначала выявляется повышенный уровень ферментов печени, что в дальнейшем приводит к диагнозу гемохроматоз. Гораздо проще, когда больные знают о гемохроматозе у родителей, поэтому приходят на обследование по этому поводу сами.
Есть несколько анализов крови, которые отражают содержание железа в организме: уровень ферритина, содержание сывороточного железа, максимальная железосвязывающая способность (TIBC) и насыщение трансферрина.
Ферритин – это протеин крови, уровень которого коррелирует с количеством железа, запасенного в организме. Уровень ферритина обычно низкий у пациентов с железодефицитной анемией (ЖДА), но он повышен у больных гемохроматозом. Уровень ферритина также повышается при некоторых инфекциях (вирусный гепатит) и других воспалительных процессах, поэтому одного этого показателя мало для точного диагноза.
Анализы на содержание сывороточного железа и насыщение трансферрина делают одновременно. Сывороточное железо отражает количество железа в жидкой части (сыворотке) крови. Связывающая способность показывает общее количество железа, которое может связать сывороточный трансферрин – белок, переносящий молекулы железа в разные части тела.
Насыщение трансферрина – это число, получаемое при делении содержания сывороточного железа на максимальную железосвязывающую способность крови. Этот показатель говорит о том, какой процент трансферрина задействован в транспорте железа. У здорового человека насыщение трансферрина находится в пределах 20-50%. У пациентов с ЖДА этот показатель аномально низкий, а при наследственном гемохроматозе – очень высокий (то есть, большая часть трансферрина «занята» транспортировкой запасов железа).
Уровень сывороточного железа может повышаться в течения дня, обычно после еды. Поэтому анализы крови должны проводиться утром, на голодный желудок.
Наиболее точный тест на гемохроматоз – это измерение содержания железа в тканях печени. Для этого теста необходимо провести биопсию – взять небольшой фрагмент печени больного. Обычно эту процедуру делают при помощи специальной длинной иглы. Больному делают анестезию, а затем вводят иглу через кожу в печень, контролируя эту процедуру при помощи аппарата УЗИ. Ткань, полученную при биопсии, изучают в лаборатории на признаки воспаления печени, цирроза (необратимого рубцевания), и проверяют содержание железа.
Биопсия печени при гемохроматозе имеет также прогностическую ценность, поскольку определяет степень необратимого рубцевания печени. Больные с гемохроматозом при сравнительно хороших результатах биопсии имеют нормальную продолжительность жизни (при условии адекватного лечения). Пациенты, у которых гемохроматоз уже вызвал цирроз печени, живут намного меньше.
Более того, у больных с циррозом резко возрастает риск рака печени (гепатоцеллюлярная карцинома), который способен убить человека гораздо раньше, чем это сделал бы цирроз. Когда печень уже поражена, этот риск остается высоким, даже если гемохроматоз активно лечить.
Ген, отвечающий за наследственный гемохроматоз, был открыт еще в 1996 году. Ген этот получил аббревиатуру HFE. Наследственный гемохроматоз у большинства больных ассоциируется с мутациями C282Y и H63D в этом гене.
Чаще всего (95%) больные гемохроматозом имеют две мутации C282Y, унаследованные от обоих родителей. В то же время, не все люди с такой генетикой страдают накоплением железа в организме. Исследования показали, что только 50% людей с двойной мутацией C282Y болеют гемохроматозом и его осложнениями. То есть, положительный генетический тест – это еще не приговор.
Комбинированная мутация C282Y/H63D возникает у детей, унаследовавших мутацию C282Y от одного, а H63D от другого родителя. В большинстве случаев такие люди имеют нормальный уровень железа, но у некоторых возникает перегрузка железом легкой или средней тяжести.
Если ребенок унаследовал только один дефект C282Y от одного из родителей, а второй ген HFE нормальный, то у него не возникнут симптомы перегрузки железом. Но такой человек становится носителем болезни. Если оба родителя имеют такой дефект, то у каждого их ребенка 25% будет вероятность развития гемохроматоза.
Рекомендуемый в США алгоритм диагностики наследственного гемохроматоза:
1. Взрослые с подозрением на наследственный гемохроматоз (к примеру, близкие родственники больных) должны сдать анализы крови на сывороточное железо, ферритин, TIBC и насыщение трансферрина.
2. Пациенты с повышенным уровнем сывороточного железа, ферритина и насыщением трансферрина выше 45% должны пройти генетический анализ.
3. Пациенты с двойной мутацией C282Y и насыщением трансферрина выше 45% считаются больными гемохроматозом. Они должны проходить лечение (терапевтическая флеботомия).
Показания для биопсии печени.
Не все пациенты с гемохроматозом нуждаются в проведении биопсии печени. Цель печеночной биопсии – выявить больных с циррозом, а также исключить другие заболевания печени (пациенты с циррозом часто страдают раком печени).
У молодых людей до 40 лет, носителей двух мутаций C282Y, с нормальными показателями ферментов печени и уровнем сывороточного ферритина менее 1000 нг/мл риск цирроза очень мал. Ввиду этого, американские эксперты рекомендуют лечить их терапевтической флеботомией без проведения биопсии печени. У таких больных отличный прогноз при адекватном лечении.
Пациенты старше 40 лет с повышенным уровнем печеночных ферментов и сывороточным ферритином более 1000 нг/мл имеют серьезный риск цирроза печени. Врач может порекомендовать биопсию печени, если эта процедура безопасна для больного. Прогноз зависит от результатов биопсии.
Лечение наследственного гемохроматоза
Наиболее эффективным лечением гемохроматоза является флеботомия (кровопускание) – регулярное удаление части крови из вен на руках. Для лечения обычно достаточно брать одну единицу крови, или 450-500 мл, каждые 7-14 дней (в одной единице крови содержится около 250 мг железа).
При этом каждые 2-3 месяца рекомендуется проверять уровень сывороточного ферритина и насыщение трансферрина. Как только уровень ферритина упадет ниже 50 нг/мл при насыщении трансферрина ниже 50%, частоту кровопусканий уменьшают до 1 процедуры в 2-3 месяца.
Преимущества терапевтической флеботомии при гемохроматозе:
1. Предотвращение цирроза и рака печени, если лечение начато рано.
2. Улучшение функций печени, частично и у больных с циррозом.
3. Преодоление таких симптомов, как слабость, утомляемость, боли в суставах.
4. Улучшение работы сердца у больных с незначительным поражением миокарда.
Если гемохроматоз вовремя диагностировать и интенсивно лечить, то повреждений печени, сердца, поджелудочной, яичек и суставов можно полностью избежать, а пациенты остаются практически здоровыми людьми. У больных с уже возникшим циррозом можно улучшить функции органов, но рубцевание печени необратимо, и риск рака останется высоким.
Диетические рекомендации для больных с наследственным гемохроматозом:
1. Нормальная, сбалансированная диета разрешается всем больным, которым делают терапевтическую флеботомию. Избегать продуктов, содержащих железо, не обязательно.
2. Следует избегать спиртных напитков, потому что регулярное употребление алкоголя негативно сказывается на печени, повышает риск цирроза и гепатоцеллюлярной карциномы.
3. Прием больших доз витамина С (аскорбиновой кислоты) у пациентов с перегрузкой железом может привести к фатальной аритмии. Нужно избегать диетических добавок с витамином С, пока болезнь не взята под контроль.
4. Нельзя употреблять сырую морскую пищу, поскольку можно приобрести опасные инфекции, которые процветают в богатой железом среде.
Ранняя диагностика рака печени у больных гемохроматозом.
Рак печени (гепатома или гепатоцеллюлярная карцинома) возникает преимущественно у больных с циррозом печени. Таким образом, пациенты с гемохроматозом и циррозом должны проходить регулярные ультразвуковые исследования (УЗИ) и сдавать анализы крови на альфа-фетопротеин (белок, вырабатываемый опухолью). Эти тесты должны проводиться каждые полгода.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Гемохроматоз ( Бронзовый диабет , Пигментный цирроз )
Гемохроматоз – наследственное полисистемное заболевание, сопровождающееся активным всасыванием железа в ЖКТ и его последующей аккумуляцией во внутренних органах (сердце, поджелудочной железе, печени, суставах, гипофизе). Клиника гемохроматоза характеризуется бронзовой пигментацией кожи и слизистых оболочек, развитием цирроза печени, сахарного диабета, кардиомиопатии, артралгий, нарушения половой функции и т. д. Диагноз гемохроматоза подтверждается при определении повышенной экскреции железа с мочой, высокого содержания железа в сыворотке крови и биоптатах печени, а также с помощью рентгенографии, УЗИ, МРТ внутренних органов. Лечение пациентов с гемохроматозом основано на соблюдении диеты, введении дефероксамина, проведении кровопусканий, плазмафереза, гемосорбции, симптоматической терапии. При необходимости решается вопрос о трансплантации печени и артропластике.
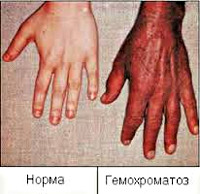
Общие сведения
Гемохроматоз (бронзовый диабет, пигментный цирроз) – генетически обусловленное нарушение метаболизма железа, приводящее к отложению железосодержащих пигментов в тканях и органах и развитию полиорганной недостаточности. Заболевание, сопровождающееся характерным симптомокомплексом (пигментация кожи, цирроз печени и сахарный диабет) было описано в 1871 г., а в 1889 г. получило название гемохроматоза за характерную окраску кожи и внутренних органов. Частота наследственного гемохроматоза в популяции составляет 1,5-3 случая на 1000 населения. Мужчины болеют гемохроматозом в 2-3 раза чаще, чем женщины. Средний возраст развития патологии – 40-60 лет. Ввиду полисистемности поражения, изучением гемохроматоза занимаются различные клинические дисциплины: гастроэнтерология, кардиология, эндокринология, ревматология и др.
В этиологическом аспекте выделяют первичный (наследственный) и вторичный гемохроматоз. Первичный гемохроматоз связан с дефектом ферментных систем, приводящим к отложению железа во внутренних органах. В зависимости от генного дефекта и клинической картины выделяют 4 формы наследственного гемохроматоза:
- I – классический аутосомно-рецессивный, HFE-ассоциированный тип (более 95% случаев)
- II – ювенильный тип
- III – наследственный HFE-неассоциированный тип (мутации в трансферриновом рецепторе 2-го типа)
- IV– аутосомно-доминантный тип.
Вторичный гемохроматоз (генерализованный гемосидероз) развивается в результате приобретенной недостаточности ферментных систем, участвующих в обмене железа, и часто ассоциирован с другими заболеваниями, в связи с чем выделяют следующие его варианты: посттрансфузионный, алиментарный, метаболический, смешанный и неонатальный.
В клиническом течении гемохроматоз проходит 3 стадии: I – без перегрузки железом; II – с перегрузкой железом, но без клинических симптомов; III – с развитием клинических проявлений.

Причины гемохроматоза
Первичный наследственный гемохроматоз является заболеванием с аутосомно-рецессивным типом передачи. В его основе лежат мутации гена HFE, расположенного на коротком плече 6-ой хромосомы. Дефект HFE-гена приводит к нарушению трансферрин-опосредованного захвата железа клетками 12-перстной кишки, следствием чего является формирование ложного сигнала о дефиците железа в организме. В свою очередь, это способствует повышенному синтезу железосвязывающего белка DCT-1 энтероцитами и усиленной абсорбции железа в кишечнике (при нормальном поступлении микроэлемента с пищей). В дальнейшем происходит чрезмерное отложение железосодержащего пигмента гемосидерина во многих внутренних органах, гибель их функционально активных элементов с развитием склеротических процессов. При гемохроматозе ежегодно в организме человека накапливается 0,5-1,0 г железа, а проявления заболевания манифестируют при достижении общего уровня железа 20 г (иногда 40-50 г и больше).
Вторичный гемохроматоз развивается в результате избыточного экзогенного поступления железа в организм. Такое состояние может возникать при частых повторных гемотрансфузиях, неконтролируемом приеме препаратов железа, талассемии, некоторых видах анемии, кожной порфирии, алкогольном циррозе печени, хронических вирусных гепатитах В и С, злокачественных новообразованиях, следовании низкобелковой диете.
Симптомы гемохроматоза
Клиническая манифестация наследственного гемохроматоза приходится на зрелый возраст, когда содержание общего железа в организме достигает критических значений (20-40 г). В зависимости от преобладающих синдромов различают гепатопатическую (гемохроматоз печени), кардиопатическую (гемохроматоз сердца), эндокринологическую формы заболевания.
Заболевание развивается постепенно; в начальной стадии преобладают неспецифичные жалобы на повышенную утомляемость, слабость, похудание, снижение либидо. В этой стадии больных могут беспокоить боли в правом подреберье, сухость кожи, артралгии, обусловленные хондрокальцинозом крупных суставов. В развернутой стадии гемохроматоза формируется классический симптомокомплекс, представленный пигментацией кожи (бронзовая кожа), циррозом печени, сахарным диабетом, кардиомиопатией, гипогонадизмом.
Обычно наиболее ранним признаком гемохроматоза выступает появление специфической окраски кожи и слизистых оболочек, выраженной, главным образом, на лице, шее, верхних конечностях, в области подмышек и наружных гениталий, рубцов кожи. Интенсивность пигментации зависит от давности течения заболевания и варьирует от бледно-серого (дымчатого) до бронзово-коричневого цвета. Характерно выпадение волос на голове и туловище, вогнутая (ложкообразная) деформация ногтей. Отмечаются артропатии пястно-фаланговых, иногда коленных, тазобедренных и локтевых суставов с последующим развитием их тугоподвижности.
Практически у всех больных выявляется увеличение печени, спленомегалия, цирроз печени. Нарушение функции поджелудочной железы выражается в развитии инсулинзависимого сахарного диабета. В результате поражения гипофиза при гемохроматозе страдает половая функция: у мужчин развивается атрофия яичек, импотенция, гинекомастия; у женщин – аменорея и бесплодие. Гемохроматоз сердца характеризуется кардиомиопатией и ее осложнениями – аритмией, хронической сердечной недостаточностью, инфарктом миокарда.
В терминальной стадии гемохроматоза развивается портальная гипертензия, асцит, кахексия. Гибель пациентов, как правило, наступает вследствие кровотечения из варикозно расширенных вен пищевода, печеночной недостаточности, острой сердечной недостаточности, диабетической комы, асептического перитонита, сепсиса. Гемохроматоз значительно увеличивает риск развития рака печени (гепатоцеллюлярной карциномы).
Диагностика гемохроматоза
В зависимости от преобладающих симптомов пациенты с гемохроматозом могут обращаться за помощью к различным специалистам: гастроэнтерологу, кардиологу, эндокринологу, гинекологу, урологу, ревматологу, дерматологу. Между тем, диагностика заболевания едина при различных клинических вариантах гемохроматоза. После оценки клинических признаков больным назначается комплекс лабораторно-инструментальных исследований, позволяющих убедиться в правомерности диагноза.
Лабораторными критериями гемохроматоза служат значительное повышение уровня железа, ферритина и трансферрина в сыворотке крови, увеличение выведения железа с мочой, снижение общей железосвязывающей способности сыворотки крови. Диагноз подтверждается с помощью пункционной биопсии печени или кожи, в образцах которых обнаруживается отложение гемосидерина. Наследственная природа гемохроматоза устанавливается в результате проведения молекулярно-генетической диагностики.
С целью оценки тяжести поражения внутренних органов и прогноза заболевания исследуются печеночные пробы, уровень глюкозы крови и мочи, гликозилированный гемоглобин и др. Лабораторная диагностика гемохроматоза дополняется инструментальными исследованиями: рентгенографией суставов, ЭКГ, ЭхоКГ, УЗИ органов брюшной полости, МРТ печени и др.
Лечение гемохроматоза
Основной целью проводимой терапии служит удаление избытка железа из организма и недопущение развития осложнений. Больным с гемохроматозом назначается диета, предусматривающая ограничение пищевых продуктов с высоким содержанием железа (яблок, мяса, печени, гречневой крупы, шпината и пр.), легкоусвояемых углеводов. Запрещается прием мультивитаминов, аскорбиновой кислоты, БАДов, содержащих железо, алкоголя. Для выведения избытков железа из организма прибегают к кровопусканиям под контролем показателей гемоглобина, гематокрита крови, ферритина. С этой же целью могут использоваться экстракорпоральные методы гемокоррекции – плазмаферез, гемосорбция, цитаферез.
Патогенетическая медикаментозная терапия гемохроматоза основана на внутримышечном или внутривенном введении пациенту дефероксамина, связывающего ионы Fe3+. Одновременно проводится симптоматическое лечение цирроза печени, сердечной недостаточности, сахарного диабета, гипогонадизма. При выраженной артропатии определяются показания к проведению артропластики (эндопротезирования пораженных суставов). У пациентов с циррозом решается вопрос о проведении трансплантации печени.
Прогноз и профилактика гемохроматоза
Несмотря на прогрессирующее течение заболевания, своевременная терапия позволяет продлить жизнь пациентов с гемохроматозом на несколько десятилетий. При отсутствии лечения средняя продолжительность жизни больных после диагностики патологии не превышает 4-5 лет. Наличие осложнений гемохроматоза (главным образом, цирроза печени и застойной сердечной недостаточности) является прогностически неблагоприятным признаком.
При наследственном гемохроматозе профилактика сводится к проведению семейного скрининга, раннему выявлению и началу лечения заболевания. Избежать развития вторичного гемохроматоза позволяет рациональное питание, контроль за назначением и приемом препаратов железа, проведением переливаний крови, отказ от приема алкоголя, наблюдение за больными с заболеваниями печени и системы крови.
Гемохроматоз 1 типа. Гемохроматоз-генетическое заболевание печени с серьезными осложнениями, лечение и прогноз. Причины наследственного гемохроматоза
Этиология и встречаемость наследственного гемохроматоза. Наследственный гемохроматоз (MIM №235200) — болезнь накопления железа, встречающаяся у некоторых лиц с гомозиготными или компаундными гетерозиготными мутациями в гене HFE. Большинство пациентов (90-95%) с наследственным гемохроматозом гомозиготны по мутации Cys282Tyr; оставшиеся 5-10% больных — компаундные гетерозиготы по Cys282Tyr и другой мутации, His63Asp. Гомозиготность по мутации His63Asp не ведет к клиническому гемохроматозу, если нет дополнительных причин перегрузки железом.
Частота носительства у белой популяции Северной Америки составляет приблизительно 11% по Cys282Tyr и приблизительно 27% для His63Asp, это означает, что примерно 1 из 330 человек — гомозигота по мутации Cys282Tyr и еще 1 из 135 — ком-паундная гетерозигота по патогенным мутациям в гене HFE. Частота этих мутаций гораздо более низкая среди монголоидов, негроидов и американских индейцев.
Клиническую пенетрантность наследственного гемохроматоза определить трудно; оценки изменяются от 10 до 70%, в зависимости от того, определяется ли наследственный гемохроматоз как органная патология, вызванная накоплением железа, или биохимическим подтверждением повышения насыщения ферритина и уровня трансферрина.
В семейных исследованиях, например, от 75 до 90% гомозиготных родственников больных оказались бессимптомными. Популяционные исследования оценивают пенетрантность наследственного гемохроматоза на основе биохимического подтверждения от 25 до 50%, но пенетрантность может быть более высокой, если выполняется биопсия печени для выявления скрытого цирроза.
Независимо от того, какова пенетрантность, ясно, что мужчины поражаются более часто, чем женщины, и сложные гетерозиготы Cys282Tyr/His63Asp имеют значительно более низкий риск наследственного гемохроматоза, чем гомозиготы Cys282Tyr. Хотя точная величина пенетрантности у гомозигот Cys282Tyr требует окончательного определения, ясно, что пенетрантность неполная.
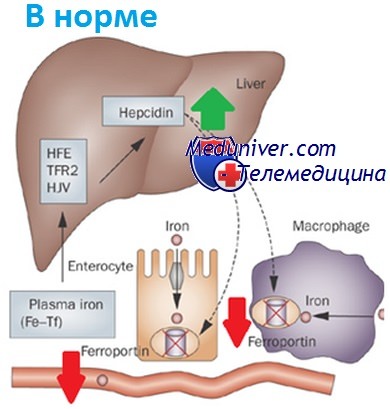
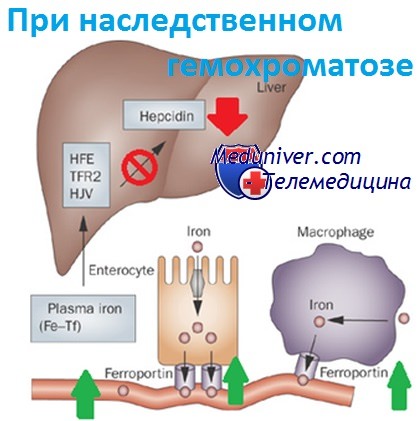
Патогенез наследственного гемохроматоза
Наследственный гемохроматоз — заболевание, связанное с избытком железа. Запасы железа определяются в основном поглощением его из пищи энтероцитами тонкого кишечника и выходом эндогенного железа из макрофагов, фагоцитирующих эритроциты.
Освобождение железа энтероцитами и макрофагами регулируется циркулирующим гормоном обмена железа, гепсидином, синтезируемым в печени и блокирующим поглощение железа, когда его достаточно. Мутантный белок HFE создает помехи сигналам гепсидина, что приводит к стимуляции энтероцитов и макрофагов к выбросу железа. Таким образом, организм продолжает усваивать железо и использовать его повторно, несмотря на его избыток.
Симптоматика избытка железа развивается лишь у небольшого числа лиц с двумя мутациями в гене HFE. Ранние симптомы включают утомляемость, боли в суставах, снижение либидо и боли в животе. Дополнительные признаки — выявление при обычном обследовании повышенного насыщения трансферрина железом или ферритина. Поздние признаки избытка железа — гепатомегалия, цирроз, печеночно-клеточная карцинома, сахарный диабет, кардиомиопатия, гипогонадизм, артрит и повышенная пигментация кожи. У мужчин симптомы появляются в возрасте 40-60 лет.
Считают, что у женщин симптоматика проявляется вдвое или в десять раз реже, чем у мужчин, симптомы могут не проявиться даже в постменопаузе. Прогноз для пациентов, диагностированных и начавших лечение до развития цирроза печени, отличный. Больные циррозом, получающие эффективное лечение кровопусканиями, все же имеют 10-30% риска развития опухоли печени.
Особенности фенотипических проявлений наследственного гемохроматоза:
• Возраст начала: 40-60 лет у мужчин; в постменопаузе у женщин
• Утомляемость, слабость, гиперпигментация («бронзовая кожа»), сахарный диабет, цирроз, кардиомиопатия
• Высокая насыщенность трансферрина сыворотки железом
• Высокий ферритин сыворотки
Лечение наследственного гемохроматоза
Индивидуумам с генотипом группы риска следует ежегодно контролировать уровень ферритина сыворотки крови. Если содержание ферритина превышает 50 нг/мл, показано кровопускание для удаления некоторого количества крови и поддержания рекомендованной нормальной концентрации ферритина. Кровопускание повторяют до тех пор, пока не будет достигнута нормальная концентрация ферритина. Невозможность достичь нормальной концентрации ферритина в течение 3 мес от начала кровопусканий — плохой прогностический признак.
Как только концентрация ферритина станет ниже 50 нг/ мл, поддерживающие кровопускания проводят каждые 3-4 мес у мужчин и каждые 6-12 мес у женщин. Больным с клиническими проявлениями и начальной концентрацией ферритина более 1000 нг/мл выполняют биопсию печени для уточнения наличия цирроза. Кровопускания пациентам с биохимическими отклонениями необходимо проводить еженедельно, пока гематокрит не составит 75% начального, а концентрация ферритина станет ниже 50 нг/мл.
Риски наследования наследственного гемохроматоза
Наследственный гемохроматоз — аутосомно-рецессивное заболевание с неполной пенетрантностью. Сибсы больного имеют 25% шанс иметь две мутации. Ребенок больного — облигатный носитель с 5% риском иметь две мутации, если оба родителя европеоиды. Из-за очень низкой пенетрантности этой болезни тотальный популяционный скрининг на наличие мутаций гена HFE не считают целесообразным.
Тем не менее из-за распространенности заболевания, неточной определенности пенетрантности и доступности легкого и эффективного лечения, может оказаться оправданным однократное определение насыщения трансферрина сыворотки и концентрации ферритина среди взрослых мужчин северо-европейского происхождения.
Пример наследственного гемохроматоза. С.Ф., 30-летний ранее здоровый мужчина европейского происхождения, направлен на консультацию в клинику генетики, поскольку у его 55-летнего отца только что диагностирован цирроз печени, вызванный наследственным гемохроматозом. Анамнестические сведения и данные медицинского осмотра в норме.
Насыщение трансферрина железом оказалось 48% (в норме 20-50%). Уровень ферритина сыворотки крови также в норме (